·论 著·
申志国1,2,黄碧霞1,陈鹏瑀1,修 荣1*(1.河北医科大学药学院物理化学教研室,河北 石家庄 050017; 2.河北省邯郸市峰峰牛儿庄矿社区管理处医院药剂科,河北 邯郸 056201)
[摘要] 目的建立一种测定盐酸雷尼替丁药物含量的新方法。方法以盐酸雷尼替丁为模板分子,邻苯二胺和甲基丙烯酸为功能单体,采用循环伏安电聚合法,制备盐酸雷尼替丁分子印迹膜电极,采用差分脉冲伏安法考察峰电流与盐酸雷尼替丁溶液浓度的关系。结果盐酸雷尼替丁在3.010×10(-7)~6.172×10(-6) mol/L浓度范围内,峰电流与其浓度呈良好的线性关系,线性方程为Ip(μA)=-2.423c+0.000 02(r=0.995 1)。结论该电极具有良好的选择性、重现性、稳定性、准确性,可用于盐酸雷尼替丁药物含量的实际测定。
[关键词] 雷尼替丁;分子印迹;循环伏安;电极
doi:10.3969/j.issn.1007-3205.2016.03.015
盐酸雷尼替丁是临床常用的H2受体拮抗剂,可抑制基础胃酸分泌以及由组胺、五肽胃泌素、咖啡、胰岛素、乙酰胆碱和进食引起的胃酸分泌,主要用于治疗消化性溃疡。目前,盐酸雷尼替丁原料及制剂的测定方法主要有高效液相色谱法(high performance liquid chromatography,HPLC)[1-3]、紫外分光光度法(Ultravioletand visiblespectra,UV)[1,4]、液相色谱-电喷雾质谱法(Liquid chromatography-electrospray ionizaiton mass spectrometry ,LC-ESI-MS)[5]等。HPLC、LC-ESI-MS法虽然测定结果准确,但存在检测成本高、操作繁琐、检测时间长等问题。UV法虽然操作简单,但难以排除其他物质及杂质的干扰,选择性较差,结果准确度不高[6]。分子印迹技术(molecularly imprinted technique,MIT)[7-9]是一种制备对目标分子具有高度识别性的聚合物技术。由MIT制备的分子印迹聚合膜,作为电化学传感器的识别元件,由于选择性高、抗干扰能力强,已成为电化学传感器制备领域研究的热点。分子印迹膜传统的制备方法存在着许多缺点,如膜的厚度不易控制,目标分子不易洗脱等。电化学聚合法可在电极上直接成膜,膜的厚度均匀、可控,膜在电极表面附着牢固,结构稳定。常采用的电化学聚合法是循环伏安扫描、恒电流和恒电位法等。本研究采用循环伏安法(cyclic voltammetry,CV)研制盐酸雷尼替丁分子印迹膜电极。该电极制备简单,成本低廉,测定快速、准确,为测定盐酸雷尼替丁药物的含量建立了一种新方法。
1.1 仪器 CHI660C型电化学工作站(上海辰华仪器有限公司);超声清洗仪(昆山市超声仪器有限公司);恒温磁力搅拌器(郑州长城科工贸有限公司);玻碳电极(GCE,Φ=4 mm);饱和甘汞电极;铂丝电极。
1.2 原料及试剂 盐酸雷尼替丁原料药(99%,石家庄制药集团);邻苯二胺、甲基丙烯酸(阿拉丁试剂);其余试剂均为分析纯。
1.3 实验方法
1.3.1 缓冲溶液 配制磷酸盐缓冲液(phosphate buffered saline,PBS,pH=6.98)和 5 mmol/L K3Fe(CN)6/K4Fe(CN)6(含0.2 mol/L KCl)溶液。
1.3.2 玻碳电极的预处理 在鹿皮上将玻碳电极分别用1.0、0.3、0.05 μm的氧化铝粉末抛光,再依次用蒸馏水、丙酮、硝酸/水(体积比为1∶1)、蒸馏水超声清洗5 min,然后将电极放入5 mmol/L K3Fe(CN)6/K4Fe(CN)6(含0.2 mol/L KCl )溶液中,在电位范围为-0.3~0.7 V内,进行CV扫描至曲线稳定,将电极取出,用蒸馏水洗净备用。
1.3.3 盐酸雷尼替丁印迹与非印迹修饰电极的制备 以盐酸雷尼替丁为模板分子,邻苯二胺、甲基丙烯酸为功能单体,进行CV电聚合反应。以玻碳电极为工作电极,饱和甘汞电极为参比电极,铂丝电极为对电极,将三电极工作体系置于含有盐酸雷尼替丁(0.01 mol/L)、邻苯二胺(0.01 mol/L)、甲基丙烯酸(0.01 mol/L)的PBS(pH=6.98)中,在-0.3~0.7 V电势范围内进行CV扫描,扫描速率为50 mV/s,扫描15圈后,将电极取出置于正十二硫醇溶液中浸泡8 h后,用甲醇洗脱10 min,即得盐酸雷尼替丁分子印迹膜电极。非印迹修饰电极的制备除不加模板分子外,其余步骤同上。
1.3.4 检测方法 印迹膜电极在使用前,必须在盐酸雷尼替丁待测液中进行孵化。本研究孵化液的浓度为1.0×10-6 mol/L。以孵化后的印迹膜电极为工作电极,饱和甘汞电极为参比电极,铂丝电极为对电极,以5 mmol/L K3Fe(CN)6/K4Fe(CN)6(含0.2 mol/L KCl )溶液为检测底液,加入适量浓度的盐酸雷尼替丁,进行微分脉冲伏安法(differential pulse voltammetries ,DPV)测定。每次测定后,将电极置于甲醇中磁力搅拌浴洗脱20 min,除去盐酸雷尼替丁分子以备下次使用。
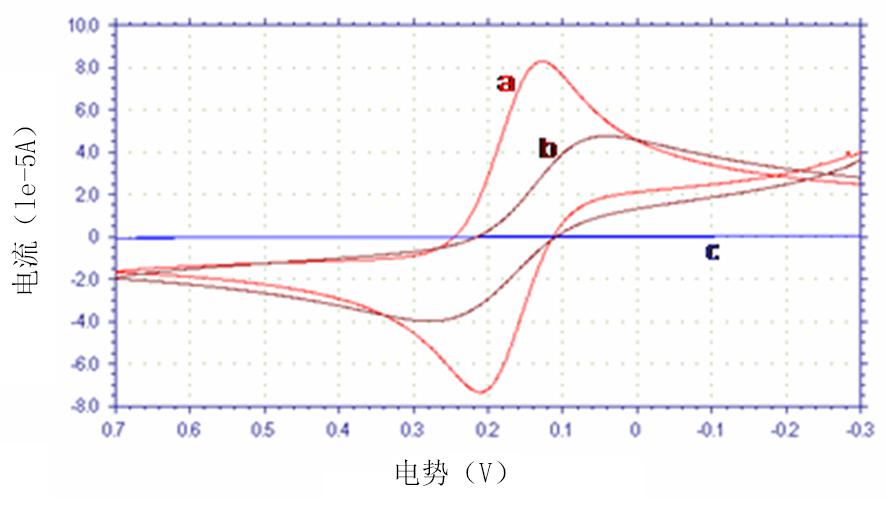
2.1 不同电极的循环伏安表征 在5 mmol/L K3Fe(CN)6/K4Fe(CN)6(含0.2 mol/L KCl )溶液中分别对裸玻电极a、洗脱模板分子后的印迹膜电极b、未洗脱的印迹膜电极c进行循环伏安表征。裸玻电极a有较大的氧化还原峰电流;b电极峰电流小于a电极,而c电极峰电流基本呈一条直线(图1)。这说明c电极表面由于被印迹分子膜完全覆盖,铁离子很难进入到电极表面,氧化还原反应很难进行,因而无峰电流。洗脱模板分子后的电极b,由于电极表面存在“空穴”,铁离子可通过空穴在电极表面发生氧化还原反应,因此有明显的峰电流。但由于模板分子不可能完全除去,故峰电流比裸玻电极a低。

图1 不同电极循环伏安图
a.裸玻电极;b.去除模板分子后的电极;c.未洗脱的印迹膜电极
Figure 1 Cyclic voltammograms of different electrodes
2.2 不同修饰电极的交流阻抗 交流阻抗法是研究电极表面特性时一种很有效的方法[10]。不同电极在5 mmol/L K4Fe(CN)4/K3Fe(CN)6 溶液中的交流阻抗图(electrochemical impedance spectroscopy,EIS)(图2)。其半圆的直径相应于印迹膜的电阻,半圆的直径越小,说明氧化还原反应进行时膜的阻抗越小,裸玻电极a的阻抗最小,未洗脱的印迹膜电极e由于表面被致密的印迹膜覆盖,阻抗最大,这与CV法表征结果一致 。加入不同浓度的盐酸雷尼替丁溶液,印迹膜的“空穴”被模板分子不同程度的封闭,随着浓度的增加,半圆直径增大,阻抗增加,见曲线c和d。上述变化表明了分子印迹膜表面状态的变化。
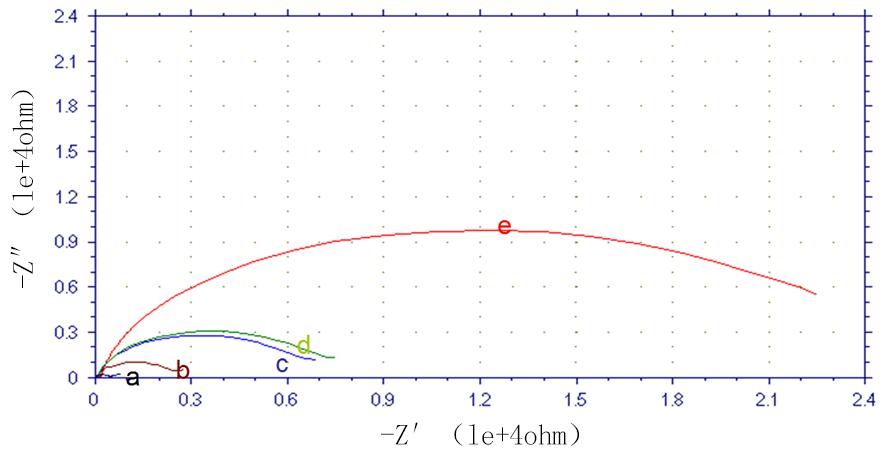
图2 不同修饰电极在5 mmol/L K4Fe(CN)4/K3Fe(CN)6溶液中的电化学阻抗图
a.裸玻电极;b.去除模板分子后的电极;c.2.315×10-6 mol/L;d.2.600×10-6 mol/L;e.未洗脱的印迹膜电极
Figure 2 Electrochemical important spectroscopy of different modified electrodes in 5 mmol/L K4Fe(CN)4/K3Fe(CN)6 (pH=8.0) solution
2.3 洗脱时间的选择 用最优洗脱液甲醇洗脱电极20 min,CV扫描曲线基本保持不变,说明模板分子基本去除。因此洗脱时间为20 min。
2.4 缓冲液最佳pH的选择 将洗脱后的电极置于一系列pH分别为5.0、6.0、7.0、8.0、9.0和10.0,盐酸雷尼替丁浓度为0.01 mol/L的PBS中,在5 mmol/L K3Fe( CN)/K4Fe(CN)6溶液中,进行CV扫描,考察酸碱度对电极印迹膜性能的影响。结果显示,当pH为7.0时,氧化还原峰峰形较好,且响应电流最大,因此选择pH为7.0的PBS溶液为检测溶液。
2.5 电极孵化时间的确定 将洗脱后的印迹膜电极置于1.0×10-6 mol/L 盐酸雷尼替丁溶液中,采用DPV法,考察峰电流与孵化时间的关系。扫描显示,孵化时间由5 min增加到到12 min时,峰电流不断上升,但12 min后峰电流基本不变。表明电极表面空穴在12 min时基本被模板分子覆盖,因此电极的孵化时间选择为12 min。
2.6 线性方程与标准曲线 随着盐酸雷尼替丁浓度的增加,模板分子占据空穴的数目增加,峰电流逐渐减小。在3.010×10-7~6.172×10-6 mol/L浓度范围内,峰电流与盐酸雷尼替丁浓度呈良好的线性关系(图3),线性回归方程为Ip(μA)=-2.423c+ 0.000 02(r=0.995 1)。检测限为6.5×10-8 mol/L。盐酸雷尼替丁浓度 (μmol/L) a~j:0.301、0.486、0.634、0.835、2.374、3.384、4.158、5.030、5.675、6.172
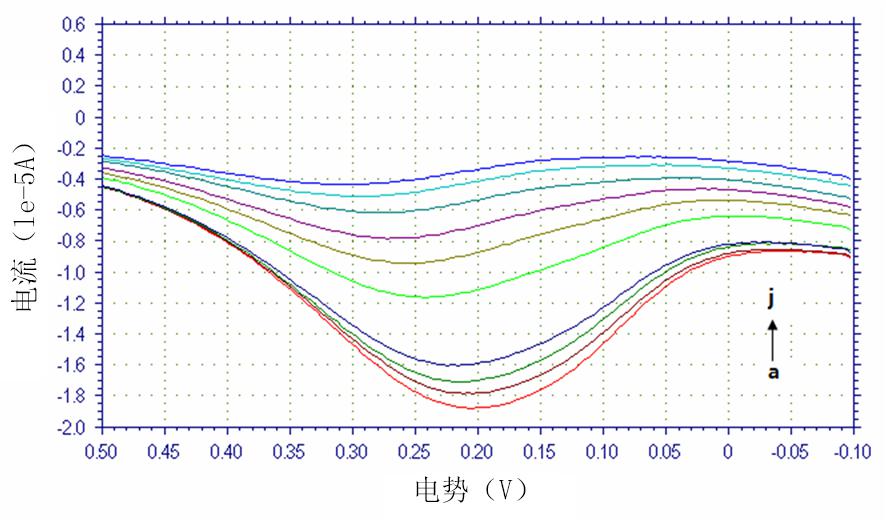
图3 不同浓度盐酸雷尼替丁微分脉冲伏安扫描图
Figure 3 Differential pulse voltammetries of different ranitidine hydrochloride concentrations
2.7 干扰实验 在最佳实验条件下,向浓度为1.0×10-6 mol/L的6份盐酸雷尼替丁溶液中,依次加入浓度为3.0×10-3 mol/L的NH4Cl、KNO3、Na2CO3、MgCl2、CaCl2、Na2SO4物质。采用DPV扫描,以峰电流的变化值小于±5%作为判定是否干扰电极性能的标准[11]。结果表明,大于盐酸雷尼替丁浓度1 000倍的上述物质对电极干扰很小,说明电极抗干扰能力较强。
2.8 重现性与稳定性 电极在盐酸雷尼替丁浓度为1.0×10-6 mol/L 的溶液中平行测定5次,其DPV扫描曲线峰电流的相对标准偏差(relative standartion,RSD)为3.78%。表明电极具有良好的重现性。电极放置2周后,峰电流下降了12%。表明该印迹电极有良好的稳定性。
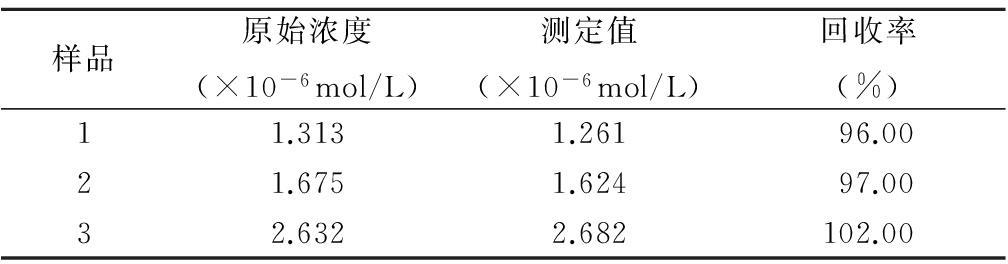
2.9 回收率测定 在最佳测定条件下,配制一定浓度盐酸雷尼替丁标准溶液进行回收率实验,每份溶液平行测定5次,取其平均值,回收率在96.00%~102.0%之间,见表1。
表1 回收率测定结果
Table 1 Determination results of recovery with the sensor
采用CV法制备的印迹膜厚度,可通过聚合时间进行控制。聚合时间长,印迹膜太厚,模板分子不易洗脱。聚合时间短,印迹膜太薄,印迹空穴结构不稳定,洗脱时极易损坏。因此,聚合时间对印迹膜的性能至关重要,要反复实验才能确定。
对不同浓度的溶液进行DPV扫描时,每次扫描完毕,电极需洗脱至模板分子基本除去(CV曲线基本不变)。
本研究采用CV法研制的盐酸雷尼替丁分子印迹膜电极,具有制作简便、成本低廉、选择性高、测定快速准确的特点,可用于盐酸雷尼替丁药物含量的检测,在临床、制药和环境监测等领域具有良好的应用前景。
[参考文献]
[1] 国家药典委员会.中国药典[S].北京:中国医药科技出版社,2010:524,583-585,796.
[2] 石笑弋,王伟姣,李昌亮.高效液相色谱法测定复方雷尼替丁胶囊中盐酸雷尼替丁的含量[J].中南药学,2013,11(8):613-616.
[3] 魏素,黄玉昌,吴芳花.HPLC法测定复方雷尼替丁的含量及其有关物质的探讨[J].中国药师,2010,13(10):1483-1485.
[4] 王琼芬,李海英. 盐酸雷尼替丁胶囊的差示紫外分光光度测定[J].中国医药工业杂志,1999,30(8):373,372.
[5] 张振南,王贤亲,孙哲,等.LC-ESI- MS测定血浆中盐酸雷尼替丁的含量[J].中国卫生检验杂志,2009,11(11):2564-2565.
[6] 张子葳,严建洋,蒋磊,等.盐酸雷尼替丁含量测定的研究进展[J].西北药学杂志,2011,26(3):226-229.
[7] 张自一,冯丽霞,修荣.尼群地平分子印迹聚合物的制备和热力学性能研究[J].河北医科大学学报,2013,34(7):796-799.
[8] 阚文涛,李欣,蹇源,等.分子印迹技术在药物缓释领域的研究进展[J].材料导报A,2014,28(7):42-45,51.
[9] 邱思聪,陈孝建,陈鹏飞,等.分子印迹技术在食品中兽药残留分析中的应用[J].食品安全质量检测学报,2015,6(6):2248-2255.
[10] 韩俊凤,董维广,赵平平,等.铋膜修饰玻碳电极伏安法测定微量铅(Ⅱ)[J].分析科学学报,2012,28(1):107-109.
[11] 王琳,谭学才,赵丹丹,等.以马来松香丙烯酸乙二醇酯为交联剂的咖啡因分子印迹电化学传感器[J].高等学校化学学报,2012,33(8):1708-1713.
(本文编辑:许卓文)
SHEN Zhi-guo1,2, HUANG Bi-xia1, CHEN Peng-yu1, XIU Rong1*
(1.Department of Physisical Chemistry,the School of Pharmaceutical, Hebei Medical University,Shijiazhuang 050017, China; 2.Department of Pharmacy, Hospital of Community Management Office, Niuerzhuang Coalmine, Fengfeng Group, Handan 056201, China)
[Abstract] Objective To establish a new method for determination of ranitidine hydrochloride drug content. Methods By using ranitidine hydrochloride as template, and using o-pheny-lenediamine as well as methacrylic acid as functional monomer, we prepared the molecular imprinted polymer membrane sensor of ranitidine hydrochloride on the surface of a glassy carbon electrode by using cyclic voltammetry(CV) electropolymerization method. Electrochemical behavior of the sensor was characterized by CV and differential pulse voltammetries(DPV). Results The peak currents of DPV and concentration have a good linear relationship in the range of 3.010×10(-7)-6.172×10(-6) mol/L, and the linear equation was Ip(μA)=-2.423c+0.000 02(r=0. 995 1). Conclusion The sensor displayed good selectivity, excellent reproducibility, stability, accuracy, and it could be used to measure ranitidine hydrochloride drug actual content.
[Key words] ranitidine; molecular imprinting; cyclic voltammograms; electrode
[中图分类号] R975.6
[文献标志码] A
[文章编号] 1007-3205(2016)03-0306-04
[作者简介]申志国(1977-),男, 河北魏县人,河北省邯郸市峰峰牛儿庄矿社区管理处医院主管药师,从事时辰药理学研究。*通讯作者。E-mail:xiurong1956@sina.com
[基金项目]河北省大学生创新创业训练计划(201410089045)
[收稿日期]2015-08-07;[修回日期]2015-09-11