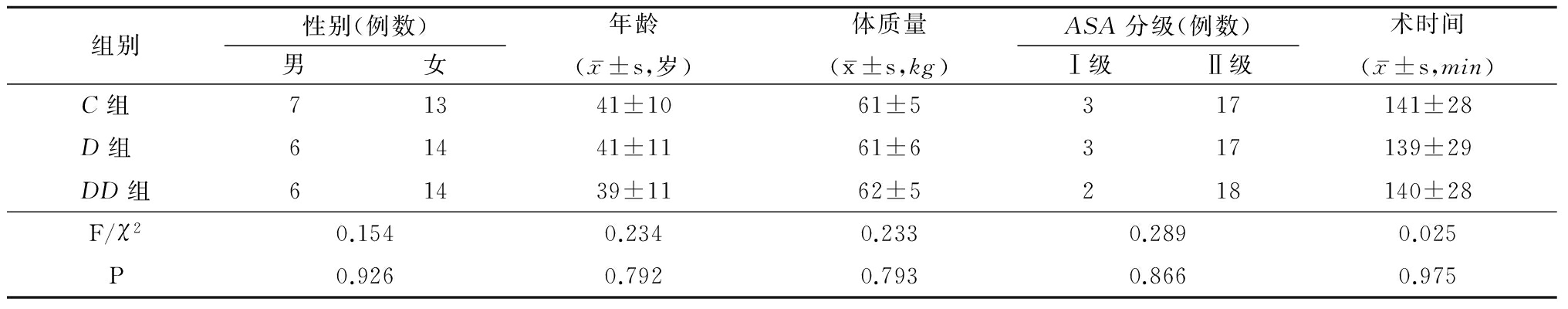
表1 3组一般资料比较
Table 1 Comparison of general information in three groups of patients (n=20)
·论 著·
张 宁1,孙保民1,程 燕2,袁矿生1
(1.冀中能源峰峰集团总医院麻醉科,河北 邯郸 056200; 2.冀中能源峰峰集团总医院输血科,河北 邯郸 056200)
[摘要]目的观察地塞米松复合右美托咪定对肌间沟臂丛神经阻滞效果的影响。方法将在肌间沟臂丛神经阻滞下行上肢骨折手术患者60例随机分为3组各20例,其中C组给予0.5%罗哌卡因,D组给予0.5%罗哌卡因+右美托咪定1 μg/kg,DD组给予0.5%罗哌卡因+右美托咪定1 μg/kg+地塞米松10 mg,药液均为25 mL。分别于入室时(T0)、手术开始时(T1)、手术开始30 min 时(T2)和手术结束时(T3)记录患者心率(hear rate,HR)、平均动脉压(mean arterial pressure,MAP)、脉搏氧饱和度(oxygen saturation,SpO2)、OAA/S评分,并记录感觉和运动神经阻滞起效时间、持续时间及心血管事件、过度镇静、恶心呕吐等不良反应。结果3组OAA/S评分、HR组间、时点间差异有统计学意义(P<0.05),而组间·时点间交互作用差异无统计学意义(P>0.05);3组MAP时点间差异有统计学意义(P<0.05),而组间与组间·时点间交互作用差异无统计学意义(P>0.05);3组SpO2组间、时点间、组间·时点间交互作用差异均无统计学意义(P>0.05)。与C组比较,D和DD组感觉和运动神经阻滞起效时间缩短,持续时间延长(P<0.05);与D组比较,DD组感觉和运动神经阻滞持续时间延长(P<0.05)。DD组恶心呕吐发生率低于D组。D组和DD组少数患者出现窦性心动过缓。结论地塞米松复合右美托咪定可以增强罗哌卡因的镇痛效果,缩短起效时间,延长作用时间,减少不良反应,但可能诱发心动过缓。
[关键词]地塞米松;右美托咪啶;麻醉
doi:10.3969/j.issn.1007-3205.2016.08.017
臂丛神经阻滞是一种常见的局部麻醉技术,广泛应用于上肢手术,但存在焦虑情绪、阻滞不全及心脏毒性等风险[1]。提高神经阻滞的效果和安全性一直为临床研究的热点。有研究表明,局部麻醉药中复合右美托咪定可缩短起效时间,延长持续时间[2]。在神经阻滞中加入地塞米松可延长感觉和运动阻滞持续时间,但对镇静、镇痛协同作用不及右美托咪定[3-4]。本研究在罗哌卡因中分别加入右美托咪定1 μg/kg及地塞米松10 mg,观察这2种药物在臂丛神经阻滞中对罗哌卡因阻滞效果的影响,旨在为临床应用提供参考。
1.1 一般资料 选择2014年12月—2015年9月本院择期行肌间沟臂丛神经阻滞下上肢手术的患者60例,美国麻醉师协会( American Society of Anesthesiologists,ASA)分级Ⅰ级或Ⅱ级,年龄20~60岁,平均(40.3±10.7)岁,体质量40~70 kg。排除标准:患有肝肾功能疾病、糖尿病神经病变、凝血功能障碍、穿刺部位感染、肥胖、怀孕者。采用随机双盲法将患者均分为3组各20例。C组给予0.5%罗哌卡因,D组给予0.5%罗哌卡因+右美托咪定1 μg/kg,DD组给予0.5%罗哌卡因+右美托咪定1 μg/kg+地塞米松10 mg,药液均为25 mL。3组性别构成比、年龄、体质量、ASA分级和手术时间差异无统计学意义(P>0.05),见表1。
本研究已获本院医学伦理委员会批准,并与患者或其家属签署知情同意书。
表1 3组一般资料比较
Table 1 Comparison of general information in three groups of patients (n=20)

1.2 麻醉方法 所有患者术前禁饮食且未术前用药。入室后常规监测心电图、心率(heart rate,HR)、平均动脉压(mean arterial pressure,MAP)、脉搏氧饱和度(oxygen saturation,SpO2),面罩吸氧,氧流量2~4 L/min。建立静脉通路,输入乳酸林格液。患者去枕仰卧位,头偏向对侧,手臂贴体旁,手尽量下垂暴露颈部。微抬头以显露胸锁乳突肌,手指触摸到胸锁乳突肌锁骨端后缘,向后外侧滑过前斜角肌肌腹,即为肌间沟间隙。应用便携式超声(13~6 MHz 25 mm宽频线阵探头)对肌间沟臂丛神经进行扫描,在前斜角肌的外下方找到低回声目标神经干后,应用神经刺激仪(德国贝朗公司)和绝缘的短斜面22号刺激针,初始电流为1.0 mA,当刺激针诱发出目标神经支配的相应肌肉收缩后,将电流减至0.25~0.40 mA,如仍有肌颤视为定位准确。将刺激针从超声探头侧外方缓慢进针,确保针体与超声探头长轴在一条直线上,在超声图像的引导下调整进针深度及角度。首先刺激针直接穿刺到肌间沟臂丛神经下干,回抽无血液、脑脊液、气体,注入局部麻醉药9 mL,然后阻滞针部分退出,依次在中干、上干神经束间分别注射局部麻醉药8 mL。采用多点注射方法,注药过程中尽量使药液包绕在目标神经的周围扩散,总的注药时间为1~2 min。所有麻醉操作均由资深麻醉医师完成。若术中出现低血压(收缩压较基础值降低30%)或心动过缓(HR<50次/min),则静脉注射麻黄碱6 mg或阿托品0.5~1.0 mg;若出现呼吸抑制(SpO2<90%),则面罩加压辅助呼吸;若镇痛不足,则静脉给予舒芬太尼0.2 μg/kg,如果仍无法完成手术,则更改麻醉方式为全身麻醉。
1.3 观察指标
1.3.1 记录各时点血流动力学变化及呼吸情况 分别于入室时(T0)、手术开始时(T1)、手术开始30 min 时(T2)和手术结束时(T3)记录患者HR、平均动脉压(mean arterial pressure,MAP)、SpO2、清醒镇静评分法(Observer′s Assessmont of Alertness/Sedation Scale,OAA/S)评分。OAA/S评分标准[5]:1分为完全清醒,对正常呼名的应答反应正常;2分为对正常呼名的应答反应迟钝;3分为对反复大声呼名有应答反应;4分为对轻拍身体才有应答反应;5分为对伤害性刺激有应答反应。非全身麻醉手术患者,OAA/S评分≥4分时为过度镇静,记录过度镇静的发生情况。
1.3.2 记录视觉模拟评分法(Visual Analogue Scale,VAS)评分及感觉阻滞起效、持续时间 于注药完毕后每隔1 min 采用针刺法测定桡神经(虎口)、正中神经(大鱼际)、尺神经(小鱼际)支配区的痛觉缺失情况,记录针刺时VAS评分(0分为无痛,<3分为良好,3~4分为基本满意,>5分为差,10分为无法忍受的剧痛),记录感觉阻滞起效时间(注药结束至VAS评分≤3分)、感觉阻滞持续时间(注药结束至痛觉恢复到VAS评分>3分)。
1.3.3 记录运动阻滞起效、持续时间 采用改良Bromage运动分级法,于注药完毕后每隔1min测定一次肘关节的运动阻滞程度(0级为无麻痹;1级为不能屈肘关节;2级为不能抬上肢;3级为不能屈指关节)[6]。记录运动阻滞起效时间(注药结束至出现3级时间)、感运动阻滞持续时间(注药结束至出现0级时间)。
1.3.4 记录不良反应 记录心血管事件、恶心呕吐、膈神经麻痹、局部麻醉药中毒、气胸等不良反应的发生情况。
1.4 统计学方法 应用SPSS 16.0统计学软件进行数据分析。计量资料比较分别采用单因素方差分析、q检验及重复测量的方差分析;计数资料比较采用χ2检验。P<0.05为差异有统计学意义。
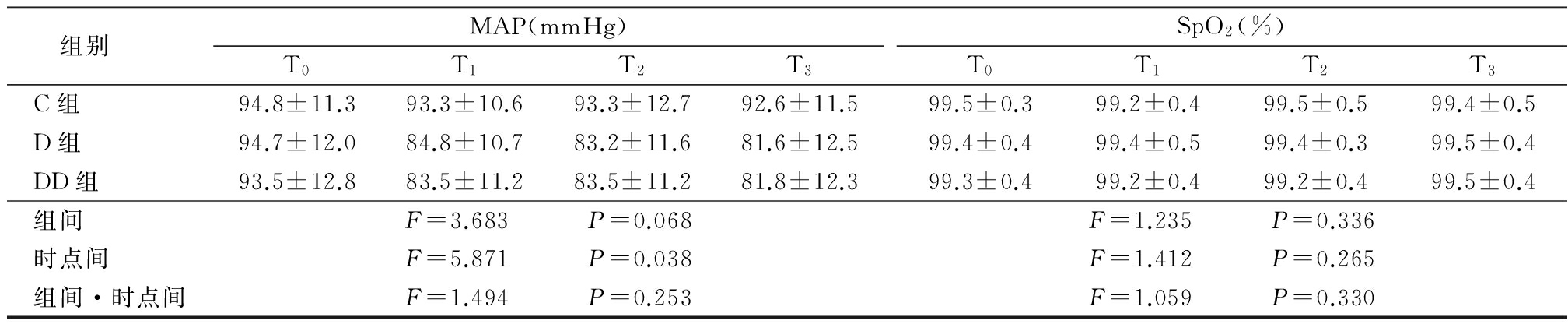
2.1 3组镇静效果和血流动力学比较 3组OAA/S评分、HR组间、时点间差异有统计学意义(P<0.05),而组间·时点间交互作用差异无统计学意义(P>0.05)。3组MAP时点间差异有统计学意义(P<0.05),而组间与组间·时点间交互作用差异无统计学意义(P>0.05)。3组SpO2组间、时点间、组间·时点间交互作用差异均无统计学意义(P>0.05)。见表2。
表2 3组镇静效果和血流动力学指标比较
Table 2 Sedative effect and hemodynamic index in three groups of patients![]()
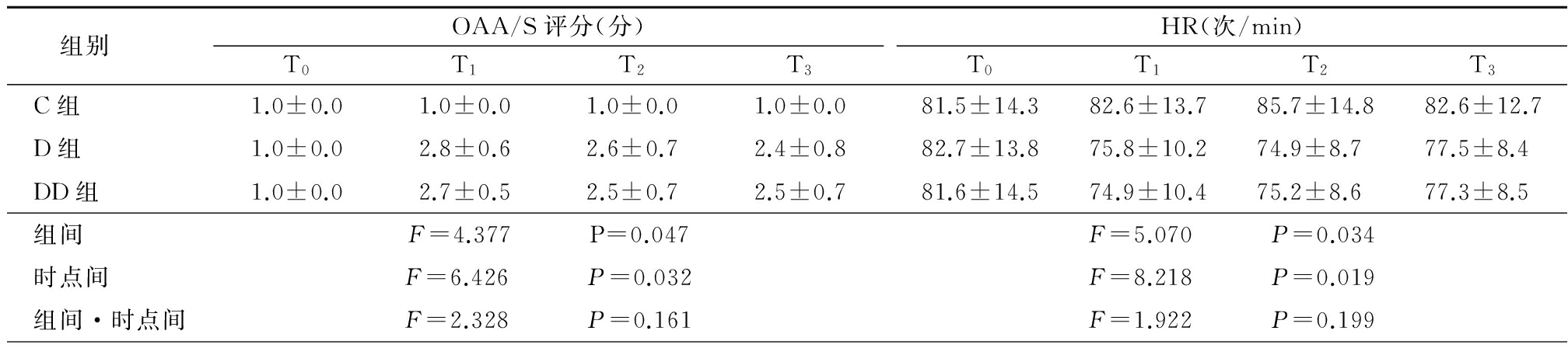
表2 (续)
2.2 3组臂丛神经阻滞效果比较 与C组比较,D和DD组感觉和运动神经阻滞起效时间缩短,持续时间延长(P<0.05);与D组比较,DD组感觉和运动神经阻滞持续时间延长(P<0.05),感觉和运动阻滞起效时间差异无统计学意义(P>0.05)。见表3。
表3 3组臂丛神经阻滞效果比较
Table 3 Comparison of the effect of brachial plexus block in the three groups![]()
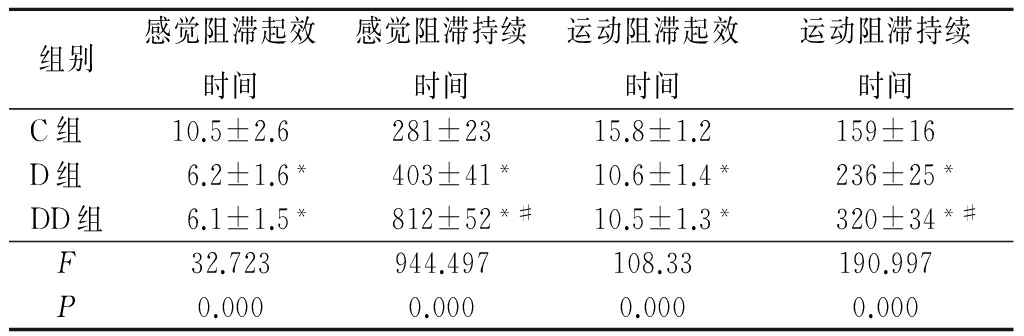
*P<0.05与C组比较 #P<0.05与D组比较(q检验)
2.3 3组不良反应比较 D组窦性心动过缓发生率5.0%(1例),恶心呕吐发生率10.0%(2例);DD组窦性心动过缓发生率5.0%(1例),未见恶心呕吐发生;C组未见不良反应发生。3组不良反应差异无统计学意义(χ2=0.278,P=0.598)。
肌间沟臂丛神经阻滞用于上肢手术常出现阻滞不全,特别是尺神经支配区域。本研究结果显示,在超声引导下行肌间沟臂丛神经阻滞效果确切、并发症少。说明超声可清晰显示臂丛各神经干的图像,可将药物准确注射在神经周围且避免神经损伤及误穿血管,确保了臂丛各神经干的药量。
臂丛神经阻滞时患者多伴有不同程度的精神紧张、焦虑和恐惧感,可诱发强烈的应激反应,因此辅助一定程度的镇静是有必要的。右美托咪定是一种高选择性α2受体激动剂,其α2∶α1受体活性(1 300∶1)远高于可乐定(39∶1),从而减少不必要的α1受体的不良反应[7-8]。右美托咪定通过与外周和中枢神经系统突触前膜的α2受体作用,产生交感阻断和副交感兴奋作用,抑制去甲肾上腺素的释放,从而降低HR和血压,产生镇静抗焦虑作用。右美托咪定可能导致的不良反应,如低血压和心动过缓,随剂量的增加而加重。
本研究参照相关文献[9]并结合临床经验,选择复合右美托咪定剂量为1 μg/kg。本研究中的有创操作均在B超引导下进行,不仅能有效避免对神经的机械性损伤,也降低了局部麻醉药中毒的风险及右美托咪定快速入血导致的不良反应。虽然3组患者术中血流动力学均未出现剧烈波动,但C组仍有部分患者由于有创刺激和紧张恐惧等心理因素,造成了HR一过性的升高。在临床使用右美托咪定过程中,低血压和窦性心动过缓的发生率较高,本研究中虽未发生低血压和严重的窦性心动过缓,但仍应提高对其发生心血管不良事件的警惕。右美托咪定复合罗哌卡因用于臂丛神经阻滞,虽为患者提供了更好的术中舒适度,但D组和DD组仍有部分患者出现了轻度窦性心动过缓,可能与右美托咪定剂量有关。
右美托咪定作用于突触前后交感神经末梢和中枢神经系统,从而降低交感神经兴奋性,减少去甲肾上腺素释放,具有镇静、镇痛、抗交感等多种药理作用和独特的“清醒镇静”而无呼吸抑制的特点。右美托咪定复合局部麻醉药用于臂丛神经阻滞不仅可加强术中镇静,而且还有增强神经阻滞效果、增加患者舒适度的作用[4]。右美托咪定在周围神经阻滞的确切作用机制尚未明确,其可能存在的主要机制有[10-11]:①右美托咪定可阻断河豚毒素敏感性电压门控钠通道和四乙基胺敏感性钾通道,抑制神经细胞膜动作电位的产生,且右美托咪定局部用药可明显降低罗哌卡因臂丛神经阻滞的半数有效浓度,均提示其具有局部麻醉药样效应;②抑制神经末梢去甲肾上腺素的释放,兴奋胆碱能神经,起协同抗伤害作用;③右美托咪定脂溶性较高,易被臂丛神经周围脂肪组织吸收入血,作用于脑干蓝板核的α2受体,产生镇静作用,同时降低机体对伤害刺激的兴奋性;④右美托咪定可通过激动血管的α2受体,引起局部血管收缩,从而延缓局部麻醉药的吸收,延长局部麻醉药的作用时间。
本研究结果表明,与C组比较,D组和DD中右美托咪定在增强罗哌卡因阻滞效果的同时能够缩短感觉、运动神经阻滞的起效时间,延长作用时间。这可能与右美托咪定多种药理作用有关。研究表明,右美托咪定不论给药途径(外周神经阻滞、椎管内阻滞以及静脉)如何均可产生良好的镇静、镇痛和抗交感作用[4]。
有研究发现,地塞米松应用于外周阻滞对神经结构和功能没有影响,可以安全地复合局部麻醉药应用于神经阻滞中[10]。地塞米松延长局部麻醉药神经阻滞作用的确切机制尚不清楚。有研究表明糖皮质激素可以使局部血管产生一定程度的收缩,从而减缓局部麻醉药的吸收,延长局部麻醉药的作用时间[3]。张大志等[3]证实地塞米松可延长罗哌卡因的神经阻滞麻醉的效果,尤以含10 mg地塞米松的罗哌卡因药液效果最显著。本研究结果显示,D组和DD组感觉和运动阻滞起效时间差异无统计学意义。表明地塞米松可延长感觉、运动阻滞持续时间,但并不能缩短臂丛神经感觉、运动起效时间。地塞米松可减轻恶心呕吐不良反应,机制可能与它抑制前列腺素合成,减少呕吐中枢5-羟色胺含量有关[12]。本研究结果表明,复合地塞米松10 mg和右美托咪定1 μg/kg比单纯加用右美托咪定延长了臂丛神经阻滞镇痛时间,且恶心、呕吐等不良反应也相应减少。
综上所述,在行肌间沟臂丛神经阻滞的罗哌卡因中加入1 μg/kg右美托咪定,能改善阻滞效果,缩短起效时间、延长持续时间;复合10 mg地塞米松能进一步延长阻滞持续时间,且不良反应减少。
[参考文献]
[1] Toju K, Hakozaki T, Akatsu M, et al. Ultrasound-guided bilateral brachial plexus blockade with propofol-ketamine sedation[J]. Anesth,2011,25(6):927-929.
[2] 李金玉,葛东健,祁宾,等.不同剂量右美托咪定混合罗哌卡因用于臂丛神经阻滞的效果[J].中华麻醉学杂志,2013,33(6):711-713.
[3] 张大志,王怀江,刘永盛,等.不同剂量地塞米松对罗哌卡因神经阻滞作用的影响[J].临床麻醉学杂志,2013,29(3):213-215.
[4] Joana Afonso,Fl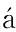 vio Reis. Dexmedetomidine:Current Role in Anesthesia and intensive care[J]. Rev Bras Anestesiol,2012,62(1):118-133.
vio Reis. Dexmedetomidine:Current Role in Anesthesia and intensive care[J]. Rev Bras Anestesiol,2012,62(1):118-133.
[5] Chernik DA,Gillings D,Laine H,et al. Validity and reliability of the observer's assessment of alertness/sedation scale:study with intravenous midazolam[J]. Clin Psychopharmacol,1990,10(4):244-251.
[6] 周俊,王汉兵,林文静,等.右美托咪啶对上肢手术患者罗哌卡因臂丛神经阻滞效果及上肢缺血再灌注损伤的影响[J].中华麻醉学杂志,2011,31(1):84-87.
[7] Agarwal S,Aggarwal R,Gupta P. Dexmedetomidine prolongs the effect of bupivacaine in supraclavicular brachial plexus block [J]. J Anaesthesiol Clin Pharmacol,2014,30(1):36-40.
[8] 杜萍,王春平,刘卫敬,等.右美托咪啶单次负荷剂量给药在肥胖患者椎管内麻醉镇静的临床观察[J].河北医科大学学报,2014,35(1):97-99.
[9] Kaur H,Singh G,Rani S,et al. Effect of dexmedetomidine as an adjuvant to levobupivacaine in supraclavicular brachial plexus block:A randomized double-blind prospective study[J]. J Anaesthesiol Clin Pharmacol,2015,31(3):333-338.
[10] Kirksey MA,Haskins SC,Cheng J,et al. Local Anesthetic Peripheral Nerve Block Adjuvants for Prolongation of Analgesia:A Systematic Qualitative Review[J]. PLoS One,2015,10(9):1-23.
[11] 李露,王晓琳,周海滨,等.右美托咪定局部用药对罗哌卡因臂丛神经阻滞半数有效浓度的影响[J].中华麻醉学杂志,2013,(33)3:328-330.
[12] Allen TK,Jones CA,Habib AS. Dexamethasone for the prophylaxis of postoperative nausea and vomiting associated with neuraxial morphine administration:a systematic review and meta-analysis[J]. Anesth Analg,2012,114(4):813-822.
(本文编辑:刘斯静)
ZHANG Ning1, SUN Bao-min1, CHENG Yan2, YUAN Kuang-sheng1
(1.Department of Anesthesiology, the General Hospital Affiliated to Jizhong Energy Fengfeng Conglomerate,Hebei Province, Handan 056200, China; 2.Department of Blood Transfusion, the General Hospital Affiliated to Jizhong Energy Fengfeng Conglomerate, Hebei Province, Handan 056200, China)
[Abstract]Objective To observe the effects of dexamethasone combined with dexmedetomidine on interscalene brachial plexus block. Methods Sixty patiens scheduled for upper extremity surgery with interscalene brachial plexus block were randomly divided into three groups, with 20 cases in each group. Control group(group C) was given 0.5% ropivacaine 25 mL; Dexmedetomidine group(group D) was received 0.5% ropivacaine+1 μg/kg dexmedetomidine 25 mL; dexamethasone combined with dexmedetomidine group(group DD) was injected with 0.5% ropivacaine +1 μg/kg dexmedetomidine and dexamethasone 10 mg 25 mL. Hear rate(HR), mean arterial pressure(MAP), oxygen saturation(SpO2) and OAA/S score at the time of entering the operating room(T0),beginning of the operation(T1), 30 min after the start of operation(T2), at the end of the surgery(T3) were observed. The onset time and duration of sensory and motor block were recorded. The adverse effects such as adverse cardiovascular events, excessive sedation, nausea and vomiting were also recorded. Results The difference in OAA/S score and HR, interblock and time dissimilarity in the three groups at the groups and time points were statistically significant(P<0.05). However, there was no significant difference in the interaction between group and time(P>0.05). In OAA/S score and HR, interblock and time dissimilarity of the three groups had statistically significant difference. There was no significant difference in interaction of interblock with time dissimilarity between the three groups. For MAP, there were statistically significant differences in time dissimilarity among the three groups(P<0.05). There was no significant difference in interblock and interaction of interblock with time dissimilarity between the three groups(P>0.05). For SpO2, there was no significant difference among the three groups(P>0.05). Compared with group C, the onset time was(P>0.05). Compared with group C, the onset time was significantly shortened, and the duration of block was prolonged(P<0.05) in group D and group DD. Compared with groups D, the duration of block was prolonged in groups DD(P<0.05). The incidence of nausea and vomiting in group DD was significantly lower than in group D. Some patients developed bradycardia in groups D and DD. Conclusion Dexamethasone combined with dexmedetomidine can enhance the analgesic effect of ropivacaine, shorten the onset time, prolong the action time, reduce the adverse reactions, but may induce bradycardia.
[Key words]dexamethasone; dexmedetomidine; anesthesia
[收稿日期]2015-11-02;
[修回日期]2015-12-03
[作者简介]张宁(1981-),男,河北邯郸人,冀中能源峰峰集团
[中图分类号]R614.4
[文献标志码]A
[文章编号]1007-3205(2016)08-0935-05
总医院主治医师,医学硕士,从事临床麻醉学研究。