表1 40例患者介入前后NIHSS评分、BI评分和mRS等评分比较![]() 分)
分)
·论著·
刘长江,李 可,张大权,李振举
(吉林大学第四医院神经外科,吉林 长春 130011)
[摘要]目的观察缺血性脑血管病患者介入治疗后的效果,探讨再发性血管事件的相关因素。方法选取缺血性脑血管病患者40例,在对患者充分术前准备后,进行支架植入术。分别于术后2 d、3个月、1年时对患者进行随访或复诊,了解术后血管再狭窄和斑块形成情况,记录终点事件,确定随访期内死亡患者原因,分析危险因素(包括高血压、糖尿病、吸烟、高血脂等)。结果40例患者共治疗血管狭窄42处,15例患者术中出现血压、心率过低,经药物治疗后均恢复正常。术后颈动脉多普勒、经颅多普勒、CT血管成像检查发现2处再狭窄,再狭窄率为4.8%。1年随访期内患者死亡1例,死因为心脏病;脑出血1例(原因为未按照医嘱服用降压药物)、脑梗死1例,均为糖尿病患者。术后3个月内患者均按照医嘱服用抗血小板药物,截至1年终点时共10例患者未按照医嘱服用药物。结论缺血性脑血管病患者,介入治疗安全有效。介入治疗后再发血管事件的危险因素可能为依从性差、糖尿病和其他多重危险因素。因此,提高患者的依从性、按时服用药物、监测和控制危险因素可减少介入治疗后血管事件的发生。
[关键词]卒中;支架植入;治疗效果;危险因素
doi:10.3969/j.issn.1007-3205.2017.11.020
文献报道我国每10万成年人当中有100~150人发生脑血管意外,其中缺血性脑血管意外的比例为80%,并且具有较高的病死率、复发率和致残率[1]。随着我国人口老龄化的加剧,缺血性脑血管病患者将持续增加。有效降低患者的病死率、复发率和致残率,可以较大改善患者的生存质量,减轻社会和家庭负担,具有重要意义。缺血性脑血管病发生的原因,主要与颈动脉系统和椎基底动脉系统的狭窄和动脉粥样硬化斑块有关[2]。传统治疗方法包括药物治疗、康复治疗和内科综合治疗,并不能从根本上逆转大血管狭窄处动脉粥样硬化斑块。血管内介入治疗技术的快速发展,为缺血性脑血管病的治疗带来新的突破,在我国介入治疗越来越普及[3]。但是目前的研究主要集中在术前评估、适应证选择、手术方法和手术并发症方面,术后的长期随访研究较少。本研究对确诊为脑血管缺血并适用于介入治疗的40例患者进行术后长期随访,旨在观察介入疗效,分析术后血管事件发生的危险因素,报告如下。
1.1 一般资料 选择2012年1月—2015年1月我院收治的缺血性脑血管病患者40例,男性23例,女性17例,年龄48~69岁,平均(52.0±3.0)岁。颅外血管症状性狭窄中度以上,无症状性狭窄重度以上,患者均签署知情同意书。
1.2 纳入标准和排除标准 纳入标准:按照1995年全国脑血管病会议制定的诊断标准,经CT或MRI检查,明确为缺血性脑血管病,且美国国立卫生研究院卒中量表(National Institute of Health stroke scale,NIHSS)评分<10分;经磁共振血管成像(magnetic resonance angiography,MRA)、CT血管成像(CT Angiography,CTA)或颈动脉彩色多普勒检查发现血管狭窄者[影像学评估狭窄的计算方法:狭窄率(%)=(D-d)/D×100%,其中D为原管腔直径,d 为狭窄处剩余管腔直径,若同一血管内存在多处斑块或狭窄,则测量狭窄最严重部位的d;狭窄程度采用北美症状性颈动脉内膜剥脱试验(North American Symptomatic Carotid Endarterectomy Trial,NASCET) 标准共分为4级,0~49%为轻度狭窄、50%~69%为中度狭窄、70%~99%为重度狭窄、100%为闭塞]。排除标准:①年龄<18岁的患者;②肌纤维发育不良、系统性血管炎、多发大动脉炎等所致颈动脉狭窄患者。
1.3 方法
1.3.1 术前检查 进行脑功能缺损和残障、日常生活能力量表(Activity of Daily Living Scale,ADL) 评分、改良Rankin量表(modified Rankin Scale,,mRS)评分、BI指数(barthel index,BI)评分,收集危险因素卒中风险评分量表等。辅助检查:所有患者先进行MRA或CTA血管筛查后,有介入指征者进一步行全脑血管造影及颈部、脑血管超声检查,显示其狭窄血管部位、长度,狭窄处直径,血流速度以及动脉腔内动脉硬化的厚度、范围、性质。
1.3.2 MRA检查 应用超导型高场3.0T磁共振仪,采用水平位及斜位扫描方法,层厚1 mm。选择高浓度造影剂40~60 mL,在肘部静脉用高压注射器快速注射,感兴趣区设在主动脉弓下的降主动脉。 数字减影血管造影(digital subtraction angiography,DSA)检查:应用Philips 3D-Allura型数字血管造影机,使用示踪图超选导入双侧锁骨下动脉、双侧颈总动脉、双侧颈内动脉、双侧椎动脉,行常规血管造影,必要时加做旋转血管造影,并充分评估侧支循环情况。
1.4 治疗方法 ①术前准备:术前口服阿司匹林100 mg/d,氯吡格雷75 mg/d,3~5 d。术前6 h禁食水,术前0.5 h肌肉注射苯巴比妥100 mg,阿托品0.5 mg。②手术操作:在患者清醒状态下,局部麻醉后行股动脉穿刺,放置8F(椎动脉6F)血管鞘成功后,全身肝素化,在导丝引导下将指引导管选入病变血管近端,再次造影,确认狭窄部位;然后,导丝引导下指引导管送达狭窄近端处2~3 cm;在路径图指导下将微导丝穿越狭窄部位,导丝头端放置于颈内动脉远端并固定位置,监视下沿微导丝小心将保护装置送达狭窄远端后释放(椎动脉支架无此过程),撤出微导丝,选用适合球囊放置于血管狭窄段,透视下用压力泵向球囊内注入造影剂,扩张满意后立即减压,同时密切观察患者血压、心率变化,必要时静脉应用阿托品、多巴胺治疗;撤出球囊,选用适合支架送达狭窄处释放,造影确认若残留狭窄不满意,谨慎选择后扩张,最后撤出保护装置。术后自然中和肝素。③术后处理:术后患者在神经内科监护病房监护24 h,多参数监测生命体征和神经系统的症状和体征,特别是监测心率与血压,血压控制在120~140/70~80 mmHg;术后继续服用阿司匹林+氯吡格雷3~6个月,对有高血压、糖尿病、高脂血症等危险因素的患者继续药物控制(分别服用相应降压、降糖、降血脂药物)。
1.5 随访 患者均进行随访观察,方式包括门诊、电话、短信、家访等。术后2 d、3个月时分别复查经颅多普勒(transcranial Doppler,TCD),1年时行DSA或CTA评估血管情况。①血管检查:介入治疗后评估支架近端和远端血流速度,血管内膜变化,有无新发斑块等;对比介入后支架处血管的直径变化,再狭窄程度等。②记录患者终点事件、死亡以及可能的死因;介入治疗后新发的血管事件包括短暂性脑缺血发作(transient ischemic attacks,TIA)、再发脑梗死、脑出血、蛛网膜下腔出血(subarachnoid hemorrhage,SAH)的时间、次数、责任血管分布情况。③记录mRS、BI、NIHSS评分:了解术后患者生活质量、残障程度变化。④了解患者危险因素控制情况:包括高血压、糖尿病、高脂血症、吸烟,血同型半胱氨酸控制情况,服药依从性情况。
1.6 统计学方法 应用SPSS 12.0统计软件处理数据。计量资料比较分别采用F检验和SNK-q检验;计数资料比较采用χ2检验。P<0.05为差异有统计学意义。
2.1 介入治疗 40例患者经过全脑血管造影,共发现可进行介入的脑血管狭窄42处(其中单侧颈内动脉狭窄28处,双侧颈动脉狭窄各2处,椎动脉狭窄8处,椎动脉合并单侧颈动脉2处),使用支架42枚(其中椎动脉支架10枚,颈动脉支架32枚)。
撤出装置后立即进行造影,评价进行介入治疗的血管及其供血区域,检查结果显示所有支架均定位准确。术前1例颈动脉重度狭窄患者残余狭窄30%,给予球囊扩张后效果满意,余患者狭窄残余均≤20%,血管腔扩张满意,血管远端供血区血流通畅。5例患者检查退出保护伞时可见脂质样物质。共有30例颈动脉支架患者在球囊扩张或支架释放过程即刻出现心率减慢伴血压降低,其中15例患者有显著变化(心率、血压降低>30%或收缩压<90 mmHg、心率<40次/min),均立即静脉注射阿托品、多巴胺或静脉滴注胶体液,所有患者均在48 h内恢复正常。2例患者术后头痛,复查头颅CT无出血,不除外高灌注所致,给予积极控制血压后1周内缓解。
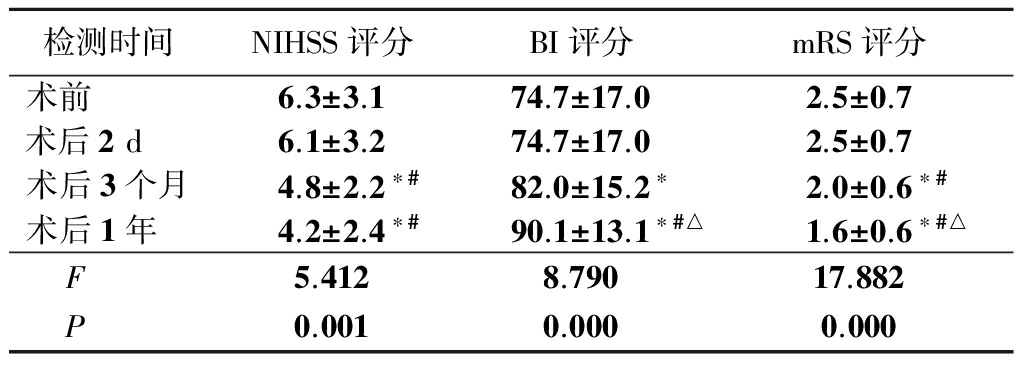
2.2 术后随访 术后2 d复查颈部血管彩色多普勒、TCD检查均血流通畅,狭窄明显改善,重度狭窄病例血流速度较前好转,无急性再狭窄形成;随着术后时间延长,NIHSS评分和mRS评分逐渐降低,BI评分逐渐升高,差异有统计学意义(P<0.05)。见表1。
2.3 不良事件及原因分析 术后3个月、1年复诊时发现介入血管再狭窄2处,介入血管再狭窄率4.8%(2/42),血管检查评估2处再狭窄分别为40%和30%,无相关TIA或梗死,发生再狭窄患者和家属拒绝进一步DSA检查,口服氯吡格雷75 mg每天1次、阿托伐他汀钙40 mg每晚1次,继续随访半年血管狭窄无明显变化。40例患者在1年随访期内死亡1 例,脑出血1例,TIA发作2例(4次),脑梗死2例。其中死亡患者死因为心脏病;脑出血患者为非介入血管供血区的血肿,患者的高血压控制不良,表现为随访时患者依从性较差,未规律监测血压,频繁换用或漏服降压药;脑梗死2例TIA发作患者中,1例后循环TIA为椎动脉支架术后患者,但复查影像学无再狭窄,给予药物治疗。发生脑梗死和TIA的患者均患2型糖尿病,有多重脑血管病危险因素。
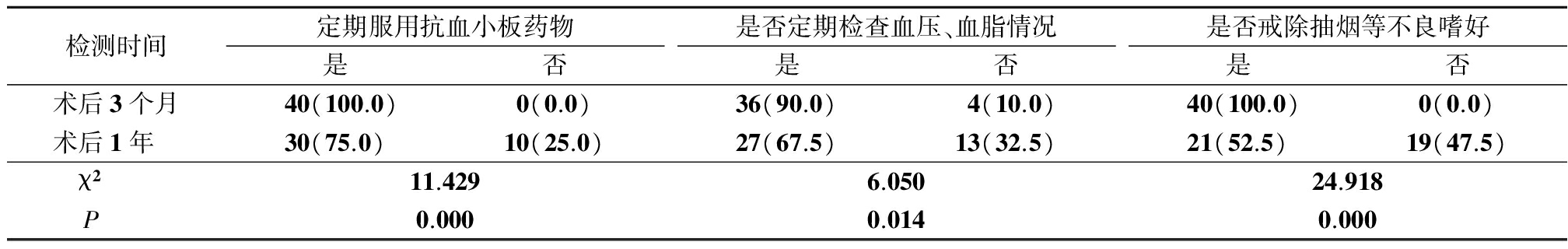
从患者依从性来看,术后3个月随访时患者均能完全按医嘱应用抗血小板聚集药物,4例患者未按医嘱控制危险因素,复诊时加强督导;1年终点时10例患者未按医嘱服药和监测、控制相关危险因素,其中包括5例出现血管事件的患者。见表2。
表1 40例患者介入前后NIHSS评分、BI评分和mRS等评分比较![]() 分)
分)

*P<0.05与术前比较 #P<0.05与术后2 d比较 △P<0.05与术后3个月比较(SNK-q检验)
表2 40例患者依从性情况比较(例数,%)
缺血性脑血管病在全世界范围内是排名第三位的人类健康杀手,而在全国范围内,其排名第一。同时,也是人类致残的重要原因之一[4]。针对颅外大动脉狭窄的治疗,椎动脉狭窄只能使用介入疗法进行重建。而对于颈动脉狭窄,颈动脉内膜剥脱术(carotid endarterectomy,CEA)因其开展时间最长,仍旧是颈动脉狭窄治疗的标准方案。但 CEA的围手术期风险十分严峻。颈动脉支架成形术只需进行局部麻醉,对心肺功能较差的患者耐受性好,恢复迅速,所以患者的接受程度较高,近年来发展非常迅速,得到了广泛的应用。颈动脉的支架植入技术早有报道,当时主要利用已有的胆道支架和外周血管支架来治疗颈动脉狭窄[5]。依据脑血管病变及血管狭窄结构的需要,还分别设计出了开环和闭环支架系统,以适应不同病变的血管。
目前缺血性脑血管病介入治疗开展广泛,动脉硬化斑块的小栓子或附壁血栓脱落是造成的术中梗死常见原因,颈动脉保护伞的应用从无到有,到目前的普遍应用,减少了围手术期缺血性卒中并发症[6],随访中短期的效果理想[7]。本研究显示保护伞内脂质样物5例,证实了其重要的保护作用。在进行球囊扩张颈内动脉起始部时,颈动脉窦压力感受器产生严重反应者可导致患者休克和心跳骤停,本研究30例实施颈动脉狭窄球囊扩张的患者,心电、血压实时监测中均发现心率减慢和血压降低,其中15例下降明显需应用阿托品和升压药物治疗。重度狭窄患者更容易出现严重反应,为减少和减轻这一反应,可依据不同患者特点,选择恰当直径的球囊扩张,并且对于≥90%的狭窄,应避免过度扩张,残留狭窄可放宽10%~20%,或者采取小球囊预扩张的方法,同时这一措施也可能对减少高灌注综合征、术中术后颅内出血有益。本研究术后头痛患者无颅内血肿,故高灌注可能最大,积极控制血压后所有患者均在1周内缓解。总体来说本研究患者介入术中和术后并发症均较轻且可控制,手术效果良好。国外较长时间的回顾性研究和随机研究提示支架介入治疗术后主要的远期并发症是支架内血栓形成及管腔再狭窄[8],对于术后血管再狭窄程度和狭窄者血管事件发生率[9]的研究预期较好;我国一些血管支架治疗脑血管病的研究也讨论了术后狭窄问题,发生率均不高[10]。本研究随访患者40例,介入治疗血管42处,术后2 d复查颈部血管彩色多普勒、TCD检查均血流通畅,狭窄明显改善,重度狭窄病例血流速度较前好转,无急性再狭窄形成;截至1年终点发现介入血管再狭窄2处,再狭窄率4.8%,国内文献综合资料显示的再狭窄率0~32.4%[11-13],波动范围较大,可能与不同的中心、样本规模和患者选择有关。欧洲多中心长达5 年的随访显示再狭窄率6.00%,本研究结果与其近似,但本研究随访时间不长,继续增加病例和延长随访时间可能会得出更准确数据。本研究2处再狭窄均为颈内动脉,再狭窄程度均在中度以下,且无相应的血管事件出现,分析原因:1例患者有高脂血症,未规律监测血压、血糖,多重危险因素的高卒中复发风险可能是患者出现再狭窄的重要原因;另1例患者术后随访中发现其未按医嘱定期检查和规律服药,血糖控制不佳,故患者依从性差,未规律应用抗血小板聚集药物和未积极控制危险因素可能促进了术后再狭窄。
[参考文献]
[1] 周华东.缺血性脑血管病介入治疗进展[J].解放军医药杂志,2014,26(3):35-37.
[2] 中华医学会神经病学分会脑血管病学组缺血性脑血管病血管内介入诊疗指南撰写组.中国缺血性脑血管病血管内介入诊疗指南[J].中华神经科杂志,2011,44(12):863-869.
[3] 宋刚,焦力群,凌锋,等.中国颈动脉支架置入术的文献评价与现状[J].中国脑血管病杂志,2014,11(3):113-117.
[4] 张桂莲,张茹,王虎清,等.缺血性脑血管病颅内外血管狭窄支架成形术的临床研究[J].临床神经病学杂志,2011,24(1):27-29.
[5] 赵美英,王润青,刘威,等.缺血性脑血管病脑血管造影及介入治疗术后并发症的分析与处理[J].中国实用神经疾病杂志,2015,18(5),85-86.
[6] 刘君鹏,汪银洲,程琼,等.颈动脉支架治疗缺血性脑血管病的疗效分析及并发症探讨[J].福建医药杂志,2014,36(2):9-13.
[7] 刘婉婷,许治强,关海涛,等.缺血性脑血管病介入手术治疗的回顾性分析[J].中国现代手术学杂志,2014,18(3):215-217.
[8] 李绍发,梁柯,黄志志.血管内支架成形术治疗症状性椎动脉开口狭窄105例临床观察[J].广西医学,2014,36(4):462-464,467.
[9] 宋洪生,吴芳,孙岩,等.颈动脉支架成形术治疗颈动脉狭窄42例疗效观察[J].海军医学杂志,2014,35(4):277-279.
[10] 钱德才,王乾成,邓磊,等.支架置入术治疗颅外段动脉狭窄16例临床分析[J].中国实用神经疾病杂志,2014,17(14):15-16.
[11] 苏治国,王秀菊,宋迎,等.临床介入治疗缺血性脑血管病的研究进展[J].中国处方药,2016,14(8):14-15.
[12] 李钊,郭德江,李淑梅,等.CT灌注成像在缺血性脑血管病患者脑-硬膜-动脉贴敷手术中的应用[J]河北医科大学学报,2015,36(3):277-279.
[13] 郭明升,李薇.冬季与夏季椎-基底动脉系统短暂性脑缺血发作临床特点比较[J].临床荟萃,2014,29(12):1342-1344.
[收稿日期]2016-11-01;
[修回日期]2017-01-04
[作者简介]刘长江(1974-),男,吉林长春人,吉林大学第四医院副主任医师,医学硕士,从事神经外科疾病诊治研究。
[中图分类号]R743
[文献标志码]B
[文章编号]1007-3205(2017)11-1327-04
(本文编辑:许卓文)