盐酸普拉克索是2007年在我国批准上市的新型抗帕金森病药物,商品名森福罗,目前已经成为抗帕金森治疗的一线药物[1],该药为非麦角类高选择性多巴胺受体激动药,临床上与左旋多巴联合使用可有效改善中晚期帕金森病患者的运动症状,同时可缓解帕金森病患者伴发的抑郁症状,避免因长期使用左旋多巴造成的神经损害[2],延缓治疗时间及降低使用剂量,可大大提高患者的生活质量[3-4]。该药在欧洲药典9.0[5]、美国药典40[6]均被收载,欧洲药典中盐酸普拉克索的含量测定采用电位滴定法,美国药典采用高效液相色谱(high performance liquid chromatography,HPLC)法进行含量测定。国内普遍采用HPLC法测定盐酸普拉克索含量[7-10],鲜见采用电位滴定法进行含量测定的报道。根据国家化学药品原料药质量标准指导原则中的相关规定:“原料药含量测定首选电位滴定法[11-12]”,本研究新建立了一种采用电位滴定法测定盐酸普拉克索含量的方法,同时与HPLC法进行对比研究,归纳总结出仪器法与电位滴定法对于原料药含量测定的优缺点,旨在建立一种更好的盐酸普拉克索含量测定方法,为盐酸普拉克索质量标准提供依据。
1 材 料 与 方 法
1.1仪器 809型自动电位滴定仪(metrohm公司),银电极(metrohm公司),Waters e2695-2489型高效液相色谱仪,色谱柱(资生堂CAPCELL PAK C18 MGII 250 mm×4.6 mm,5 μm),XD105 DU 型十万分之一电子天平(德国Mettler-Toledo公司),Milli-Q超纯水仪(美国Millipore 公司)。
1.2试剂与试药 盐酸普拉克索对照品(USP,批号:G0L469;含量:99.8%);盐酸普拉克索供试品(自制,批号:20161201、 20161202、20161203);硝酸、磷酸二氢钾、磷酸为分析纯;辛烷磺酸钠和乙腈为色谱纯;水为超纯水。
2 方法与结果
2.1电位滴定法
2.1.1试验条件 银电极;参数设置:1个等当点,预馈5.0 mL,总体积10 mL。
2.1.2滴定方法 精密称取盐酸普拉克索0.12 g,加水150 mL使其溶解,同时加入3 mol/L硝酸溶液10 mL,照2015年版药典项下电位滴定法,用0.1 mol/L硝酸银滴定液滴定,并将滴定的结果用空白试验校正。每1 mL硝酸银滴定液(0.1 mol/L)相当于14.213 mg盐酸普拉克索(C10H19Cl2N3S)。
2.1.3空白试验 量取150 mL水,同时加入3 mol/L硝酸溶液10 mL,按“2.1.2”项下方法滴定,结果消耗硝酸银滴定液(0.1 mol/L)0.001 2 mL。
2.1.4溶液稳定性试验 取已知含量的盐酸普拉克索对照品5份,按“2.1.2”项下方法制备样品溶液,分别于0、1、2、3、4 h后测定,结果分别为99.2%、99.3%、99.5%、98.9%、99.5%,相对标准偏差(relative standard deviation,RSD)为0.251%(n=5),可见本品在溶液状态下4 h内稳定性良好。
2.1.5重复性试验 取盐酸普拉克索供试品(批号:20161201)6份,按“2.1.2”项下方法滴定,平行操作6次,结果分别为99.5%、99.5%、99.6%、99.6%、99.7%、99.3%,平均值为99.5%,RSD为0.137% (n=6) ,可见该方法重复性良好。
2.1.6准确度试验 取已知含量的盐酸普拉克索对照品9份,分别称取对照品0.096、0.12、0.144 g各3份,按“2.1.2”项下方法分别配制高、中、低3个浓度的样品溶液进行测定,结果分别为99.1%、99.5%、99.7%、99.2%、99.6%、98.9%、99.3%、99.6%、99.8%,平均值为99.4%,与盐酸普拉克索对照品的实际值99.8%比较,RSD为0.201%(n=9),可见该法准确度符合要求。
2.2HPLC法验证试验
2.2.1色谱条件[13]色谱柱:CAPCELL PAK MGII C18(250 mm×4.6 mm,5 μm);检测波长 264 nm;柱温40 ℃;流速1.5 mL/min;进样量 5 μL;稀释剂:磷酸二氢钾缓冲液-乙腈(80∶20);流动相:以磷酸二氢钾缓冲液(称取9.1 g磷酸二氢钾和5.0 g辛烷磺酸钠,加水1 000 mL,用磷酸调节pH值至3.0)为流动相A,以磷酸二氢钾缓冲液-乙腈(1∶1)为流动相B。
2.2.2溶液的制备 ①对照品溶液:精密称取盐酸普拉克索对照品150 mg,置100 mL量瓶中,加稀释剂溶解并稀释至刻度,摇匀,即得。②试品溶液:精密称取盐酸普拉克索供试品150 mg,置100 mL量瓶中,加稀释剂溶解并稀释至刻度,摇匀,即得。
2.2.3系统适用性试验 精密量取对照品溶液和供试品溶液各5 μL,按 “2.2.1”项下方法测定,记录色谱图。结果:盐酸普拉克索峰的拖尾因子不得超过2.0;理论板数按盐酸普拉克索峰计应不得低于3 000。
2.2.4线性关系考察 精密称取盐酸普拉克索对照品50、75、150、180、200 mg,分别置于100 mL量瓶中,加稀释剂溶解并稀释至刻度,摇匀,制成浓度分别为0.501 1、0.750 2、1.501 5、1.800 6、2.000 1 g/L系列的标准对照品溶液,按“2.2.1”项下方法测定,记录峰面积。以浓度(C,g/L)为横坐标,峰面积(A)为纵坐标进行线性回归,得回归方程为A=691.02C+22.082(r=0.999 5)。结果表明盐酸普拉克索在0.501 1~2.000 1 g/L浓度范围内线性关系良好。
2.2.5检测限考察 取线性关系考察项下对照品溶液(浓度为0.501 1 g/L),逐级稀释,按“2.2.1”项下方法测定,记录色谱图,当信噪比为3∶1时,得检测限为0.25 mg/L。
2.2.6仪器精密度试验 取“2.2.2”项下对照品溶液,按“2.2.1”项下方法测定6次,记录色谱图,计算峰面积。结果:盐酸普拉克索峰面积的RSD值为0.611%(n=6),表明仪器精密度良好。
2.2.7溶液稳定性试验 取20161201批供试品溶液,在室温条件下分别放置0、2、4、8、12、24 h,按“2.2.1”项下方法测定,记录色谱图,计算盐酸普拉克索峰面积的RSD值为0.801%,结果表明供试品溶液在24 h内溶液稳定性良好。
2.2.8重复性试验 精密称取20161201批供试品150 mg,置100 mL量瓶中,加稀释剂溶解后并定容至刻度,摇匀,作为供试品溶液,按“2.2.1”项下方法测定,记录峰面积,并按外标法计算供试品含量。平行操作6次,盐酸普拉克索的平均含量为99.8%,RSD值为1.123%(n=6),结果表明本方法重复性良好。
2.2.9回收率试验 精密称取盐酸普拉克索对照品(批号:G0L469)120、150、180 mg各3份,分别置于100 mL量瓶中,用稀释剂溶解并定容至刻度,按“2.2.1”项下方法测定,记录色谱图,并计算回收率,结果显示该方法准确度良好。
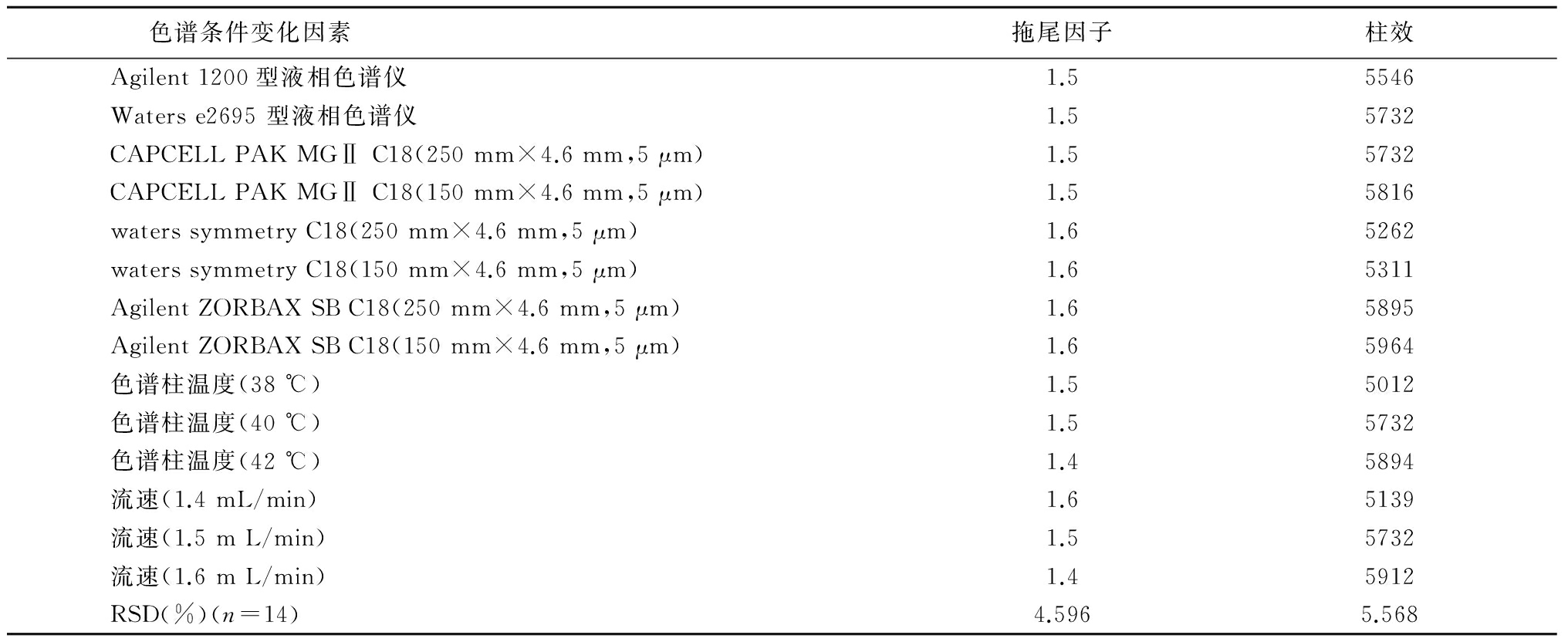
2.2.10耐用性试验[14-15]①以CAPCELL PAK MGⅡ C18(250 mm×4.6 mm,5 μm)为固定相,分别用Agilent 1200和Waters e2695型HPLC仪测定系统适用性溶液,考察不同仪器对检测的影响。②使用Waters e2695型液相色谱仪,分别用CAPCELL PAK MGⅡ C18(250 mm×4.6 mm,5 μm)、CAPCELL PAK MGⅡ C18(150 mm×4.6 mm,5 μm)、waters symmetry C18(250 mm×4.6 mm,5 μm)、waters symmetry C18(150 mm×4.6 mm,5 μm)、Agilent ZORBAX SB C18(250 mm×4.6 mm,5 μm)、Agilent ZORBAX SB C18(150 mm×4.6 mm,5 μm)3个品牌2种规格的6根色谱柱测定系统适用性溶液,考察不同厂家生产的同一类型不同规格色谱柱对测定的影响。③将色谱柱温度分别设置为38 ℃、40 ℃、42 ℃ 3种不同温度,其他条件不变,测定系统适用性溶液,考察不同色谱柱温度对测定结果的影响。④将流速分别设置为1.4、1.5、1.6 mL/min,其他条件不变,测定系统适用性溶液,考察不同流俗对测定结果的影响。耐用性试验结果见表1。
通过对不同仪器、不同品牌色谱柱、不同规格色谱柱、不同色谱柱温度及不同流速的考察结果表明色谱条件发生微小变化不会影响检测结果,不同厂家色谱柱及不同规格的色谱柱对测定均未产生显著差异,可见该方法的耐用性良好。
表1 HPLC法测定盐酸普拉克索含量耐用性试验
Table1Determination of pramipexole hydrochloride content durability tested by HPLC
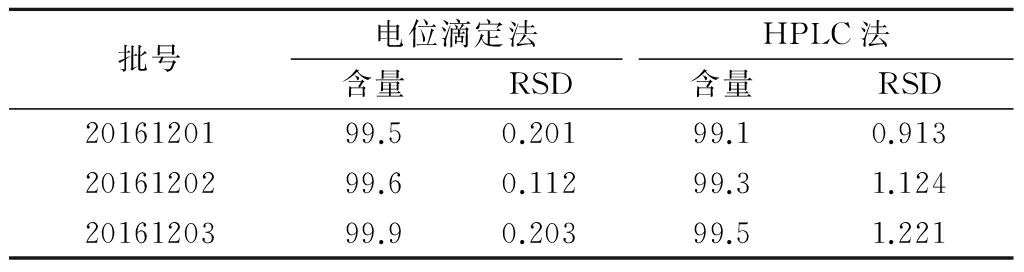
2.3样品含量测定 取盐酸普拉克索供试品3批(批号:20161201、20161202、20161203)适量,分别采用上述2种方法对盐酸普拉克索进行含量测定,结果见表2。
采用2种不同的方法对盐酸普拉克索含量进行测定,结果基本一致,电位滴定法的RSD均小于HPLC法,HPLC法测定误差高于电位滴定法,因为原料药的含量测定范围一般在98.0%~102.0%范围内。
表2 样品含量测定结果
Table2Results of content determination in sample(n=2,%)
3 讨 论
3.1盐酸普拉克索含量测定方法建立的依据 采用HPLC法和电位滴定法测定盐酸普拉克索含量结果基本一致。但由于盐酸普拉克索含量的限度要求为99.0%~101.0%,如果采用色谱法测定含量,仪器误差的允许范围为不得超过2.0%,即为98.0%~102.0%,超出了99.0%~101.0%的范围要求,故在检测过程中很难对结果进行判定。而电位滴定法的误差范围为不得超过1.0%,能满足含量测定的限度要求,可见电位滴定法比色谱法更适合实际生产检测的要求,该方法顺应性更好。因此,通过对比试验研究结果,最终选电位择滴定法作为盐酸普拉克索含量测定的方法。
3.2盐酸普拉克索含量测定目前国外研究现状 目前,美国药典和欧洲药典均对盐酸普拉克索的含量测定进行收载,美国药典采用HPLC法进行测定,欧洲药典则采用电位滴定法进行测定。本研究针对上述2种方法进行对比研究,结果表明上述2种方法测定结果基本一致。根据2种方法检测精密度的要求,美国药典和欧洲药典对含量测定结果的限度要求分别为98.0%~102.0%、99.0%~101.0%(按无水物计算),可见欧洲药典含量测定方法对精密度及准确度要求更为严格。
3.3色谱法与电位滴定法进行含量测定的优缺点 常见的化学原料药含量测定方法分为色谱法和电位滴定法。由于大多数化合物没有典型的官能团与合适的电位滴定液进行反应,且化合物中的相关杂质可能会干扰主成分的测定,很难选择一种合适的电位滴定法进行含量测定,故色谱法的应用越来越广泛。但由于化学原料药的纯度范围要求比较窄,色谱法的重复性较差,不能满足原料药的含量测定要求,故色谱法的应用也有局限性。一般情况下,如果该化合物采用色谱法和电位滴定法均能满足检测时,首选电位滴定法作为化学原料药的含量测定方法。
3.4一般原料药含量测定方法的建立依据 基于电位滴定法和色谱法测定化学药品原料药的优缺点考虑,一般在进行含量测定的检测方法开发时,通常采用2种或2种以上的方法进行比较,以克服检测方法本身的局限性,避免由于方法本身的原因所引起的误差。
3.5硝酸银滴定法的滴定原理 本研究所选用的电位滴定法为经典的氯离子和银离子反应生成硝酸银沉淀的反应,利用盐酸普拉克索中游离的氯离子与硝酸银滴定液中的银离子反应生成硝酸银沉淀,而达到定量的目的。由于硝酸银在碱性条件下不稳定,容易生成络合物而影响方法的准确度,为避免因氯化银沉淀与氯离子形成络合物,故在样品溶液中需加入过量的3 mol/L硝酸溶液。
3.6电位滴定法测定含量的经济效益与社会效益 本研究考虑到美国药典规定的方法(色谱法)检测周期长,检测对仪器和色谱柱均有要求,另外检测过程中使用了辛烷磺酸钠,该试剂不仅价格昂贵,且会对环境造成污染,故在满足测量准确的前提下,最终选择欧洲药典方法(电位滴定法)作为盐酸普拉克索含量测定的方法。
[参考文献]
[1] 毛远湖,汤磊,王建塔.盐酸普拉克索的合成[J].广州化工,2014,42(12):84-85,107.
[2] 曹丽丽,郑忠辉,李进都,等.盐酸普拉克索的合成工艺研究[J].中国药物化学杂志,2014,24(3):201-204.
[3] 刘明周,陈平,汤进华,等.HPLC-/MS/MS法测定健康人血浆中普拉克索浓度[J].中国临床药理学杂志,2013,29(5):378-380.
[4] 李华,陈笑艳,施孝金,等.高灵敏度液相色谱-串联质谱法测定人血浆中普拉克索[J].药物分析杂志,2011,31(2):330-335.
[5] 欧洲药典委员会.欧洲药典[S].8版.斯特拉斯堡:欧洲药品质量管理局,2016:3082-3083.
[6] 美国药典委员会.美国药典[S].40版.华盛顿:美国药典委员会,2016:5795-5798.
[7] 曲丽丽.HPLC测定盐酸普拉克索含量[J].包头医学院学报,2012,28(4):16-17.
[8] 蒲婷婷,陈海硕,汪晴,等.普拉克索贴剂及其有关物质的HPLC法测定[J].中国医药工业杂志,2015,46(9):1017-1020.
[9] 徐晨,张根元,王德才,等.HPLC测定片剂中的盐酸普拉克索[J].华西药学杂志,2014,29(4):428-430.
[10] 郭艳超,李阅东,唐建飞,等.HPLC法检测设备表面盐酸普拉克索残留量[J].首都医药,2014,21(4):56.
[11] 宋倩男,梁敏,杜艳玲,等.电位滴定法测定匹伐他汀钙中的钙含量[J].中国药房,2012,23(45):4301-4302.
[12] 李思源,杨颖.HPLC法与滴定法测定磷酸伯氨喹原料药含量的比较[J].中国药房,2016,27(21):2962-2965.
[13] 李晶,石森林,杨继斌.加校正因子的主成分自身对照法测定盐酸普拉克索的有关物质[J].中国现代应用药学,2015,32(11):1366-1370.
[14] 杨庆云,王志鹏,邓愉凤,等.正相高效液相色谱法拆分普拉克索对映异构体[J].药物分析杂志,2014,34(11):2005-2009.
[15] 朱梅,李善茂.高效液相色谱法测定盐酸普拉克索的手性杂质[J].药物与人,2015,28(1):12.