嗜铬细胞瘤(pheochromocytoma,PC)即主要来源于肾上腺髓质嗜铬组织的可分泌儿茶酚胺(catecholamine,CA)类激素的神经内分泌肿瘤,典型临床症状为高血压、头痛、心悸、大汗。当瘤体释放大量CA入血严重影响血流动力学稳定、并造成器官功能障碍时,即发生嗜铬细胞瘤危象(pheochromocytoma crisis,PCC)。作为威胁全身多脏器系统的内分泌急危重症,PCC一旦发生,如不给予及时处理将严重威胁患者生命[1]。因此,笔者对1例PCC患者的临床救治进行总结,并回顾分析相关文献,旨在为临床医师提供诊疗参考。
1 临床资料
1.1 一般资料 患者,女性,55岁,主因间断头晕、头痛、恶心9 d于2018年1月4日入院。患者自述9 d前受凉后突发头晕、头痛,伴恶心、大汗、咽痛、流涕,自行服用“感冒药”后症状无明显好转,就诊于当地医院诊断为神经性头痛,给予对症治疗(具体不详)后症状稍缓解。2 d前患者头晕、头痛程度加重,伴大汗、恶心、呕吐,为进一步诊治以“头晕待查”收入院。发病以来精神、饮食、睡眠欠佳,体重无明显变化。既往史:既往高血压病史2年余,血压最高达170/100 mmHg,间断口服替米沙坦80 mg,1次/d,未规律监测血压变化;糖尿病病史1年余,间断口服盐酸二甲双胍片0.5 g,3次/d,未规律监测血糖。入院查体:体温35.5 ℃,心率87次/min,呼吸频率21次/min,血压167/111 mmHg,意识清楚,语言流利,查体合作,无颈静脉怒张,双肺呼吸音清,未闻及干湿性啰音,心律齐,各瓣膜听诊区未及杂音,腹部查体无特殊,双下肢无水肿。入院诊断:①头晕原因待查;②上呼吸道感染?③高血压2级高危;④2型糖尿病。
1.2 诊疗经过 给予降压、降糖、调脂、营养神经等综合治疗,拟完善相关检查后制定进一步诊疗方案。患者入院后反复头晕、恶心、呕吐、大汗,程度较院前加重,对症治疗效果欠佳。查体:心率 110次/min,血压87/55 mmHg,意识清楚,皮肤湿冷,心肺腹查体未见异常。考虑患者低血容量休克前期,补液治疗后患者症状稍缓解。急查头颅+胸部+全腹平扫CT显示:头颅未见异常;左肺上叶上舌段及下叶前基底段结节;左肾不规则形等密度为主的等低混杂密度影,右侧肾上腺类圆形等低混杂密度影并多发液液平面。患者于2018年1月5日12:55突发意识丧失,随即意识恢复,心电监护提示室性心动过速,给予胺碘酮150 mg缓慢静脉注射转复为窦性心律。下病危通知、吸氧、综合心电监护,急查心脏超声:心室射血分数59%,左心室舒张功能减低。
为进一步监测生命体征,行锁骨下静脉穿刺置管、有创动脉血压监测。反复测中心静脉压波动于0~3 cmH2O,患者院内血流动力学极不稳定,血压剧烈波动,最高可超过测量上限(>300/140 mmHg),最低降至50/25 mmHg,高血压、低血压状态反复交替,每小时可波动8~10次。患者间断诉头痛、头晕、心悸、恶心、呕吐、大汗,偶有胸闷,无胸痛、视物模糊、视野缺损、一过性意识丧失等不适。患者间断烦躁、精神差,全身多汗、手足厥冷,心肺腹查体未见显著异常。结合患者症状及相关检查,考虑原发病为嗜铬细胞瘤可能性大,患者血压反复波动,治疗上存在矛盾,中心静脉压提示基础血容量不足,给予琥珀酰凝胶注射液、羟乙基淀粉注射液、葡萄糖氯化钠注射液扩容补液,同时加用α受体阻滞剂酚妥拉明以30 mg/h小剂量起始静脉输注,根据患者病情,逐渐增加剂量,调整至60~80 mg/h静脉泵入。
进一步行腹部强化CT显示:左肾中部较大异常密度肿块,恶性病变不除外;右侧肾上腺区肿块伴多发囊变坏死,肾上腺嗜铬细胞瘤不除外(图1)。
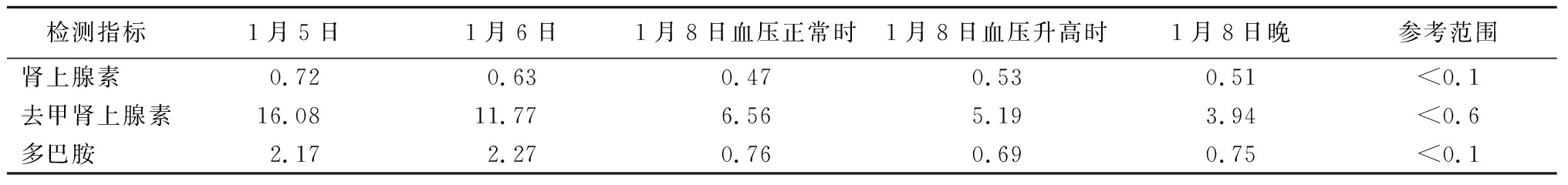
结合患者腹部CT检查结果及相关临床症状、体征,考虑嗜铬细胞瘤可能性大,完善相关实验室检查,测定血尿儿茶酚胺(血压升高时和降至正常时分别留取)、皮质醇(0:00、8:00、16:00血浆皮质醇和24 h尿游离皮质醇),可见患者血尿儿茶酚胺浓度明显升高,见表1~4。
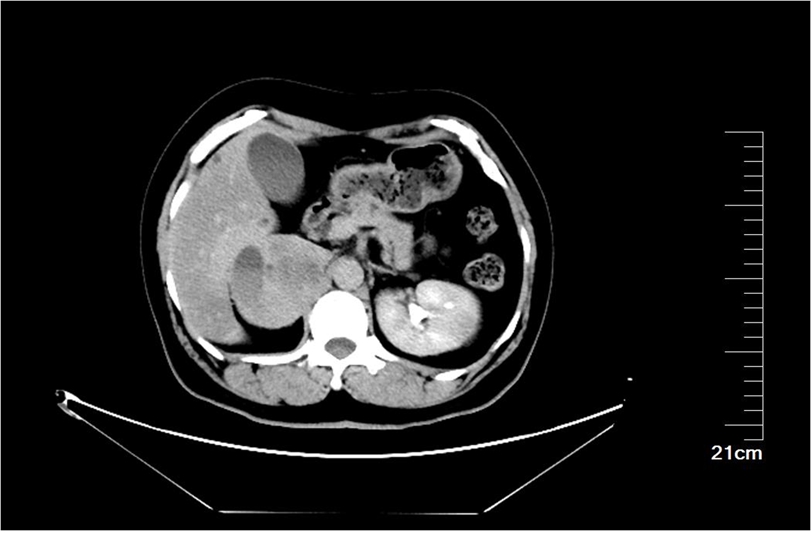
图1 腹部强化CT可见右肾上腺肿物
表1 血浆儿茶酚胺浓度测定 (μg/L)
检测指标1月5日1月6日1月8日血压正常时1月8日血压升高时1月8日晚参考范围肾上腺素 0.720.630.470.530.51<0.1去甲肾上腺素16.0811.776.565.193.94<0.6多巴胺 2.172.270.760.690.75<0.1
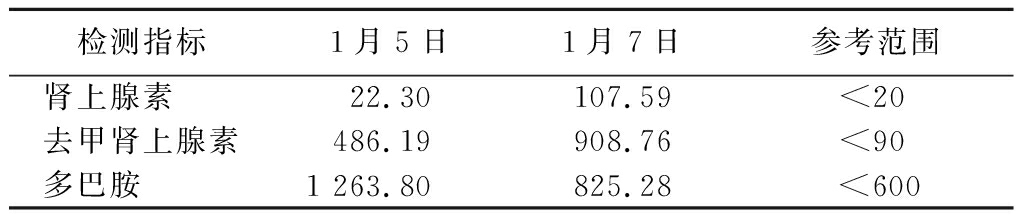
表2 尿儿茶酚胺浓度测定 (μg/24 h)
检测指标1月5日1月7日参考范围肾上腺素 22.30107.59<20去甲肾上腺素486.19908.76<90多巴胺 1 263.80825.28<600
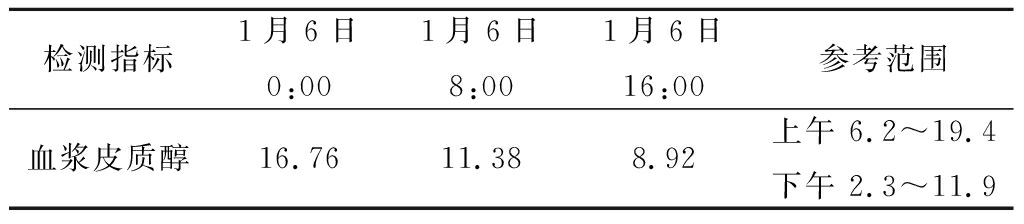
表3 血浆皮质醇浓度测定 (μg/dL)
检测指标1月6日0:001月6日8:001月6日16:00参考范围血浆皮质醇16.7611.388.92上午 6.2~19.4下午 2.3~11.9
表4 尿游离皮质醇浓度测定 (μg/24 h)
检测指标1月7日参考范围24 h尿游离皮质醇112.6136~137
考虑患者病情危重,请内分泌科、泌尿外科、影像科等多学科医师联合会诊制定诊疗方案。结合患者症状、体征及相关辅助检查,考虑患者目前血流动力学不稳定手术风险高,建议待生命体征平稳后充分完善术前准备再行手术治疗。继续维持补液、α受体阻滞剂降压的治疗原则,根据患者病情调整方案。
患者于2018年1月8日12:45有创血压下降并持续波动于50~70/30~40 mmHg,将酚妥拉明剂量逐渐减低并停用,急查心脏超声显示:心室射血分数 63%,肺动脉收缩压 59 mmHg,二、三尖瓣少量反流,肺动脉压增高,左心室舒张功能减低。给予去甲肾上腺素升压治疗,配合多巴胺静脉应用,监测患者血压变化。患者随后出现肺部感染、发热及肺水肿等并发症,其院内病情变化、时间节点及处理策略见表5。
为保证治疗效果,院内治疗期间给予患者镇静、营养支持、降糖、补充白蛋白、纠正电解质紊乱、控制心室率、改善循环等辅助治疗。
表5 患者PCC发作期间患者病情变化

病情(时间)主诉症状及体征辅助检查处理策略室性心动过速2018年1月5日 12:55患者意识丧失心电监护示室性心动过速胺碘酮150 mg缓慢静脉注射,0.5~1 mg/min维持血压波动2018年1月5日14:00患者诉头痛、心悸、恶心、呕吐、大汗血压监测提示血压反复剧烈波动给予扩容、补液,应用酚妥拉明静脉泵入持续性低血压2018年1月8日12:45患者精神差,全身湿冷血压不升,有创血压持续波动于50~70/30~40 mmHg酚妥拉明减量停药,去甲肾上腺素升压肺部感染2018年1月8日14:30患者无不适主诉胸部X线片提示肺部感染给予哌拉西林他唑巴坦纳抗感染治疗发热2018年1月9日10:00患者低热、乏力体温最高达38.2 ℃物理降温,效果不佳时给予激素或非甾体抗炎药降温急性肺水肿2018年1月9日10:00诉气短、胸闷,查体双肺听诊可闻及啰音胸部X线片提示双肺渗出控制液体入量,去乙酰毛花苷、多巴胺强心,无创正压通气,利尿治疗
经治疗患者血压波动逐渐减小,生命体征趋于平稳,症状较前稍改善。为进一步完善术前准备,加用酚苄明片10 mg口服,3次/d。待患者病情及生命体征平稳行CT检查,结果示:右侧肾上腺区高代谢肿块,结合临床考虑嗜铬细胞瘤;左肾中部混杂密度肿块,代谢稍高于本底,考虑恶性病变可能性大,肾癌?左肺下叶前外侧基底段稍高代谢结节,考虑转移瘤。双肾磁共振检查未:左肾占位性病变,考虑肾癌可能性大,右侧肾上腺转移瘤伴出血、囊变可能性大,原发肾上腺肿瘤亦不除外(图2)。
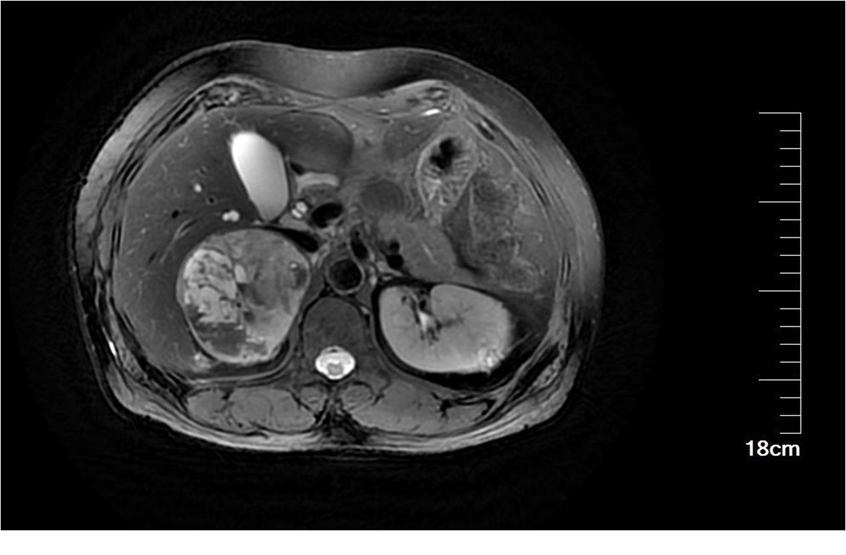
图2 双肾磁共振可见右肾上腺肿瘤
根据以上相关检查明确诊断:①嗜铬细胞瘤危象;②肺部感染;③急性肺水肿;④心律失常室性心动过速;⑤高血压3级很高危;⑥2型糖尿病;⑦左肾占位。
完善相关术前准备后,患者于2018年3月1日在全身麻醉下行择期右侧肾上腺肿瘤切除+左侧肾根治性切除+胆囊切除术。术中暴露右侧肾上腺肿瘤,约8.0 cm×7.0 cm×4.0 cm,与周围组织粘连严重,切面灰红色、质软,内多个囊腔、含血性液体,沿肿瘤表面行钝锐性游离,完整切除肿瘤;探查胆囊有2.0 cm×1.5 cm×1.5 cm实性肿物,游离胆囊后行胆囊切除术;于左肾中部外侧触及一肿物,约5.0 cm×4.0 cm×3.5 cm,切除左侧肾脏。手术过程顺利,术中标本送病理检查:①左肾嫌色性肾细胞癌,伴多灶状钙化,免疫组织化学染色:Vimentin(-),PAX-8(局灶弱+),P53(局灶弱+),Ki-67活跃区阳性率约10%;②右肾上腺嗜铬细胞瘤,瘤细胞明显多形性,局灶弥漫性生长,可见非典型核分裂象,包膜局部脉管腔内见瘤细胞团,提示恶性潜能,周围肾上腺髓质增生,免疫组织化学染色:Syn(+),CgA(+),CD34(血管+),Ki-67阳性率<5%;③胆囊腺肌症,黏膜轻度慢性炎症(图3)。
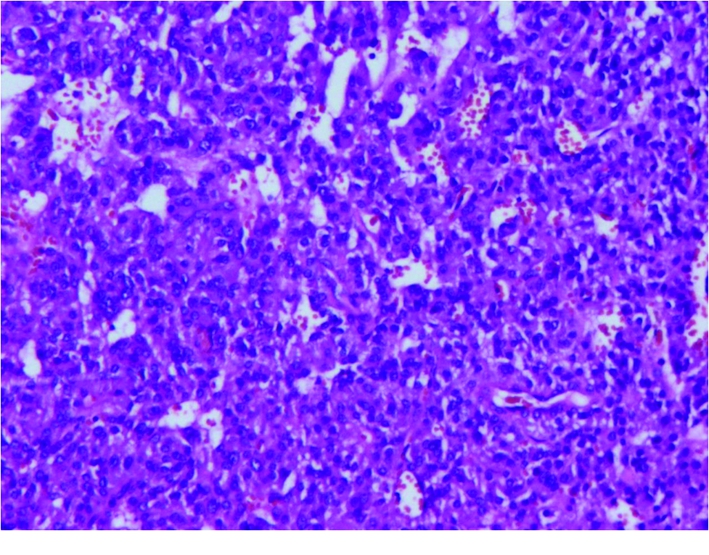
图3 术中切除肾上腺肿瘤细胞病理
术后停用镇静药物后患者意识逐渐转清,拔除经口气管插管后监测患者自主呼吸平稳。术后第1天血压下降至90/60 mmHg,给予适量补液及去甲肾上腺素静脉泵入,维持血压波动在110~120/60~80 mmHg,查体未见明显异常。继续给予抗感染、升压、补液、营养支持、保护胃黏膜等综合治疗。术后密切观察切口引流量及出入量,根据患者血压水平调整去甲肾上腺素用量并逐渐减量停用。患者病情稳定,无不适主诉,于2018年3月16日出院。出院医嘱:注意休息,乌苯美司片10 mg口服,3次/d,定期复查血尿常规、肝肾功能、腹部超声等。
2 讨 论
PC起源于肾上腺髓质嗜铬细胞,其瘤体可合成、分泌CA,如肾上腺素、去甲肾上腺素和多巴胺[2]。PC是引起继发性高血压的常见病因之一,患者临床症状体征多种多样,常引起心、脑、肾等多器官损害,表现为持续性或阵发性高血压、头痛、心悸和大汗等症状[3]。
当CA快速大量释放、机体应激创伤、应用药物(糖皮质激素、麻醉药物、β受体阻滞剂等)、围手术期肿瘤受压等情况发生时,可能诱发PCC,影响机体血流动力学,引起多器官系统功能障碍[4]。PCC是临床较为少见的内分泌急危重症,一旦发生如不及时识别和处理,患者死亡风险极高,严重影响患者治疗效果及预后。查阅相关文献,目前关于PCC的相关临床资料多以个案报告和回顾性分析为主,尚缺乏前瞻性对照研究。Falhammar等[5]对单中心PC患者进行回顾性分析,报道PCC的发生率约为5%。Scholten等[4]对单中心病理数据库统计出PCC的发生率为18.2%。Riester等[6]对德国三家中心内接受手术切除的PC患者进行调查,发现约11.1%患者院内出现PCC。
本例患者院内表现为头痛、大汗、心悸等症状,相关影像学检查提示肾上腺肿物,连续多次测量血浆CA浓度均在正常参考值4倍以上,均有助于PC的诊断。在此基础上,患者院内出现室性心动过速、血压反复剧烈波动、持续性低血压、急性肺水肿等,高度提示患者PCC发作。
PCC最常见的临床表现为高血压危象或儿茶酚胺性心肌病[7]。本例患者高血压与低血压频繁交替,血压波动范围非常大,严重影响血流动力学稳定。查阅既往相关报道,持续性血压波动为PCC较为特异的临床表现之一[8-10]。患者血压升高,考虑与肿瘤细胞反复释放CA、收缩全身血管相关;而全身血管收缩的同时,瘤体细胞血供减少发生缺血坏死,CA进一步释放,血压再次升高形成恶性循环。大量CA持续作用于血管,造成血管内皮细胞缺血缺氧、血管壁通透性增高,血浆大量外渗至组织,减少有效血容量;且患者大汗、呕吐、进食差造成基础血容量不足,从而血压显著下降[11]。当PCC患者血压持续降低时,提示机体血流动力学进一步恶化,病情加重,应紧急处理,停用α受体阻滞剂,应用血管活性药物升压,维持重要脏器灌注。
对于PCC患者,治疗以补液、保护重要脏器、应用a受体阻滞剂为主要原则。PCC早期患者循环血量不足,在其他药物治疗基础上,应积极扩容补液治疗,预防低血压,以保证器官灌注。本例患者在抢救过程中胶体液、晶体液交替静脉输注,通过中心静脉压评估液体出入量。值得重视的是,心脏是PC患者最常受累的重要脏器,除儿茶酚胺性心肌病外,部分患者还表现为急性冠状动脉综合征、心肌炎、心律失常等。其可能的主要机制包括:CA浓度升高诱发冠脉收缩痉挛、血小板聚集,加重冠状动脉缺血;心脏后负荷增加,增加心肌耗氧,进一步诱导心脏结构发生变化;大剂量CA释放能够诱导心肌细胞氧自由基增加、钙超载、线粒体功能异常,加速细胞凋亡等[12-13]。因此,对于存在心功能不全的PCC患者,补液过程中应慎重,监护出入量,定期查心脏超声、脑利钠肽或其氨基末端前体协助判断。
此外,其他重要脏器功能及内环境稳态维持也应给予重视。CA收缩肺动脉使血管通透性增加,严重时导致急性呼吸窘迫综合征和肺水肿。PCC患者一旦出现呼吸系统功能障碍,应尽早行呼吸机辅助通气,必要时行气管插管治疗。PCC造成严重血压反复波动时影响脑循环灌注,且颅内血管收缩、血小板聚集诱导微血栓形成,部分PCC患者可能出现神经系统症状或脑血管意外,应重视患者主诉及查体,必要时联合应用营养神经、改善循环药物。PCC患者需定期监测肝肾功能情况,一旦出现进行性损伤,需早期行替代治疗。CA浓度升高还可诱发高血糖、乳酸酸中毒及酮症等代谢性疾病;PCC患者处于高代谢状态,体内大量炎症因子释放可能使体温升高。患者处于高代谢、高消耗状态,且食欲欠佳、进食困难时应给予肠内外营养支持;治疗过程中如患者出现间断烦躁不安,可适量应用镇静药物,以保证治疗效果。
肿瘤全切手术是症状性PC最有效的治疗策略,已有研究证实腹腔镜下手术与开放手术均能保证肿瘤组织完整、安全地被切除[14]。本例患者在切除嗜铬细胞瘤同时,接受左侧肾根治性切除+胆囊切除术,故选择开放术式。麻醉及术中切除肿瘤可能造成CA大量释放入血,人为诱发类似PCC不良事件发生。因此,术前应用α受体阻滞剂拮抗CA,可避免围手术期相关并发症的发生。α受体阻滞剂不仅适用于PCC合并高血压危象患者的救治,还是保证手术顺利开展的关键环节之一,对于降低PC患者病死率具有重要意义,是PC患者血压管理的首选药物[15-16]。本例患者PCC发作时,选择酚妥拉明小剂量起始静脉应用,根据病情逐渐增加剂量,待高血压危象纠正后,改用酚苄明替代桥接治疗,进一步完善术前准备。
综上所述,PCC是临床中较为少见的内分泌急危重症,其临床症状复杂,主要表现为血压剧烈波动、血流动力学异常、多脏器功能损伤等,严重影响患者预后。PCC一旦发生,应给予足够重视,在完善影像学及实验室检查的同时,对患者临床危象要早期识别、及时救治,待病情控制后行手术切除肿瘤。
[1] 中华医学会内分泌学分会肾上腺学组.嗜铬细胞瘤和副神经节瘤诊断治疗的专家共识[J].中华内分泌代谢杂志,2016,32(3):181-187.
[2] 林果为,王吉耀,葛均波.实用内科学[M].15版.北京:人民卫生出版社,2017:2239-2244.
[3] Lenders JW,Duh QY,Eisenhofer G,et al. Pheochromocytoma and paraganglioma:an endocrine society clinical practice guideline[J]. J Clin Endocrinol Metab,2014,99(6):1915-1942.
[4] Scholten A,Cisco RM,Vriens MR,et al. Pheochromocytoma crisis is not a surgical emergency[J]. J Clin Endocrinol Metab,2013,98(2):581-591.
[5] Falhammar H,Kjellman M,Calissendorff J. Initial clinical presentation and spectrum of pheochromocytoma:a study of 94 cases from a single center[J]. Endocr Connect,2018,7(1):186-192.
[6] Riester A,Weismann D,Quinkler M,et al. Life-threatening events in patients with pheochromocytoma[J]. Eur J Endocrinol,2015,173(6):757-764.
[7] Whitelaw BC,Prague JK,Mustafa OG,et al. Phaeochromocytoma[corrected] crisis[J]. Clin Endocrinol (Oxf),2014,80(1):13-22.
[8] Chatzizisis YS,Ziakas A,Feloukidis C,et al. Pheochromocytoma crisis presenting with cardiogenic shock[J]. Herz,2014,39(1):156-160.
[9] Larouche V,Garfield N,Mitmaker E. Extreme and cyclical blood pressure elevation in a pheochromocytoma hypertensive crisis[J]. Case Rep Endocrinol,2018,2018:4073536.
[10] Sauneuf B,Chudeau N,Champigneulle B,et al. Pheochromocytoma crisis in the ICU:a french multicenter cohort study with emphasis on rescue extracorporeal membrane oxygenation[J]. Crit Care Med,2017,45(7):e657-665.
[11] 姚阳,吴珏莅,周波.嗜铬细胞瘤多系统危象研究进展[J].世界临床医学,2017,11(10):124-125.
[12] Stolk RF,Bakx C,Mulder J,et al. Is the excess cardiovascular morbidity in pheochromocytoma related to blood pressure or to catecholamines[J]. J Clin Endocrinol Metab,2013,98(3):1100-1106.
[13] 宫士坤,刘忠.嗜铬细胞瘤伴心血管损害的临床分析[J].心脑血管病防治,2015,15(1):31-33.
[14] 卢庆,许恩赐,江玮,等.后腹腔镜肾上腺嗜铬细胞瘤切除术38例临床分析[J].河北医科大学学报,2012,33(11):1302-1304.
[15] 王东明,王宏磊,倪少滨.α受体阻滞剂在嗜铬细胞瘤和副神经节瘤围手术期的应用[J].临床与病理杂志,2018,38(2):406-411.
[16] Livingstone M,Duttchen K,Thompson J,et al. Hemodynamic stability during pheochromocytoma resection:lessons learned over the last two decades[J]. Ann Surg Oncol,2015,22(13):4175-4180.