我国2型糖尿病的患病率逐年增加。随着病程的延长,2型糖尿病患者会出现一系列并发症,包括认知功能障碍[1],影响患者治疗效果及生活质量。阿格列汀是一种新型口服高选择性、二肽基肽酶(dipeptidyl peptidase-4,DPP-4)抑制剂,目前临床应用广泛。2017年版中国2型糖尿病防治指南指出[2],2型糖尿病患者如果单用二甲双胍治疗血糖仍不达标,可加用DPP-4抑制剂、α-糖苷酶抑制剂、胰岛素促泌剂等进行二联治疗。2型糖尿病轻度认知功能障碍(mild cognitive impairment,MCI)患者作为2型糖尿病的一类特殊群体,其应用二甲双胍血糖控制欠佳时,加用DPP-4抑制剂、α-糖苷酶抑制剂、胰岛素促泌剂进行二联治疗的有效性及安全性有无区别,目前证据较少。本研究探讨2型糖尿病MCI患者在二甲双胍基础上加用DPP-4抑制剂、α-糖苷酶抑制剂、胰岛素促泌剂的有效性、安全性及其区别,旨在为2型糖尿病MCI患者制定更加合理的临床治疗方案提供理论依据。
1 资料与方法
1.1 一般资料 选取2017年1—11月就诊于河北医科大学第一医院内分泌科的2型糖尿病MCI 患者120例,随机分为阿格列汀组、阿卡波糖组和瑞格列奈组各40例。研究结束时,阿格列汀组因自行停用阿格列汀退出1例,男性23例,女性16例,年龄39~65岁,平均(48.20±8.63)岁;阿卡波糖组因未按时复诊退出1例,男性20例,女性19例,年龄39~64岁,平均(47.60±7.34)岁;瑞格列奈组因未按时复诊退出2例,男性18例,女性20例,年龄40~65岁,平均(49.90±9.41)岁。3组性别、年龄差异均无统计学意义(P>0.05),具有可比性。
本研究经河北医科大第一医院伦理委员会批准;患者或家属均签署知情同意书。
1.2 纳入标准、排除标准和退出标准
1.2.1 纳入标准 均符合1999年世界卫生组织制定的2型糖尿病诊断标准;均符合国际MCI工作组制定的MCI诊断标准:患者本人或知情人主诉记忆力损害;客观检查提示认知功能损害:蒙特利尔认知评估评分<26分;总体认知功能正常,日常生活基本能力保持正常,复杂工具性生活能力轻微损害;不符合痴呆诊断标准;年龄18~65岁;体重指数(body mass index,BMI)为20~45[3];坚持饮食控制、运动,应用二甲双胍(商品名:格华止,美国百时美施贵宝公司,0.5 g,3次/d)单药治疗至少3个月;糖化血红蛋白(hemoglobin A1c,HbA1c)为7%~10%;尿酮体检测阴性。
1.2.2 排除标准 ①1型糖尿病、继发性糖尿病;②近3个月内有糖尿病酮症酸中毒等糖尿病急性并发症,心肌梗死、不稳定型心绞痛、充血性心力衰竭、心功能NYHA分级Ⅲ~Ⅳ级,进行过冠状动脉血管成形术、植入冠状动脉支架、冠状动脉旁路移植术等心脏疾病,肝硬化、慢性活动性肝炎、肝功能异常等肝脏疾病,慢性肠道功能紊乱,肾脏疾病或临床诊断肾功能不全者,原发性高血压筛选时收缩压≥180 mmHg和(或)舒张压≥110 mmHg[3],有血红蛋白异常病史或者诊断为慢性贫血,有活动的或未治疗的恶性肿瘤;④妊娠或哺乳期妇女;⑤已知或可能对阿格列汀、阿卡波糖、瑞格列奈或其辅料过敏。
1.2.3 退出标准 ①不能耐受阿格列汀、阿卡波糖或瑞格列奈不良反应;②研究期间出现糖尿病并发症或心、脑、肝、肾等脏器疾病或肿瘤;③要求退出的患者。
1.3 治疗方法
1.3.1 导入期(第0~2周) 阿格列汀组加用阿格列汀(商品名:尼欣那,日本武田药品工业株式会社,25 mg,1次/d)治疗,阿卡波糖组加用阿卡波糖(商品名:拜唐苹,拜耳医药保健有限公司,50 mg,3次/d)治疗,瑞格列奈组加用瑞格列奈(商品名:诺和龙,诺和诺德公司,1 mg,3次/d)治疗,其间辅以严格控制饮食、餐后活动,心理指导、健康教育等干预措施。应用血糖仪监测三餐前及餐后2 h、睡前(21:00)血糖,必要时加测0:00及3:00血糖,以FPG 4.4~7.0 mmol/L,2 hPBG≤10.0 mmol/L为目标进行治疗[4]。每3天根据患者血糖调整瑞格列奈剂量(最大剂量不超过12 mg/d)、阿卡波糖剂量(最大剂量不超过300 mg/d),阿格列汀组无需调整剂量,直至血糖达标或导入期结束。
1.3.2 维持期(第3~24周) 各组继续接受导入期药物治疗,每周复诊,测定FPG和2 hPBG,根据血糖监测结果调整药物剂量,记录治疗过程中所有不良事件,出现低血糖时检测当时血糖。
1.4 观察指标 本研究为24周随机、平行、对照临床研究,各组在治疗前、治疗12周、治疗24周检测HbA1c、空腹血糖(fasting plasma glucose,FPG)、餐后2 h血糖(2 h postprandial blood glucose,2 hPBG)、三酰甘油(triglycerides,TG)、总胆固醇(total cholesterol,TC),测量收缩压(systolic blood pressure,SBP)、舒张压(diastolic blood pressure,DBP)、身高、体重,计算BMI。HbA1c≤7%为血糖控制达标[4]。
1.5 安全性指标 治疗期间记录所有低血糖事件。低血糖事件定义为:血糖≤3.9 mmol/L,无论有无症状均视为低血糖[4]。严重低血糖定义为:任何需要他人救助的低血糖发作。用药期间观察患者是否出现胃肠道反应(恶心、呕吐、腹泻)及皮疹、皮肤红痒等不良反应,在第0,12,24周分别检测肝功能、肾功能等。
1.6 统计学方法 应用SPSS 21.0统计软件分析数据。计量资料比较采用重复测量的方差分析;计数资料比较采用χ2检验。P<0.05为差异有统计学意义。
2 结 果
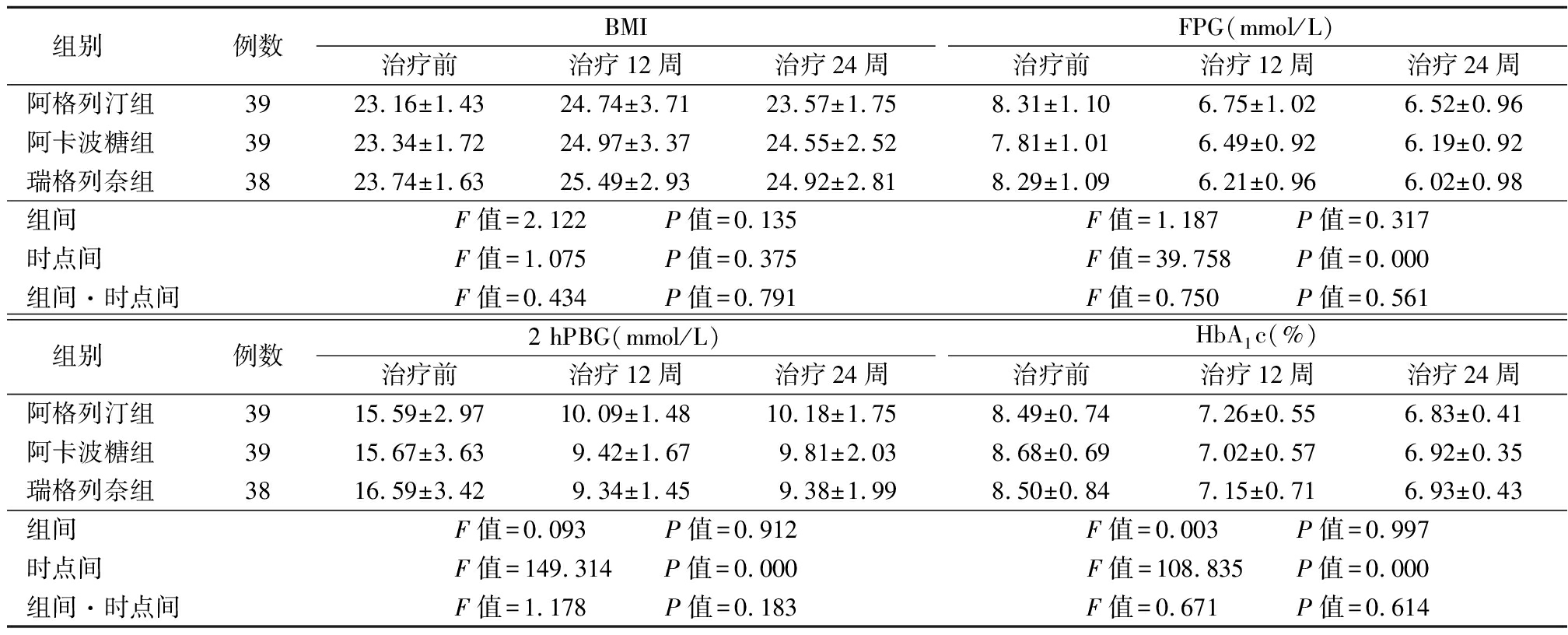
2.1 3组不同时点BMI、FPG、2 hPBG和HbA1c比较 3组FPG、2 hPBG和HbA1c均呈逐渐下降趋势,但3组间FPG、2 hPBG和HbA1c只在不同时点间差异有统计学意义(P<0.01),组间和组间·时点间交互作用差异均无统计学意义(P>0.05);3组BMI变化不大,在组间、不同时点间及组间·时点间交互作用差异均无统计学意义(P>0.05)。见表1。
表1 3组BMI、FPG、2hPBG和HbA1c比较
Table 1 Comparison of BMI、FPG、2hPBG and HbA1c among the three groups ![]()
组别 例数BMI治疗前治疗12周治疗24周FPG(mmol/L)治疗前治疗12周治疗24周阿格列汀组 3923.16±1.4324.74±3.7123.57±1.758.31±1.106.75±1.026.52±0.96阿卡波糖组 3923.34±1.7224.97±3.3724.55±2.527.81±1.016.49±0.926.19±0.92瑞格列奈组 3823.74±1.6325.49±2.9324.92±2.818.29±1.096.21±0.966.02±0.98组间 F值=2.122 P值=0.135F值=1.187 P值=0.317时点间 F值=1.075 P值=0.375F值=39.758 P值=0.000组间·时点间F值=0.434 P值=0.791F值=0.750 P值=0.561组别 例数2 hPBG(mmol/L)治疗前治疗12周治疗24周HbA1c(%)治疗前治疗12周治疗24周阿格列汀组 3915.59±2.9710.09±1.4810.18±1.758.49±0.747.26±0.556.83±0.41阿卡波糖组 3915.67±3.639.42±1.679.81±2.038.68±0.697.02±0.576.92±0.35瑞格列奈组 3816.59±3.429.34±1.459.38±1.998.50±0.847.15±0.716.93±0.43组间 F值=0.093 P值=0.912F值=0.003 P值=0.997时点间 F值=149.314 P值=0.000F值=108.835 P值=0.000组间·时点间F值=1.178 P值=0.183F值=0.671 P值=0.614
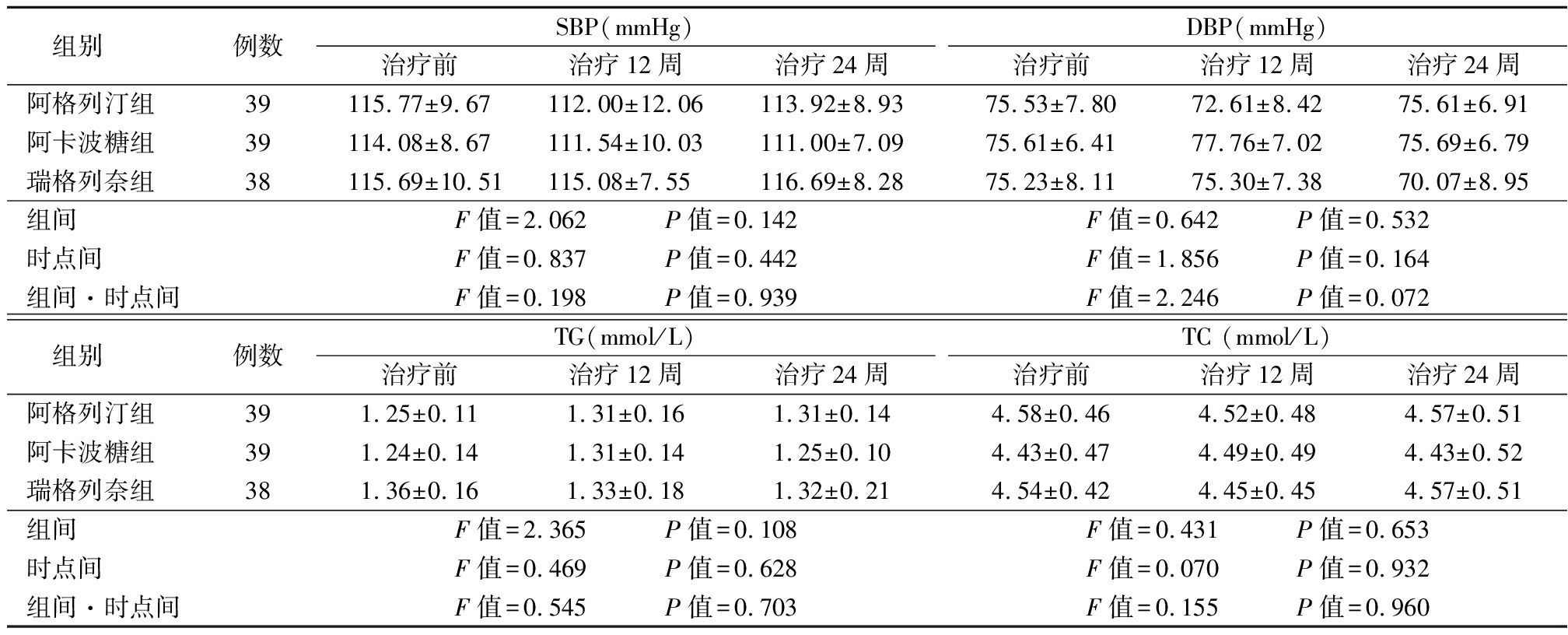
2.2 3组不同时点SBP、DBP、TG和TC比较 3组SBP、DBP、TG和TC变化不大,在组间、不同时点间及组间·时点间交互作用差异均无统计学意义(P>0.05),见表2。
表2 3组不同时点SBP、DBP、TG和TC比较
Table 2 Comparison of SBP、DBP、TG and TC at different time point in three groups ![]()
组别 例数SBP(mmHg)治疗前治疗12周治疗24周DBP(mmHg)治疗前治疗12周治疗24周阿格列汀组 39115.77±9.67112.00±12.06113.92±8.9375.53±7.8072.61±8.4275.61±6.91阿卡波糖组 39114.08±8.67111.54±10.03111.00±7.0975.61±6.4177.76±7.0275.69±6.79瑞格列奈组 38115.69±10.51115.08±7.55116.69±8.2875.23±8.1175.30±7.3870.07±8.95组间 F值=2.062 P值=0.142F值=0.642 P值=0.532时点间 F值=0.837 P值=0.442F值=1.856 P值=0.164组间·时点间F值=0.198 P值=0.939F值=2.246 P值=0.072组别 例数TG(mmol/L)治疗前治疗12周治疗24周TC (mmol/L)治疗前治疗12周治疗24周阿格列汀组 391.25±0.111.31±0.161.31±0.144.58±0.464.52±0.484.57±0.51阿卡波糖组 391.24±0.141.31±0.141.25±0.104.43±0.474.49±0.494.43±0.52瑞格列奈组 381.36±0.161.33±0.181.32±0.214.54±0.424.45±0.454.57±0.51组间 F值=2.365 P值=0.108F值=0.431 P值=0.653时点间 F值=0.469 P值=0.628F值=0.070 P值=0.932组间·时点间F值=0.545 P值=0.703F值=0.155 P值=0.960
2.3 血糖达标情况比较 治疗结束时,阿格列汀组血糖达标率最高为74.36%(29/39),阿卡波糖组血糖达标率最低为46.15%(18/39),瑞格列奈组血糖达标率居中为57.89%(22/38),阿格列汀组血糖达标率高于阿卡波糖组(χ2=6.496,P<0.01)。
2.4 安全性比较 ①3组均无因不能耐受其不良反应退出者。②治疗过程中各组肝功能以及肾功能均未见明显异常。③治疗过程中阿格列汀组无胃肠道反应发生;阿卡波糖组56.41%(22/39)出现腹胀、恶心,持续2周后可自行缓解;瑞格列奈组15.79%(6/38)出现腹胀、恶心。阿卡波糖组胃肠道反应发生率最高,瑞格列奈组胃肠道反应发生率次之,阿格列汀组胃肠道反应发生率最低(χ2=37.853,P<0.01)。④治疗过程中3组患均无皮疹、皮肤红痒等不良反应发生。⑤治疗结束时,阿格列汀组低血糖发生率为2.56%(1/39),阿卡波低血糖发生率为28.20%(11/39),瑞格列奈组低血糖发生率为42.10%(16/38);阿格列汀组组低血糖发生率最低,阿卡波糖组低血糖发生率居中,瑞格列奈组低血糖发生率最高(χ2=16.955,P<0.01)。阿格列汀组未发生严重低血糖,阿卡波糖组严重低血糖发生率为7.69%(3/39),瑞格列奈组严重低血糖发生率为18.42%(7/38);瑞格列奈组严重低血糖发生率显著高于阿卡波糖组(χ2=8.318,P<0.05)。
3 讨 论
2013年调查研究显示我国成人2型糖尿病患病率为10.4% 。但HbA1c不达标率却高达80%,54.7%~63.8%的患者至少伴有一种并发症。2型糖尿病可引起认知功能障碍[5],早期可表现为MCI,以学习记忆力、注意力、语言理解力、思维判断力、执行力等认知功能下降或功能障碍为主[6]。Zheng等[7]研究发现,我国老年2型糖尿病患者DPP-4高活性可显著升高MCI风险。
阿格列汀属于口服DPP-4抑制剂,目前广泛应用于临床。其可通过抑制DPP-4活性,减少体内胰高血糖素样肽1(glucagon-like peptide 1,GLP-1)灭活,升高内源性GLP-1水平。后者以葡萄糖浓度依赖的方式促进胰岛素分泌,抑制胰高糖素分泌,二者共同作用可有效降低HbA1c、FPG、2 hPBG水平以及血糖波动[8-11]。此外,DPP-4抑制剂还可增加胰岛β细胞数量、减少β细胞凋亡[12]。
潘长玉等[3]研究显示,与安慰剂相比,中国2型糖尿病患者应用阿格列汀单药或联用二甲双胍可显著降低HbA1c和FPG,提高HbA1c达标率,且不增加低血糖发生率,总体安全性类似。与阿卡波糖相比,未经药物治疗的中国2型糖尿病患者应用DPP-4抑制剂治疗有效率与其相似,且耐受性较好,不引起体重增加,胃肠道不良事件更少。与胰岛素促泌剂相比,DPP-4抑制剂与其降糖效果相当。应用二甲双胍血糖控制欠佳的糖尿病患者,应用西格列汀降糖效果与格列吡嗪相似,并能改善胰岛β细胞功能,耐受性更好,低血糖和体重减轻风险更低。2型糖尿病患者单用二甲双胍血糖控制欠佳时,分别联合DPP-4抑制剂与格列齐特治疗52周,二者疗效相似,耐受性均很好,但应用DPP-4抑制剂治疗的患者低血糖事件发生率无显著增加。与格列美脲相比,DPP-4抑制剂降糖效果无显著差异,但DPP-4抑制剂组体重无增加,低血糖事件显着减少。王丽芳等[13]关于老年糖尿病患者应用阿格列汀的研究显示,与年轻患者相比,老年人使用阿格列汀有效,耐受性好,低血糖、体重增加的风险亦无显著增加。
本研究结果显示,2型糖尿病MCI患者应用阿格列汀的降糖效果不劣于阿卡波糖和瑞格列奈,三者均可有效控制HbA1c、FPG、2 hPBG。本研究进一步发现,2型糖尿病MCI患者应用阿格列汀的低血糖发生率、胃肠道反应发生率均低于阿卡波糖和瑞格列奈,糖化血红蛋白达标率显著高于阿卡波糖和瑞格列奈。提示与阿卡波糖和瑞格列奈相比,2型糖尿病MCI患者应用阿格列汀血糖控制更理想,低血糖和胃肠道反应发生率更低。
综上所述,临床工作中,2型糖尿病MCI患者应用二甲双胍单药治疗HbA1c不达标时,推荐联合DPP-4抑制剂[14]。阿格列汀每天1次,口服简便,具有良好疗效及安全性。此外,在二甲双胍基础上联合应用 DPP-4抑制剂更具有成本效果[15]。但本研究样本量相对较少,有待日后扩大样本量进一步验证,以便为2型糖尿病MCI患者制定更加合理的临床治疗方案提供理论依据。
[1] Kuo SC,Lai SW,Hung HC,et al. Association between comorbidities and dementia in diabetes mellitus patients:population-based retrospective cohort study[J]. J Diabetes Complications,2015,29(8):1071-1076.
[2] 中华医学会糖尿病学分会.中国2型糖尿病防治指南(2017年版)[J].中华糖尿病杂志,2018,10(1):4-67.
[3] 潘长玉,李文慧,曾姣娥,等.阿格列汀治疗2型糖尿病的有效性与安全性中国大陆多中心、随机、双盲、安慰剂对照Ⅲ期临床研究[J].中华内科杂志,2015,54(11):949-953.
[4] 中华医学会糖尿病学分会.中国2型糖尿病防治指南(2013年版)[J].中华糖尿病杂志,2014,6(7):447-498.
[5] Tong J,Geng H,Zhang Z,et al. Brain metabolite alterations demonstrated by proton magnetic resonance spectroscopy in diabetic patients with retinopathy[J]. Magn Reson Imaging,2014,32(8):1037-1042.
[6] 李梅,马兰,范鹰,等.2型糖尿病患者轻度认知功能改变特点及其相关因素的研究[J].中华老年多器官疾病杂志,2016,15(1):6-10.
[7] Zheng T,Qin L,Chen B,et al. Association of plasma DPP4 activity with mild cognitive impairment in elderly patients with type 2 diabetes:Results from the GDMD study in China[J]. Diabetes Care,2016,39(9):1594-1601.
[8] 中华医学会糖尿病学分会.基于胰高血糖素样肽1降糖药物的临床应用共识[J].中华糖尿病杂志,2014,6(1):14-20.
[9] Kaneto H,Matsuoka TA. Role of pancreatic transcription factors in maintenance of mature B-cell function[J]. Int J Mol Sci,2015,16(3):6281-6297.
[10] 黄汉伟,黎健南,蔡雪,等.DPP-4抑制剂对胰岛素治疗2型糖尿病患者血糖波动的影响[J].重庆医学,2017,46(17):2365-2368.
[11] Xiao C,Dash S,Morgantini C,et al. Sitagliptin,a DPP-4 inhibitor,acutely inhibits intestinal lipoprotein particle se-cretion in healthy humans[J]. Diabetes,2014,63(7):2394-2401.
[12] 郑坤杰,武革,耿建林,等.不同降糖药物对2型糖尿病大鼠胰岛β细胞凋亡及再生作用的影响[J].河北医科大学学报,2017,38(11):1260-1264.
[13] 王丽芳,谢宁生,何勇,等.阿格列汀联合甘精胰岛素对初诊老年2型糖尿病患者的临床疗效观察[J].现代诊断与治疗,2016,27(21):4039-4040.
[14] 母义明,翟所迪.基于肠促胰素治疗药物临床应用的快速建议指南[J].中华内分泌代谢杂志,2016,32(6):448-454.
[15] Geng J,Yu H,Mao Y,et al. Cost effectiveness of dipeptidyl peptidase-4 inhibitors for type 2 diabetes[J]. Pharmacoeconomics,2015,33(6):581-597.