静脉血栓栓塞症(venous thromboembolism,VTE)是肺血栓栓塞症(pulmonary thromboembolism,PTE)和深静脉血栓(deep venous thrombosis,DVT)的合称。PTE系因来自静脉系统或右心的血栓阻塞肺动脉或其分支所致的一种最常见的急性肺栓塞类型;DVT多发于下肢或骨盆深静脉,是引起PTE的主要血栓来源。以华法林为代表的维生素K拮抗剂(vitamin K antagonist,VKA)自上世纪50年代起即开始用于治疗VTE,起着基石的作用。VKA价格便宜,但只有狭窄的治疗窗,需要在频繁的监测下用药且存在很多食物-药物交互作用,导致患者依从性差。非维生素K拮抗剂新型口服抗凝药(non-vitamin K antagonist oral anticoagulants,NOACs)相比华法林等VKA花费昂贵,但无需实验室监测,且少有食物-药物交互作用。近年来,有关NOACs的临床研究成果与日俱增,NOACs在临床上的应用也越来越广泛,其疗效和安全性也受到越来越多的临床医师关注。本研究就NOACs对比VKA治疗VTE的有效性和安全性进行荟萃分析,以期为临床用药决策提供循证医学依据。
1 资料与方法
1.1 纳入与排除标准 ①纳入公开发表的NOACs治疗VTE的随机对照试验(randomized controlled trials,RCTs)和多中心对照研究,无论其是否采用盲法,限制语种为英文;②NOACs对比VKA治疗急性VTE的Ⅲ期临床试验;③受试者被客观诊断为DVT或PTE,或诊断为同时患有DVT和PTE;④受试者遵循随机分配原则;⑤国籍、种族不限。排除标准:①因有潜在肝毒性而停止使用的希美加群[1]的相关研究; ②NOACs应用于短期抗凝的研究; ③不能获得摘要、全文的研究;④重复发表的研究;⑤综述、个案报道、社评、会议记录、观察性研究等。
1.2 干预措施 试验组:NOACs抗凝治疗,药物主要有阿哌沙班(apixaban)、利伐沙班(rivaroxaban)、依度沙班(edoxaban)和达比加群(dabigatran),无论是否桥接于肠道外抗凝剂之后应用。对照组:VKA抗凝治疗,不限于华法林,无论是否桥接于肠道外抗凝剂之后应用,无论桥接于何种肠道外抗凝剂之后应用。
1.3 结局指标 本研究以复发性VTE和VTE相关的死亡为疗效指标,以全因死亡率、出血事件为安全性指标。
1.4 检索策略及数据提取 以“venous thromboembolism、anticoagulants、randomized”为关键词检索PubMed、Cochrane Library、EMbase数据库,结合主题词、自由词检索,检索日期自建库起截至2017年6月,同时手工检索已纳入文献相关的参考文献,必要时联系原文作者以获取个别未提及信息。数据提取时按上述纳入、排除标准由2名研究者独立提取所需资料并交叉核对,如有争议则共同探讨或寻求第三方意见。提取资料包括研究名称、年份、病例数、随机方法、盲法、干预措施、疗程、结局指标等。
1.5 质量评价 采用Cochrane 手册5.2所推荐的质量评价标准(包含6个方面,7个条目):①随机序列产生(选择偏倚);②是否实施分配隐藏(选择偏倚);③是否对研究者和受试者施盲(实施偏倚)、是否有研究结局的盲法评价(测量偏倚);④结局数据是否存在缺失(随访偏倚);⑤是否存在选择性报告研究(报告偏倚);⑥是否存在其他来源的偏倚(其他偏倚)。根据偏倚风险评估对各条目判定为“低偏倚风险”、“不清楚”或“高偏倚风险”,分别标为“+”“?”“-”,记录在偏倚风险总结图中。
1.6 统计学方法 本研究遵循系统综述和Meta分析优先报告条目规范,使用RevMan5.3软件进行Meta分析,根据Q统计量检验和I2检验对纳入研究进行同质性分析,借助P值与I2判断各研究间是否有统计学异质性,对无异质性(P>0.1,I2<50%)的研究使用固定效应模型进行合并分析;存在异质性(P<0.1,I2>50%)则使用随机效应模型。本研究中的结局指标均为计数资料,以比值比(odds ratio,OR)、95%可信区间(95% confidence interval,95%CI)表示效应量。P<0.05为差异有统计学意义。
2 结 果
2.1 纳入研究概况 检索出相关文献共计2 685篇,通过阅读文献题目、摘要或全文,最终纳入7篇文献[2-8],均为多中心RCTs,共计29 879例患者,其基本特征见表1。
表1 纳入研究基本特征
Table 1 Characteristics of studies included
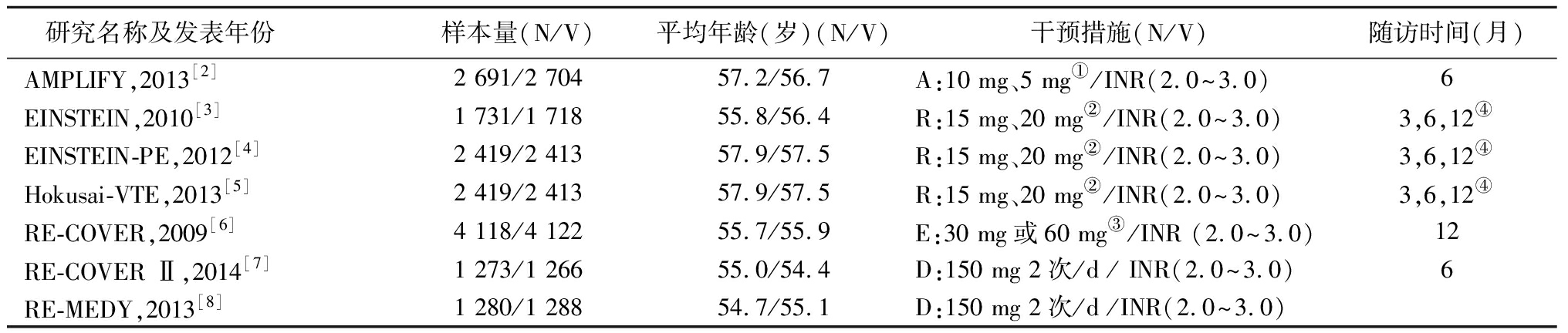
研究名称及发表年份样本量(N/V)平均年龄(岁)(N/V)干预措施(N/V)随访时间(月)AMPLIFY,2013[2]2 691/2 70457.2/56.7A:10 mg、5 mg①/INR(2.0~3.0)6EINSTEIN,2010[3]1 731/1 71855.8/56.4R:15 mg、20 mg② /INR(2.0~3.0)3,6,12④EINSTEIN-PE,2012[4]2 419/2 41357.9/57.5R:15 mg、20 mg②/INR(2.0~3.0)3,6,12④Hokusai-VTE,2013[5]2 419/2 41357.9/57.5R:15 mg、20 mg②/INR(2.0~3.0)3,6,12④RE-COVER,2009[6]4 118/4 12255.7/55.9E:30 mg或60 mg③/INR (2.0~3.0)12RE-COVER Ⅱ,2014[7]1 273/1 26655.0/54.4D:150 mg 2次/d / INR(2.0~3.0)6RE-MEDY,2013[8]1 280/1 28854.7/55.1D:150 mg 2次/d /INR(2.0~3.0)
注:N:新型口服抗凝药组; V:维生素K拮抗剂组; INR (2.0~3.0):调整国际标准化比值在2.0~3.0之间;A:阿哌沙班;R:利伐沙班;E:依度沙班;D:达比加群;①2次/d,每次口服10 mg,7 d后改为2次/d,每次口服5 mg;②2次/d,每次口服15 mg,3周后改为1次/d,每次口服20 mg;③如果受试者肌酐清除率在30~50 mL/min时或体重≤60 kg时或同时在应用P-糖蛋白抑制剂(如维拉帕米)时则1次/d,每次口服30 mg,推荐剂量为1次/d,每次口服60 mg;④意向治疗时间为3,6或12个月,由研究者事先确定并随机分组
2.2 质量评价 除EINSTEIN和EINSTEIN-PE 2项研究的实施偏倚被评估为“高偏倚风险”外,其余研究的所有条目和这2项研究的其他条目均被评估为“低偏倚风险”(图1)。因纳入文献<10篇,故无法用漏斗图评估发表偏倚。
2.3 Meta分析结果
2.3.1 以复发性VTE/VTE相关死亡为疗效指标分析 7 篇文献中,EINSTEIN和EINSTEIN-PE 2项研究虽仅报道了复发性VTE ,但结果中包含了致死性PE等信息,其余5项研究均报道了复发性VTE或VTE相关的死亡,故将7项研究结果予以合并,研究之间无异质性(P=0.43,I2=0%),使用固定效应模型分析,结果显示NOACs组和VKA组治疗VTE出现复发性VTE或VTE相关的死亡的概率差异无统计学意义(OR=0.94,95%CI=0.81~1.08,P=0.38)(图2)。表明NOACs与VKA相比,在降低出现复发性VTE或VTE相关死亡的风险方面作用相仿。
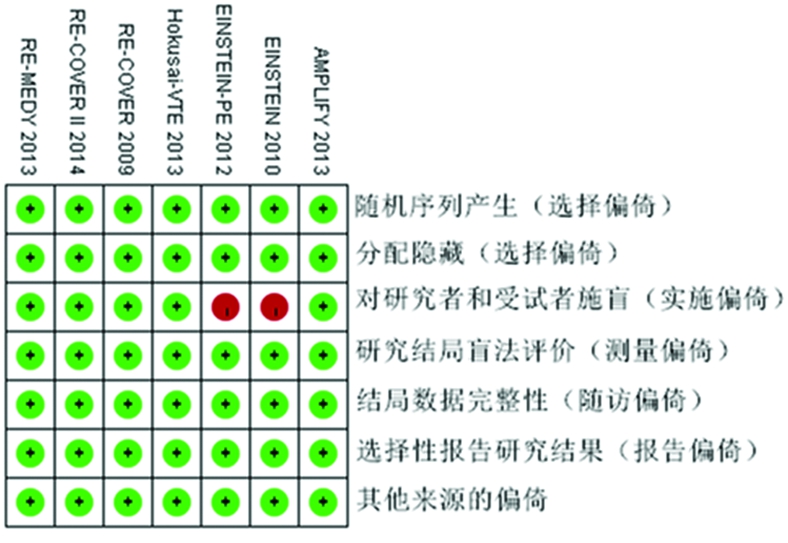
图1 纳入文献的质量评价(偏倚风险总结图)
Figure 1 Bias assessment for the studies included
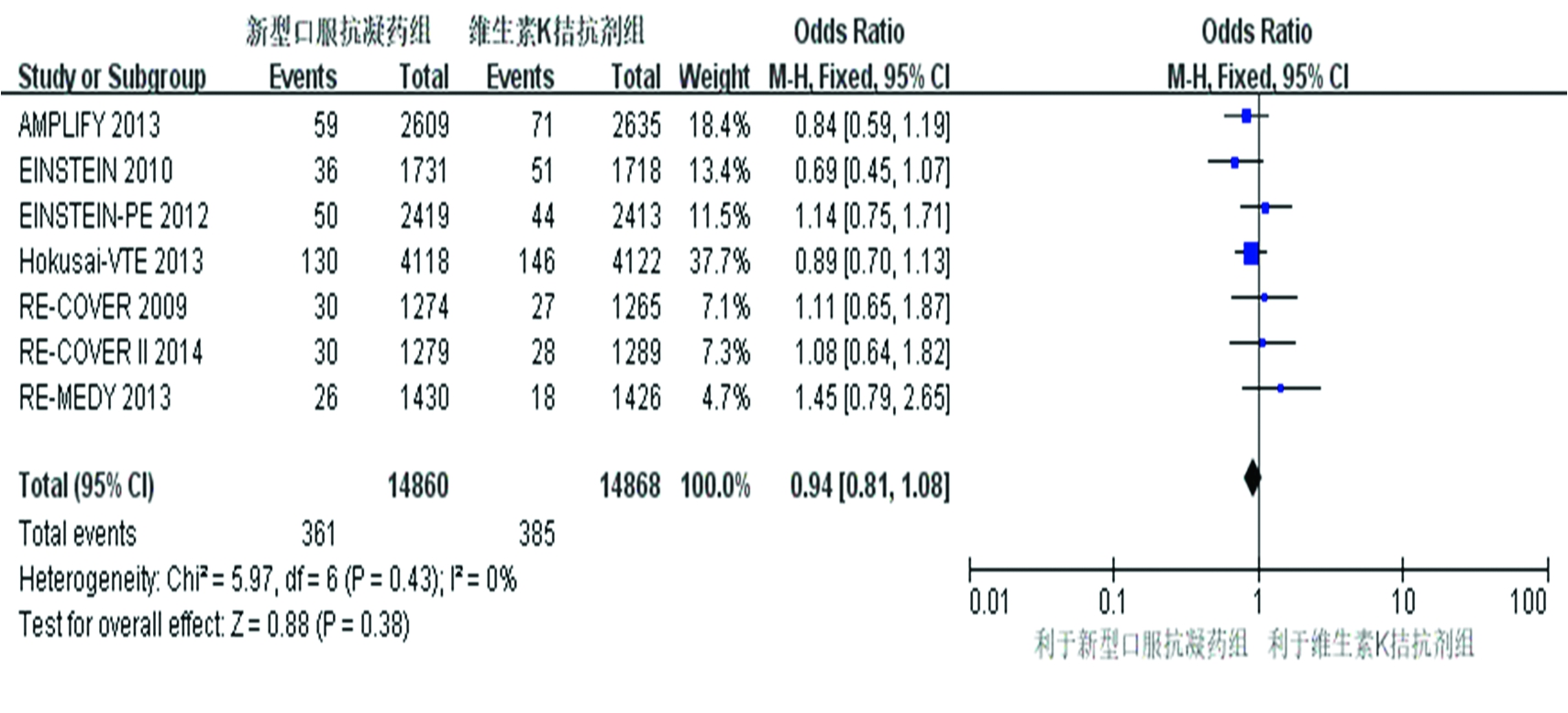
图2 复发性VTE/VTE相关死亡的森林图
Figure 2 Forest plot for the risk of recurrent venous thromboembolism(VTE)or VTE-related death
2.3.2 以全因死亡率为安全性指标之一分析 7 篇文献均报道了全因死亡人数,研究之间无异质性(P=0.75,I2=0%),使用固定效应模型分析,结果显示NOACs组和VKA组治疗VTE的全因死亡率差异无统计学意义(OR=0.97,95%CI=0.83~1.13,P=0.70)(图3)。表明NOACs与VKA相比,并不能降低死亡风险。
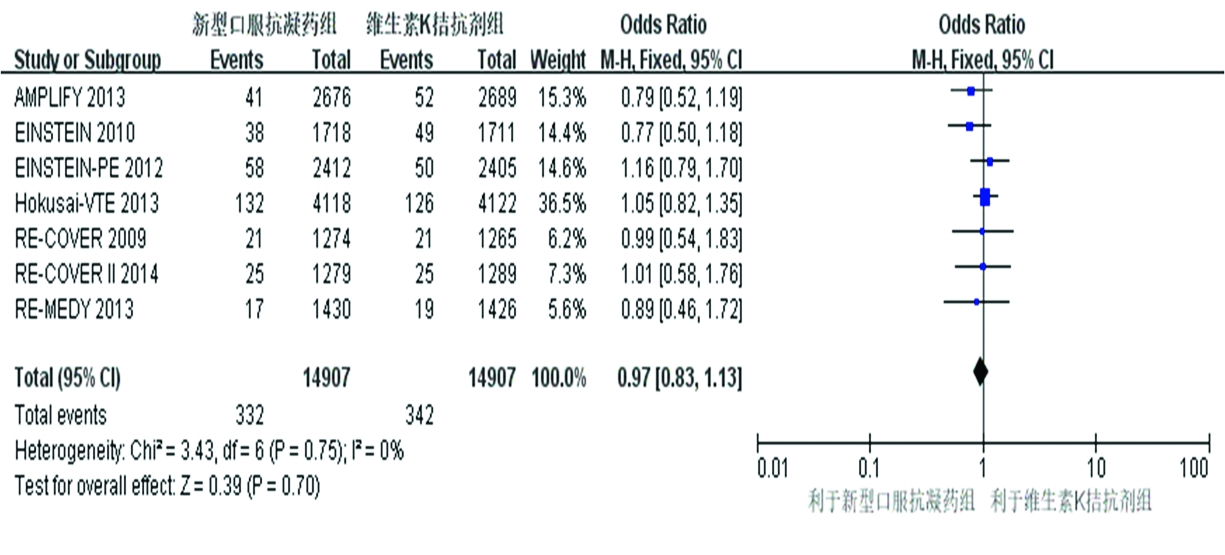
图3 全因死亡率的森林图
Figure 3 Forest plot for the risk of all-cause mortality
2.3.3 以大出血事件为安全性指标之一分析 7 篇文献均报道了出现大出血事件的病例数,研究之间有轻度异质性(P=0.09,I2=45%),根据Cochrane 手册当I2=45%时,该异质性可以接受,使用固定效应模型分析,结果显示NOACs组和VKA组治疗VTE出现大出血的概率差异有统计学意义(OR=0.61,95%CI=0.50~0.75,P<0.01)(图4)。表明NOACs较VKA相比可明显降低大出血事件发生的风险。
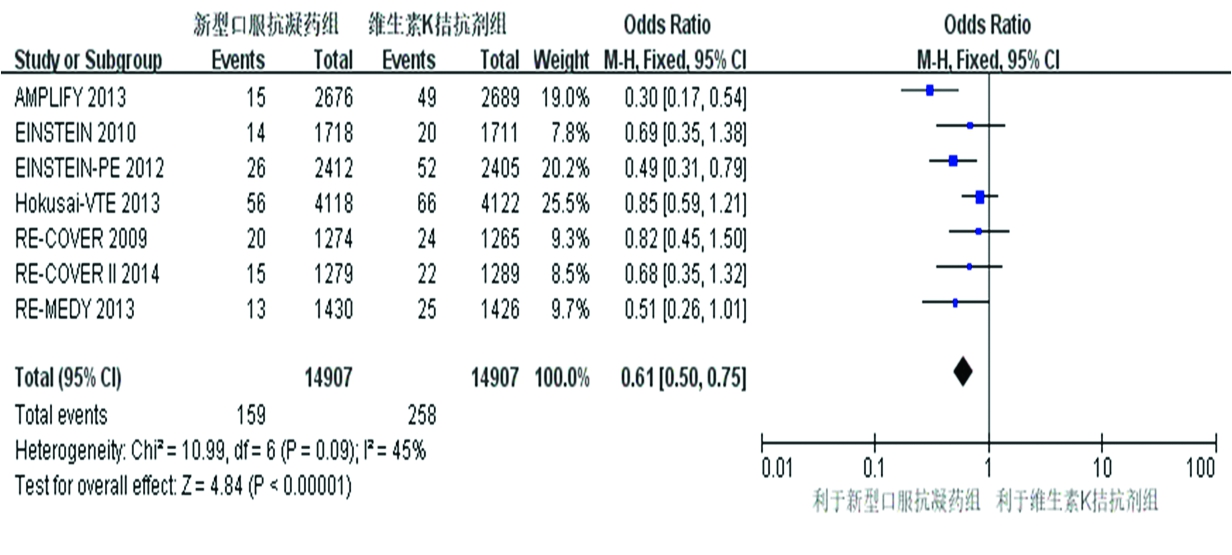
图4 大出血事件的森林图
Figure 4 Forest plot for the risk of major bleeding
2.3.4 以致命性出血事件为安全性指标之一分析 7 篇文献均报道了出现致命性出血事件的病例数,研究之间有无异质性(P=0.59,I2=0%),使用固定效应模型分析,结果显示NOACs组和VKA组治疗VTE出现致命性出血事件的概率差异有统计学意义(OR=0.37,95%CI=0.17~0.81,P=0.01)(图5)。表明NOACs较VKA相比可明显降低致命性出血事件发生的风险。
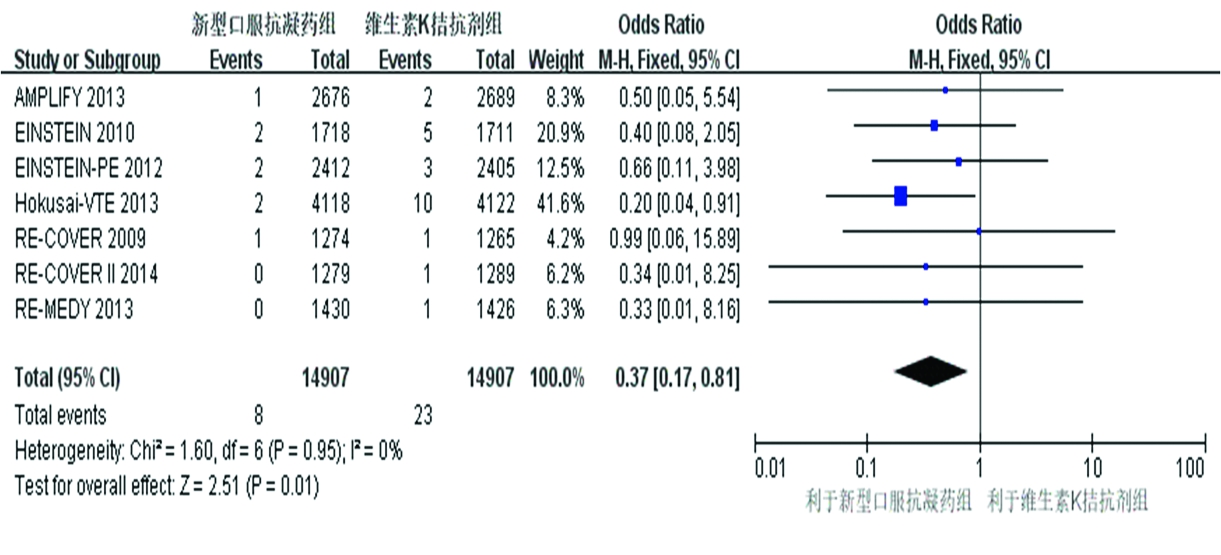
图5 致命性出血事件的森林图
Figure 5 Forest plot for the risk of fatal bleeding
2.3.5 以不良反应发生率为安全性指标之一分析 7篇文献均报道了出现不良事件的病例数,不良反应主要有颅内出血、消化道出血等,但各研究的评价指标存在极大差异,报道的不良反应条目无法统一,故不予以合并分析。其中AMPLIFY研究中阿哌沙班出现不良反应的概率为67.08%,VKA为71.51%;EINSTEIN研究中利伐沙班出现不良反应的概率为62.75%,VKA为63.12%;EINSTEIN-PE研究中利伐沙班出现不良反应的概率为80.47%,VKA为79.13%;Hokusai-VTE研究中依度沙班出现不良反应的概率为68.50%,VKA为71.03%;RE-COVER研究中达比加群出现不良反应的概率为66.30%,VKA为67.61%;RE-COVER Ⅱ研究中达比加群出现不良反应的概率为66.61%,VKA为71.06%;RE-MEDY研究中达比加群出现不良反应的概率为71.96%,VKA为70.82%。
3 讨 论
VTE是一类常见的血管疾病,其发病率高,极易漏诊、误诊,一旦发生,将带给患者沉重的经济负担和严重的死亡威胁[9]。目前临床上治疗VTE主要依靠抗凝、溶栓、手术取栓、安置静脉滤器等手段。近年来,越来越多新型抗凝药物被开发并投入临床应用,使临床工作者和患者拥有更多选择。VKA通过抑制维生素K环氧还原酶,阻止凝血因子Ⅱ、Ⅶ、Ⅸ、Ⅹ的生成从而发挥抗凝作用,但VKA对已经产生的凝血因子无灭活效应,故需桥接于肝素类药物后应用。NOACs中达比加群属于凝血因子Ⅱa抑制剂,阿哌沙班、依度沙班、利伐沙班均为凝血因子Ⅹa抑制剂,可见NOACs的共同特点是仅抑制一个关键的凝血因子,这是其起效迅速的药理学基础。同时,NOACs与其他药物发生相互作用的位点仅有P-gp和CYP3A4,相比VKA(如华法林)NOACs的可控性强,且也不像VKA那样易受绿茶、菠菜等食物的影响而降低疗效[10-11]。本研究纳入的7个RCTs质量高,研究过程遵循Cochrane系统评价原则,对VTE的复发率和相关死亡、出血事件、全因死亡率情况进行了Meta分析。本研究表明NOACs在保证疗效的前提下,在降低出血事件方面具有独特的优势(尤其能降低颅内出血的风险[2,4-8]),提示临床上有高出血风险的患者可以优先考虑选择NOACs用于抗凝治疗,特别对于有出血致死高风险的患者,NOACs是更佳选择。
就单个药物而言,在降低复发性VTE或VTE相关的死亡发生率方面,AMPLIFY和Hokusai-VTE 2项研究分别提示阿哌沙班、依度沙班较VKA相比为更优选择,而RE-COVER、RE-COVER Ⅱ、RE-MEDY 3项研究提示VKA较达比加群疗效更佳。在降低全因死亡率方面,AMPLIFY研究提示阿哌沙班较VKA效果更佳,Hokusai-VTE研究提示VKA较依度沙班相比,全因死亡率更低。在降低总不良反应事件方面,AMPLIFY研究中的阿哌沙班和Hokusai-VTE研究中的依度沙班出现不良反应的概率明显低于对应的VKA组;而利伐沙班的EINSTEIN和EINSTEIN-PE 2个研究结果相反,利伐沙班体现出的优势并不明显,但总体来看利伐沙班组出现不良反应的概率为70.10%,对应的VKA组出现不良反应的概率为72.47%,提示利伐沙班安全性较高。RE-COVER、RE-COVER Ⅱ 2项研究中达比加群出现不良反应的概率均低于对应的VKA组,虽RE-MEDY研究中达比加群出现不良反应的概率大于对应的VKA组,但总体来看,达比加群组出现不良反应的概率为68.43%,对应的VKA组出现不良反应的概率为69.88%,提示达比加群发生不良反应的总体概率小于对应的VKA组[2-8]。
在实际临床工作中,除了对新型药物的疗效和安全性的担忧外,经济效益也是影响临床决策的重要因素。研究表明,NOACs用于心房颤动的患者时,其总体费用明显高于使用华法林[12]。有关VTE患者使用NOACs的成本分析仍有赖于更多大样本数据,可以预见NOACs的使用成本一定会大大增加这类患者的经济负担。更重要的是目前仅有达比加群的特异拮抗剂Idarucizumab被美国食品药品监督管理局批准用于临床[13],其余少数NOACs拮抗剂(如andexanetalfa、aripazine)仍处于研究阶段[14-16]。此外已有研究证实,若患者合并肝、肾功能不全,应慎用甚至禁用NOACs[10,17]。因此,对于NOACs的研发,仍需加大力度、加快进度。
本研究存在一定局限:①纳入研究的数量较少,可能存在发表偏倚;②纳入研究占比不均衡,达比加群相关研究独占三席,而阿哌沙班、依度沙班分别仅有一项研究,不足以进行亚组分析,这也可能导致结果的真实性受到影响,随着相关研究成果的不断发表,未来可以通过进行亚组分析获取单个NOACs的疗效和安全性;③未纳入中文文献和除英文以外的其他外文文献,可能增大了分析偏差及选择偏倚;④纳入研究所报道的不良反应结果各异,无法合并分析,故NOACs的安全性优势有待进一步评估。
综上所述,NOACs治疗VTE的效果不亚于传统VKA,且在降低出血风险方面前者更具优势。但由于纳入研究所报道的不良反应结果无法合并,其总体安全性优势还需更多结局指标报道详实的、高质量、大样本RCTs深入论证。
[1] Fiessinger JN,Huisman MV,Davidson BL,et al. Ximelagatran vs lowmolecular-weight heparin and warfarin for the treatment of deep vein thrombosis:a randomized trial[J]. JAMA,2005,293(6):681-689.
[2] Agnelli G,Buller HR,Cohen A,et al. Oral apixaban for the treatment of acute venous thromboembolism[J]. N Engl J Med,2013,369(9):799-808.
[3] Bauersachs R,Berkowitz SD,Brenner B,et al. Oral rivaroxaban for symptomatic venous thromboembolism[J]. N Engl J Med,2010,363(26):2499-2510.
[4] Büller HR,Prins MH,Lensin AW,et al. Oral rivaroxaban for the treatment of symptomatic pulmonary embolism[J]. N Engl J Med,2012,366(14):1287-1297.
[5] Büller HR,Décousus H,Grosso MA,et al. Edoxaban versus warfarin for the treatment of symptomatic venous thromboembolism[J]. N Engl J Med,2013,369(15):1406-1415.
[6] Schulman S,Kearon C,Kakkar AK,et al. Dabigatran versus warfarin in the treatment of acute venous thromboembolism[J]. N Engl J Med,2009,361(24):2342-2352.
[7] Schulman S,Kakkar AK,Goldhaber SZ,et al. Treatment of acute venous thromboembolism with dabigatran or warfarin and pooled analysis[J]. Circulation,2014,129(7):764-772.
[8] Schulman S,Kearon C,Kakkar AK,et al. Extended use of dabigatran,warfarin,or placebo in venous thromboembolism[J]. N Engl J Med,2013,368(8):709-718.
[9] Elisha S,Heiner J,Nagelhout J,et al. Venous Thromboembolism:new concepts in perioperative management[J]. AANA J,2015,83(3):211-221.
[10] Schulman S. Advantages and limitations of the new anticoagulants[J]. J Intern Med,2014,275(1):1-11.
[11] Ahrens I,Lip GY,Peter K. New oral anticoagulant drugs in cardiovascular disease[J]. Thromb Haemost,2010,104(1):49-60.
[12] Janzic A,Kos M. Cost effectiveness of novel oral anticoagulants for stroke prevention in atrial fibrillation depending on the quality of warfarin anticoagulation control[J]. Pharmacoeconomics,2015,33(4):395-408.
[13] Pollack CV Jr,Reilly PA,Eikelboom J,et al. Idarucizumab for dabigatran reversal[J]. N Engl J Med,2015,373(6):511-520.
[14] Fu W,Guo H,Guo J,et al. Relative efficacy and safety of direct oral anticoagulants in patients with atrial fibrillation by network meta-analysis[J]. J Cardiovasc Med(Hagerstown),2014,15(12):873-879.
[15] Lu G,DeGuzman FR,Hollenbach SJ,et al. A specific antidote for reversal of anticoagulation by direct and indirect inhibitors of coagulation factor Ⅹa[J]. Nat Med,2013,19(4):446-451.
[16] Ansell JE,Bakhru SH,Lanlicht BE,et al. Use of PER977 to reverse the anticoagulant effect of edoxaban[J]. N Engl J Med,2014,371(22):2141-2142.
[17] Tripodi A. Laboratory tests and the new oral anticoagulants[J]. Thromb Res,2012,130(Suppl 1):S95-97.