带状疱疹后神经痛(post herpetic neuralgia,PHN)指带状疱疹的皮损消退后(通常4周后)神经痛持续存在[1]。其主要特征为持续性抽搐样疼痛、灼痛或间歇性闪电样疼痛、刀割样疼痛、深在性跳痛、痛觉超敏及感觉异常[2]。由于其疼痛程度严重,持续时间长,干扰患者睡眠,易导致患者出现焦虑、抑郁情绪,严重者甚至出现自杀倾向[3-4]。三环类抗抑郁药物阿米替林治疗PHN有一定效果,但药物不良反应限制了其在临床上的应用。2010年普瑞巴林在我国被批准用于PHN的治疗,本研究应用普瑞巴林治疗PHN患者30例,取得良好效果,现报告如下。
1 资料与方法
1.1 一般资料 选择2017年1—12月海南省皮肤病医院门诊及住院部收治的PHN患者60例。按照随机数字表分为:普瑞巴林治疗组(A组)30例,男性20例,女性10例,年龄42~78岁,平均(63.3±9.4)岁,病程1~24 个月,平均(6.5±3.2)个月,疼痛视觉模拟评分法(Visual Analogue Scale,VAS)评分4~9分,平均(6.6±1.5)分,受累部位为肋间神经12例、腰骶神经6例、股神经5例、三叉神经5例、臂丛神经2例;阿米替林对照组(B组)30例,男性19例,女性11例,年龄42~78岁,平均(62.6±9.7)岁,病程1~22个月,平均(6.3±4.1)个月,VAS评分4~9分,平均(6.0±1.5)分,受累部位为肋间神经13例、腰骶神经7例、股神经4例、三叉神经3例、臂丛神经3例。2组性别、年龄、病程、VAS评分、受累部位差异均无统计学意义(P>0.05),具有可比性。
本研究经医院伦理委员会批准;患者均签署知情同意书。
1.2 入选标准和排除标准 入选标准:确诊的PHN患者,年龄≥18岁,同意接受药物治疗,治疗前VAS评分≥4分。排除标准:对上述2种药物过敏者,妊娠或哺乳期者,合并严重心、肝、肾功能不全者,患有神经、精神疾病者,有严重免疫功能低下者,长期使用糖皮质激素及免疫抑制剂者。剔除标准:①治疗期间自行要求退出研究; ②因不良反应无法耐受; ③未按照本研究要求完成治疗方案及随访者;④理解能力有限,无法完成VAS评分、每日睡眠干扰评分法(Daily Sleep Interference Scale,DSIS)、焦虑自评量表(Self-Rating Anxiety Scale,SAS)评分。
1.3 治疗方法 A组第1周口服普瑞巴林胶囊(商品名:莱瑞克,重庆赛维药业有限公司)75 mg,2次/d,至第1周末增加剂量至150 mg,2次/d。B组口服盐酸阿米替林片(湖南洞庭药业股份有限公司)25 mg,2次/d,若至第1周末疼痛控制不理想,可加量至25 mg,3次/d。疗程均为8周。
1.4 评价指标
1.4.1 疼痛指标 采用VAS评价疼痛,0分为完全无疼痛,10分为不能忍受的剧烈疼痛。
1.4.2 睡眠干扰指标 采用DSIS评价对PHN患者睡眠的影响,评分等级为0~10分,0分为疼痛对睡眠完全无影响,10分为疼痛完全影响睡眠。
VAS及DSIS评分均由患者在纳入研究后每日晨起对过去1 d的疼痛及睡眠状态进行自我评定,并进行记录。分别于治疗后第1,2,4,6,8周各时点对过去1周的日评分表汇总,取其平均值作为上述各评定时点的评分。治疗前评分取入组当天的两评分值。
1.5 焦虑测试 采用SAS评价患者焦虑状态。于治疗前以及治疗后第1,2,4,6,8周门诊随访时在医生指导下完成。
1.6 不良反应 记录患者服药期间的不良反应,如头晕、嗜睡、外周水肿、视物模糊、共济失调等。若出现严重不良反应,立即停药,并给予相应处理。于治疗前及治疗后8周进行血常规、肝肾功能检查。
1.7 统计学方法 应用SPSS 20.0统计软件分析数据。计数资料比较采用χ2检验;计量资料比较分别采用t检验和重复测量的方差分析。P<0.05为差异有统计学意义。
2 结 果
A组入组30例,完成30例。B组入组30例,完成29例,1例因无法耐受头晕,于入组后第6天退出。
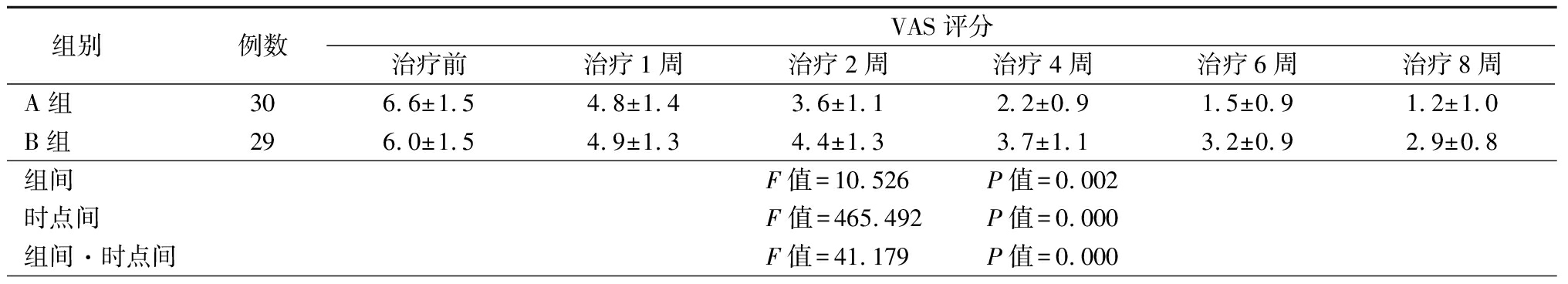
2.1 2组治疗前后VAS评分、DSIS评分和SAS评分比较 2组治疗后VAS评分、DSIS评分和SAS评分均呈逐渐降低趋势,但A组降低更多, 2组VAS评分、DSIS评分和SAS评分在组间、不同时点以及组间与不同时点交互作用差异均有统计学意义(P<0.05),见表1。
表1 2组治疗前后VAS评分、DSIS评分和SAS评分比较
Table 1 Comparison of VAS scores,DSIS scores,SAS scores before and after treatment between two groups ![]() 分)
分)
组别 例数VAS评分治疗前治疗1周治疗2周治疗4周治疗6周治疗8周A组306.6±1.54.8±1.43.6±1.12.2±0.91.5±0.91.2±1.0B组296.0±1.54.9±1.34.4±1.33.7±1.13.2±0.92.9±0.8组间F值=10.526 P值=0.002时点间F值=465.492 P值=0.000组间·时点间F值=41.179 P值=0.000
表1 (续)
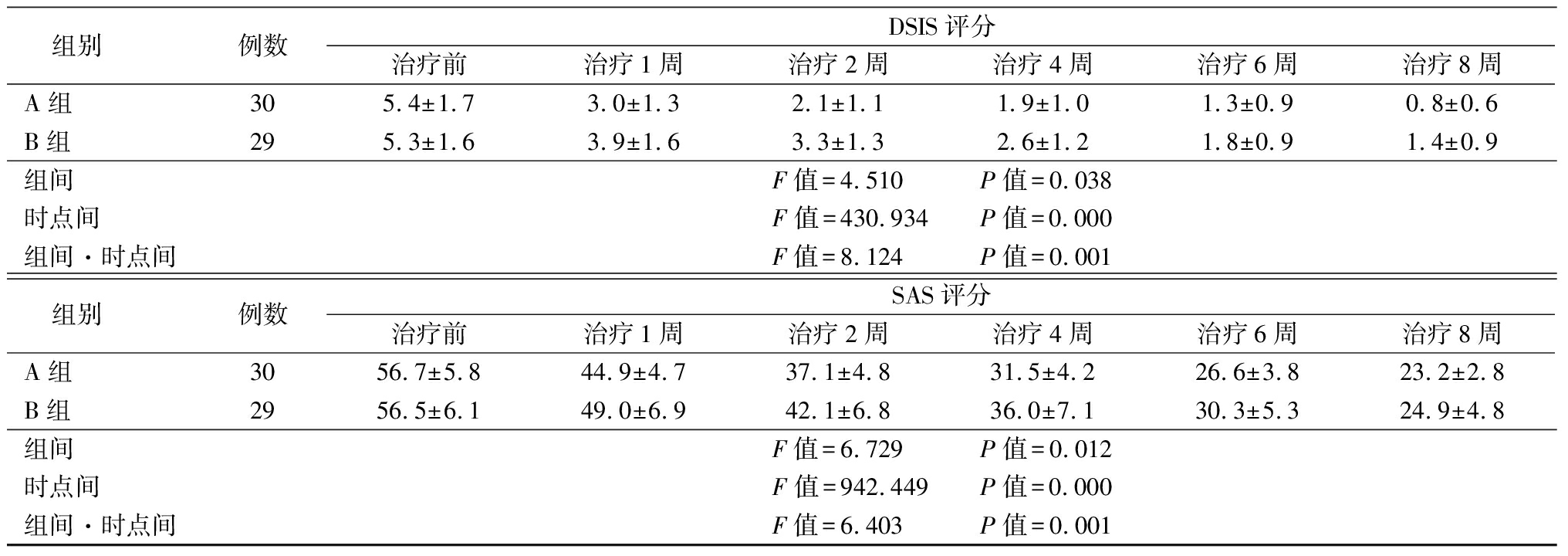
组别 例数DSIS评分治疗前治疗1周治疗2周治疗4周治疗6周治疗8周A组305.4±1.73.0±1.32.1±1.11.9±1.01.3±0.90.8±0.6B组295.3±1.63.9±1.63.3±1.32.6±1.21.8±0.91.4±0.9组间F值=4.510 P值=0.038时点间F值=430.934 P值=0.000组间·时点间F值=8.124 P值=0.001组别 例数SAS评分治疗前治疗1周治疗2周治疗4周治疗6周治疗8周A组3056.7±5.844.9±4.737.1±4.831.5±4.226.6±3.823.2±2.8B组2956.5±6.149.0±6.942.1±6.836.0±7.130.3±5.324.9±4.8组间F值=6.729 P值=0.012时点间F值=942.449 P值=0.000组间·时点间F值=6.403 P值=0.001
2.2 2组不良反应比较 A组5例(16.7%)出现不良反应(其中4例于服药第1周出现轻度头晕、嗜睡症状,均能耐受,治疗2周后症状逐渐缓解,1例于治疗后第8周出现共济失调症状)。B组12例(41.4%)出现不良反应(其中5例患者服药第1周出现口干、便秘症状;4例患者出现头晕、嗜睡症状;2例出现视物模糊;1例出现心悸症状)。A组不良反应发生率显著低于B组(χ2=4.390,P<0.05)。
所有患者在治疗后进行血常规、肝肾功能检查,均未发现明显异常。
3 讨 论
急性带状疱疹常常伴有持续和严重慢性疼痛发生的风险,约10%~20%的带状疱疹患者可出现PHN症状[5]。PHN危险因素主要是年龄以及机体免疫力降低,还与急性期皮损严重程度、发病部位及疼痛强度相关[6-7],发生率随年龄增加[8],60岁以上带状疱疹患者发生PHN达65%[9]。PHN的发病机制尚未完全清楚,目前认为其可能的作用机制有:带状疱疹病毒感染可引起外周及中枢神经的损伤,导致其处于超敏状态,自发放电阈值降低,对刺激呈超常反应。神经元的超兴奋性在某种程度上与神经元的分子通道的改变有关,其中包括钠离子通道的改变、对疼痛起抑制作用的氨基丁酸的改变等[10]。PHN除疼痛本身外,尚对患者睡眠、情绪、功能状态和健康相关生活质量产生负面影响[11-12],部分长期疼痛患者因得不到有效治疗而使生活质量下降,甚至导致机体其他功能损伤或产生严重的心理疾病,并给患者造成沉重的经济负担。
目前临床治疗PHN常用药物包括加巴喷丁类药物、三环类抗抑郁药、阿片类药物等[13]。普瑞巴林属于加巴喷丁类药物,为新型γ-氨基丁酸受体激动剂,2004年12月美国FDA批准其用于治疗糖尿病性神经痛及带状疱疹后神经痛。普瑞巴林可结合位于外周和中枢神经系统突触前电压门控性钙通道的α2-δ亚基,调节钙离子通道性,减少神经末梢钙离子内流以及活化神经元去甲肾上腺素、谷氨酸盐和P物质等突触神经递质的释放,减少兴奋信号传入神经中枢,进而有效控制神经病理性疼痛[14-15]。
本研究普瑞巴林组在治疗1周后患者VAS评分显著降低,并且其治疗后各观察时点疗效均优于阿米替林组。说明普瑞巴林治疗PHN起效快,疗效显著。本研究结果表明普瑞巴林能在治疗后第1周显著降低疼痛对患者睡眠的干扰程度,随着治疗时间的延长,疗效越显著,且效果明显优于阿米替林组;此外,普瑞巴林组能有效缓解患者焦虑程度,在治疗后第1周患者SAS评分显著降低,随着治疗时间的延长,改善患者的焦虑越显效,也优于阿米替林组。因此,相对于阿米替林,普瑞巴林能更有效、更快减轻PHN,同时降低疼痛对睡眠的干扰,有效缓解患者焦虑。普瑞巴林可诱发不同程度的不良反应,与其他研究类似[16-17]。本研究中普瑞巴林不良反应为头晕、嗜睡、共济失调,其不良反应发生率较阿米替林低。有研究发现普瑞巴林不良反应以轻、中度为主,重度的不良反应与剂量有关,在用于治疗PHN时,建议从低剂量开始,逐渐加量[18]。
目前普瑞巴林用于PHN的治疗方案包括固定剂量及可变剂量2种。固定剂量常为第1周时300 mg/d,随后均为600 mg/d;而可变剂量则根据患者对药物的反应性和耐受性,从150 mg/d开始,每周剂量递增150 mg/d,直至最大剂量600 mg/d,随后保持该剂量不变,维持用药时间为4~12周。研究证实,与安慰剂组相比,可变剂量和固定剂量均可显著降低疼痛评分,改善睡眠及生活质量。本研究采用的是普瑞巴林可变剂量的方法,从75 mg、2次/d开始,于治疗后第1周末调整为150mg、2次/d,此后维持300mg/d的剂量就能够较好的控制症状。该治疗方法在快速减轻患者疼痛症状及减少疼痛对患者睡眠影响程度的同时,还能减轻患者焦虑程度,降低药物的不良反应,值得临床推广。
[1] 张学军.皮肤性病学[M].北京:人民卫生出版社,2013:65-67.
[2] 带状疱疹后神经痛诊疗共识编写专家组.带状疱疹后神经痛诊疗中国专家共识[J].中国疼痛医学杂志,2016,22(3):161-167.
[3] Schhereth T,Heiland A,Breimhorst M,et al. Association between pain,central sensitization and anxiety in postherpetic neuralgia[J]. Eur J Pain,2015,19(2):193-201.
[4] Hall TD,Shah S,Ng B,et al. Changes in mood,depression and suicidal ideation after commencing pregabalin for neuropathic pain[J]. Aust Fam Physician,2014,43(10):705-708.
[5] Hiom S,Patel GK,Newcombe RG,et al. Severe postherpetic neuralgia and other neuropathic pain syndromes alleviated by topical gabapentin[J]. Br J Dermatol,2015,173(1):300-302.
[6] Makharita MY. Prevention of post-herpetic neuralgia from 4 dream to reality:aten-step model [J]. Pain Physician,2017,20(2):E209-220.
[7] Chen JY,Lan KM,Sheu MJ,et al. Peptic ulcer as a risk factor for postherpetic neuralgia in adult patients with herpes zoster[J]. J Med Virol,2015,87(2):222-229.
[8] Takao Y,Miyazaki Y,Okeda M,et al. Incidences of herpes zoster and postherpetic neuralgia in Japanese adults aged 50 years and older from a community-based prospective cohort study:the SHEZ study[J]. J Epidemiol,2015,25(10):617-625.
[9] Opstelten W,Van Wijck AJ,Van Essen GA,et al. The PINE study: rationale and design of a randomized comparison of epidural injection of local anaesthetics and steroids versus care-as-usual to prevent postherpetic neuralgia in the elderly[J]. BMC Anesthesiol,2004,4(1):2.
[10] Kinchington PR,Goins WF. Varicella zoster virus-induced pain and post-herpetic neuralgiain the human host and in rodent animal models[J]. J Neurovirol,2011,17(6): 590-599.
[11] Johnson RW,Bouhassira D,Kassianos G,et al. The impact of herpes zoster and post-herpetic neuralgia on quality-of-life[J]. BMC Med,2010,8:37.
[12] Hadley GR,Gayle JA,Ripoll J,et al. Post-herpetic neuralgia:a review [J]. Curr Pain Headache Rep,2016,20(3):17.
[13] 杜玉敏,任玉娥,丛海静,等.疼痛管理对带状疱疹后神经痛患者治疗效果的影响[J].河北医科大学学报,2016,37(3):293-295,300.
[14] Sampathkumar P,Darge LA,Martin DP. Herpes zoster(shingles) and postherpetic neuralgia[J]. Mayo Clin Proc,2009,84(3):274-280.
[15] 孙龙.干扰素联合普瑞巴林治疗带状疱疹后遗神经痛效果观察[J].山东医药,2017,57(26):76-77.
[16] 罗宏丽,肖顺林,王海雪.普瑞巴林治疗带状疱疹后神经痛的临床评价[J].医药报导,2017,36(3):336-341.
[17] 吴潞明,邹旭辉,郑博文,等.普瑞巴林治疗44例带状疱疹后神经痛疗效观察[J].皮肤病与性病,2015,37(2):102-104.
[18] 尹君.普瑞巴林治疗带状疱疹后遗神经痛的疗效:随机对照试验的Meta分析[D].杭州:浙江大学,2016.