变应性鼻炎(allergic rhinitis,AR)是患者吸入致敏原后触发的由 IgE介导的鼻腔黏膜变态反应和2型辅助性T细胞(T helper 2 cell,Th2)驱动的鼻腔黏膜炎症,打喷嚏、鼻痒、鼻阻塞、流清水样涕等为典型临床症状[1]。儿童鼻炎分为过敏性及非过敏性。AR是儿童最常见的慢性过敏性疾病之一。部分中重度AR患儿可以继发分泌性中耳炎、慢性鼻-鼻窦炎、支气管哮喘、阻塞性睡眠呼吸暂停低通气综合征等并发症[2]。中重度AR严重影响患儿的身心健康。近年来,伴随生活方式改变、空气污染加重及城市化进程,我国AR的发病率呈逐年增长的趋势[3]。胡思洁等[4]通过对中国大陆AR发病率和危险因素的Meta分析研究发现,儿童AR发病率高于成人,不同地区差异明显。由于儿童自身鼻部解剖及生理特点,治疗儿童AR具有特异性,临床疗效和用药安全要兼顾,鼻腔冲洗是治疗AR的安全有效方法[5]。抗过敏药物是儿童AR最常用的治疗手段之一。AR诊疗指南目前将鼻喷激素同口服抗组胺剂列为一线用药[6]。本研究观察生理性海水联合糠酸莫米松鼻喷剂及依巴斯汀对患儿鼻部症状及体征的影响,旨在探讨治疗儿童中重度AR的优化方案。
1 资料与方法
1.1 一般资料 按照AR诊疗指南(2015年,天津)中的诊断标准及根据疾病严重程度的分型[6],选取2015年8月—2018年8月河北省石家庄市第一医院耳鼻咽喉头颈外科门诊就诊的中重度AR患儿80例,均经变应原皮内试验确诊。入组标准: ①中重度AR病程持续4周以上且每周发作时间超过4 d,疾病对患儿的学习和生活质量有严重影响;②发病年龄4~14岁,性别不限;③患儿有明确的变应原接触史及典型的AR症状和特异性体征;④变应原皮内试验阳性,并且1种或以上变应原为(++)或(++)以上。排除标准:①合并鼻息肉、严重鼻中隔偏曲、先天性鼻腔畸形等鼻部解剖异常;②实验前2周内应用过抗过敏药物;③试验前6周曾行鼻腔鼻窦手术;④试验前1年内应用过特异性免疫治疗;⑤合并急性上呼吸道感染或其他急性炎性疾病;⑥合并全身严重器质性疾病或免疫性疾病;⑦合并严重哮喘;⑧经过培训及沟通不能正确使用药物、不能进行视觉模拟评分法(Visual Analogue Scale,VAS)评分或不能及时随访者。按照随机数字表将患儿分为对照组和试验组各40例。对照组男性19例,女性21例,年龄5~14岁,平均(8.93±2.83)岁;试验组男性20例,女性20例,年龄4~14岁,平均(8.98±2.81)岁。2组性别、年龄差异均无统计学意义(P>0.05),具有可比性。
本研究经医院伦理委员会批准通过;均获得患儿家长知情同意。
1.2 方法 对照组采用外用糠酸莫米松鼻喷剂(内舒拿)和依巴斯汀片(开思亭)治疗。外用糠酸莫米松鼻喷剂用法:12岁以上儿童,每侧鼻孔2 喷,1次/d (总量为200 μg);3~11 岁儿童,每侧鼻孔1喷,1次/d (总量为100 μg)。依巴斯汀片(开思亭)口服方法:12岁以上儿童,10 mg,1次/d;6~11岁儿童,5 mg,1次/d;4~5岁儿童,2.5 mg,1次/d。试验组在对照组基础上联合应用生理性海水(鼻朗)。使用方法:3次/d,每侧鼻孔每次2喷。冲洗后将冲洗液擤出。糠酸莫米松喷鼻剂和依巴斯汀用药剂量及使用方法同对照组。2组疗程均为8周。治疗期间叮嘱患儿及家属停用其他抗过敏药物和影响鼻腔通气的药物。
对AR患儿进行随访并评分。通过电话及门诊随访的方式指导患儿用药,监测药物不良反应,了解患儿症状改善、体征变化等情况。
1.3 观察指标 分别于治疗前、治疗后4周、治疗后8周评估2组鼻相关症状VAS评分、体征评分和不良反应发生情况。VAS评分:使用VAS评分评估AR患者的鼻部症状(包括鼻阻塞、鼻痒、打喷嚏及流清水样涕)。让家长帮助患儿于10 cm标尺上,按照自己感到的鼻部症状痛苦程度,依据以下评判标准进行记分:无症状0分;症状轻微记录<4分;症状严重,但患者能承受4~6分;患者不能耐受的严重症状记录>6~10分。
鼻腔体征评分:通过鼻内镜观察患儿下鼻甲形态、下鼻甲与中鼻甲及鼻中隔解剖位置关系、鼻腔容积等情况,进行鼻腔体征量化评分。具体鼻腔体征记分标准见表1。
表1 鼻腔体征评分标准
Table 1 The standard of nasal signs score

鼻腔体征0分1分2分 3分下鼻甲形态正常 稍显苍白肿胀明显肿胀严重水肿 鼻腔容积 宽敞 轻度减少 明显减少严重减少,甚至完全阻塞 中鼻甲暴露可窥及可窥及 部分窥及 下甲紧贴鼻中隔,不能窥及中鼻甲
不良反应:治疗期间注意密切观察患儿不良反应,分为局部不良反应和全身不良反应。 局部不良反应包括用药后出现鼻黏膜干燥、鼻部出血以及局部皮肤红肿和(或)瘙痒等。全身不良反应按照症状的轻重程度进行分级[7]:0 级,未发现患儿全身症状;Ⅰ级,出现轻度全身不良反应症状;Ⅱ级,治疗过程中出现中度全身不良反应症状;Ⅲ级,出现严重的全身不良反应症状,但尚不致命;Ⅳ级:出现过敏性休克症状。
1.4 疗效评价 根据治疗前后鼻部症状总积分,按下列公式算出治疗后积分下降指数,患者用药后的积分下降指数=(用药前积分-用药后积分)/用药前积分×100%,积分下降指数的数值越大表明疗效越好。≥66%为显效,>25%~65%为有效,≤25%为无效。总有效率=(显效例数+有效例数)/总例数×100%。
1.5 统计学方法 应用SPSS 22.0统计软件分析数据。计量资料比较采用重复测量的方差分析;计数资料比较采用χ2检验;等级资料比较采用秩和检验。P<0.05为差异有统计学意义。
2 结 果
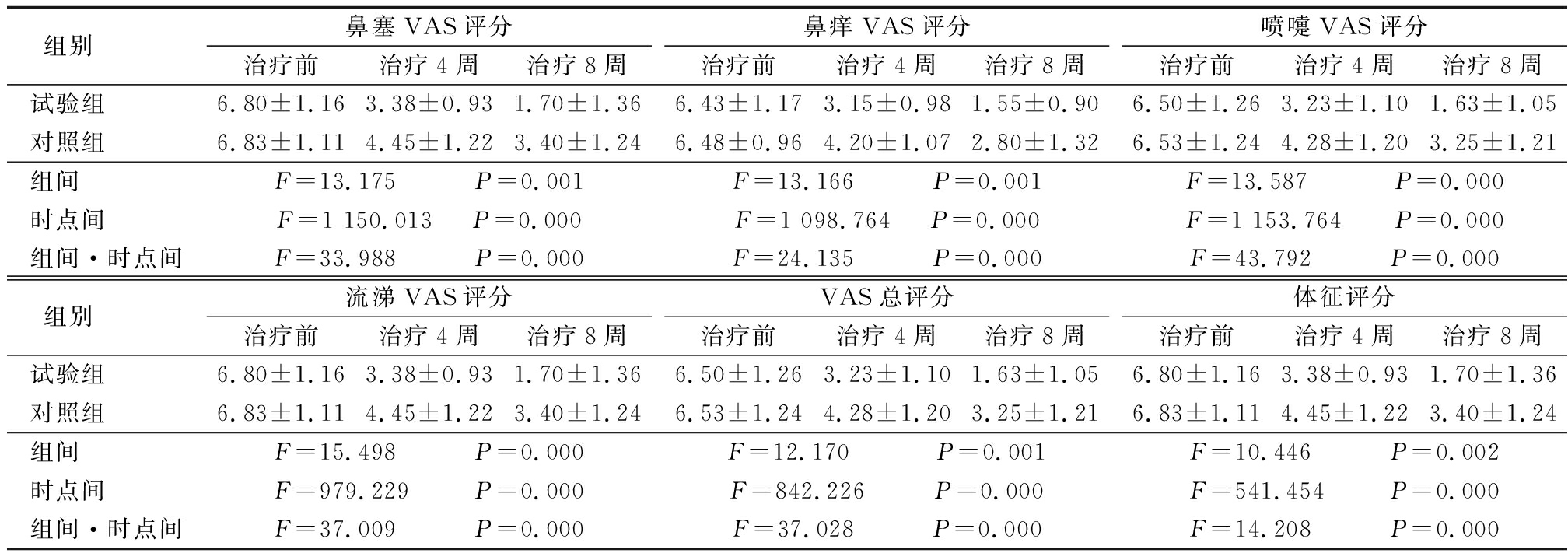
2.1 2组鼻症状VAS评分及体征评分比较 治疗后,2组鼻塞VAS评分、鼻痒VAS评分、喷嚏VAS评分、流涕VAS评分、总VAS评分和体征评分均呈逐渐降低趋势,且试验组各评分降低幅度大于对照组,其组间、时点间、组间·时点间交互作用差异均有统计学意义(P<0.05),见表2。
表2 2组治疗前后鼻症状VAS评分及体征评分比较
Table 2 Comparison of VAS score and signs score before and after treatment between two groups ![]() 分)
分)
组别 鼻塞VAS评分治疗前治疗4周治疗8周鼻痒VAS评分治疗前治疗4周治疗8周喷嚏VAS评分治疗前治疗4周治疗8周试验组 6.80±1.163.38±0.931.70±1.366.43±1.173.15±0.981.55±0.906.50±1.263.23±1.101.63±1.05对照组 6.83±1.114.45±1.223.40±1.246.48±0.964.20±1.072.80±1.326.53±1.244.28±1.203.25±1.21组间 F=13.175 P=0.001F=13.166 P=0.001F=13.587 P=0.000时点间 F=1 150.013 P=0.000F=1 098.764 P=0.000F=1 153.764 P=0.000组间·时点间F=33.988 P=0.000F=24.135 P=0.000F=43.792 P=0.000组别 流涕VAS评分治疗前治疗4周治疗8周VAS总评分治疗前治疗4周治疗8周体征评分治疗前治疗4周治疗8周试验组 6.80±1.163.38±0.931.70±1.366.50±1.263.23±1.101.63±1.056.80±1.163.38±0.931.70±1.36对照组 6.83±1.114.45±1.223.40±1.246.53±1.244.28±1.203.25±1.216.83±1.114.45±1.223.40±1.24组间 F=15.498 P=0.000F=12.170 P=0.001F=10.446 P=0.002时点间 F=979.229 P=0.000F=842.226 P=0.000F=541.454 P=0.000组间·时点间F=37.009 P=0.000F=37.028 P=0.000F=14.208 P=0.000
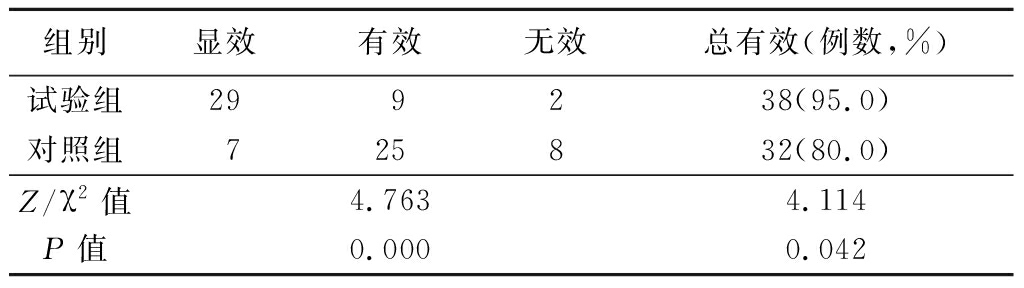
2.2 2组临床疗效比较 试验组临床疗效优于对照组,总有效率高于对照组,差异均有统计学意义(P<0.05),见表3。
表3 2组临床疗效比较
Table 3 Comparison of clinical efficacy between two groups (n=40,例数)
组别显效有效无效总有效(例数,%)试验组299238(95.0)对照组725832(80.0)Z/χ2值4.7634.114P值0.0000.042
2.3 安全性 试验组未发现明显全身不良反应及局部反应。对照组发生鼻出血1例,鼻干3例,停药后缓解。2组均无过敏性休克等全身严重不良反应。2组不良反应发生率差异无统计学意义(χ2=2.368,P=0.123)。
3 讨 论
AR在小儿耳鼻喉疾病中有较高的发病率。伴随城市化发展、环境污染加重、汽车尾气及PM2.5的增加,儿童和成人AR的发病率呈现逐年增长趋势。流行病学研究表明,在发达国家,AR的流行率在逐步升高,目前影响到全世界10%~40%的成年人和2%~25%的儿童[3]。儿童AR的疾病特点与成人存在较大差异:在相同年龄段患儿中,男性儿童AR的发病率较女性高;幼龄儿童AR的发病率比年长儿童高;城镇儿童AR的患病率较乡村儿童高[3]。按照AR的严重程度进行分类,可分为轻度AR和中重度AR。轻度AR症状比较轻微,对学习及生活质量无明显影响;中重度AR症状较严重,对学习及生活质量有较严重的影响。
AR治疗包括抗过敏药物治疗、免疫治疗及外科治疗等。传统手术治疗AR近期效果不错,但远期疗效待观察,且存在并发症,外科治疗AR存在争议[8]。而免疫治疗则需要患儿家长陪同按时脱敏治疗,存在治疗周期长且费用较高等不足。近些年来,药物联合治疗儿童中重度AR成为研究热点。儿童因免疫力较成年人低,儿童的特殊体质极易受外界环境因素影响,故儿童AR的治疗与成年人存在一定差异。对儿童中重度AR的防控是三位一体的系统体系,包括环境中致敏原的控制、抗过敏药物治疗、特异性免疫治疗、患儿及家长的健康教育。其中抗过敏药物治疗在耳鼻喉科临床最为常用。在AR诊治指南(2015年,天津)中,鼻用糖皮质激素、口服二代抗组胺药均已经成为治疗AR的一线用药。
鼻用糖皮质激素具有使用方便、疗效确切、安全性较高等优点,可直接与鼻腔黏膜上的激素受体结合,产生局部抗感染、减轻鼻腔黏膜水肿等作用,对缓解中重度AR患者鼻部症状[9]以及改善其工作、学习和生活质量均有明显的作用。日本学者认为激素不仅对治疗AR有明显效果,短期预防性应用鼻喷激素还可以有效预防季节性AR[10]。国外研究发现,鼻喷激素治疗鼻息肉和常年性AR后,嗜酸粒细胞炎症参数指标显著降低[11]。糠酸莫米松鼻喷剂为第3代鼻用糖皮质激素,在治疗AR过程中较其他种类鼻喷激素鼻黏膜抗过敏作用更强,并且还具有生物利用度低、不良反应少等优点。Dibildox[12]对糠酸莫米松鼻喷剂治疗儿童AR的疗效及安全性进行研究,发现治疗后糠酸莫米松鼻喷剂组患儿症状评分低于安慰剂组,且无明显不良反应。糠酸莫米松鼻喷剂的主要作用机制是能使AR患者鼻腔黏膜血管通透性降低,鼻腔黏膜上腺体对胆碱能刺激反应减低,抑制并降低炎性介质的产生和释放,可减少炎症细胞因子产生,并能减弱嗜酸粒细胞等炎性细胞的趋化和移动,从而抑制AR的炎症进程。另外,糠酸莫米松鼻喷剂还能够改善AR患者鼻黏膜上皮形态,而且长期应用后一般不会出现减充血剂引起的鼻腔黏膜萎缩。
组胺为鼻黏膜变态反应发病进程中的核心炎症介质。抗组胺剂为治疗AR和慢性荨麻疹等过敏性疾病中应用最广泛的药物之一。依巴斯汀为二代口服抗组胺剂,可有效治疗季节性和常年性AR。依巴斯汀有起效迅速、抗过敏作用持久等优点。老年AR患者合并肾性或轻至中度高血压不需要剂量调整。一代抗组胺药往往对患者认知功能、精神活动、心血管功产生不良反应,依巴斯汀一般耐受性好,不良反应很少。钟康华[13]研究发现,变应性鼻炎患者应用依巴斯汀联合布地奈德治疗后血清白细胞介素4、白细胞介素6及白细胞介素10等炎症指标降低幅度大于对照组,有效率高于对照组,且无明显不良反应。二代抗组胺剂没有明显的中枢抑制作用,且对变态性反应中的炎性介质具有长期抑制作用[14],已慢慢代替一代抗组胺剂。H1受体拮抗剂与H1受体相结合,进而与组胺竞争间接抑制组胺相关的炎症反应,对控制AR速发相有重要作用。
鼻腔冲洗已经普遍应用于鼻窦炎、鼻炎治疗以及鼻内镜术后鼻腔和鼻窦的清洗。鼻腔冲洗具有携带方便、操作简单、耐受性良好等优点,鲜有不良反应发生[15]。因生理性海水中无任何药物成分,更易被患儿家长所接受。Head等[16]研究发现,盐水鼻腔冲洗治疗成人及儿童AR较对照组效果更明显,并且治疗期间无明显不良反应产生。Jung等[17]临床研究发现,鼻盐水灌洗治疗AR合并支气管哮喘儿童,各项指标改善明显优于对照组,其能对AR患儿的鼻部过敏症状显著缓解,并有助于改善患儿的生活学习质量。鼻腔冲洗可明显降低AR患者鼻腔中组胺浓度,还可以抑制炎症细胞和白三烯等炎性介质的释放。鼻腔冲洗有良好的耐受性,价格低廉,易于使用,安全性高,对成人和儿童AR患者均能明显改善鼻部症状、减少药物用量、增加黏膜纤毛清除速度,从而改善AR患者生活质量。但是对于中重度AR患者,单用鼻腔灌洗治疗效果欠佳。采用药物和鼻生理盐水联合治疗可以改善AR症状,最大限度提高药物的疗效,在儿童群体中有很好的耐受性。杜经纬等[18]应用鼻腔冲洗及鼻喷激素联合治疗AR,可有效降低患者呼出一氧化氮浓度,在一定程度上改善了患者肺功能,提高了患者的生活质量。国内张进等[19]在药物联合鼻腔冲洗的临床研究中发现,鼻腔冲洗联合鼻喷激素治疗AR,在改善鼻部不适症状、提高生活质量方面均较对照组有更明显的效果,并且实验过程中未发现明显不良反应。生理性海水鼻腔喷雾器通过独特的微喷技术,打破生理性海水表面的张力,使生理性海水产生雾化,雾化液均匀分布于鼻腔内,达到冲洗鼻腔内细菌、过敏原等有害物的目的。另外,生理性海水内富含多种微量元素,这些微量元素在杀灭细菌、对抗变态反应过程中很有意义,生理性海水不但可以清洗鼻腔内环境,还可以改善鼻腔各项生理功能。因为儿童鼻腔较成人狭窄,且年幼儿童不能自行擤鼻,鼻腔鼻涕及各类变应原容易存留于鼻腔黏膜表面。生理性海水鼻腔喷雾器能够稀释排除鼻腔中的鼻涕、致病菌、过敏原,减轻过敏原引起的鼻部过敏反应,减少鼻部炎症细胞浸润及炎症因子的浓度。生理性海水还有湿润鼻腔的作用,减少药物引起的鼻腔干燥、鼻出血等局部不良反应,能有效改善鼻塞、鼻痒、鼻干、鼻痂、打喷嚏、流清水样涕等不适,适用于婴儿、儿童及成人等各个年龄段,无明显使用禁忌证。本研究应用生理性海水鼻腔喷雾器治疗各种鼻腔、鼻窦疾病,其操作简单,具有良好的安全性和耐受性,是防治儿童AR安全有效的手段。
本研究结果显示,2组鼻症状VAS评分均呈逐渐降低趋势,2组鼻部症状VAS总评分及鼻塞VAS评分、鼻痒VAS评分、打喷嚏VAS评分、流涕VAS评分均较用药前明显降低,说明2种方法均有助于缓解中重度AR患儿鼻部症状;试验组鼻部症状VAS总评分及鼻塞VAS评分、鼻痒VAS评分、打喷嚏VAS评分、流涕VAS评分低于对照组,其组间、时点间、组间·时点间交互作用差异有统计学意义,试验组临床疗效优于对照组,总有效率高于对照组,证明生理性海水联合糠酸莫米松鼻喷雾剂、依巴斯汀治疗中重度AR的效果更加显著;试验组体征评分低于对照组,表明生理性海水联合药物治疗中重度AR不仅可以明显改善症状,而且对减轻鼻甲的苍白水肿、减少鼻腔分泌物也有明显效果;在治疗阶段,试验组未发现严重全身不良反应及局部不良反应,对照组出现鼻出血1例,鼻干3例,均停药后缓解,未发现其他明显严重不良反应,考虑生理性海水联合药物治疗的过程中,由于应用生理性海水对鼻腔黏膜有湿润作用降低了鼻喷激素引起的鼻干、鼻出血等不良反应。因此,生理性海水联合糠酸莫米松鼻喷剂、依巴斯汀在治疗儿童中重度AR过程中可以联合发挥作用,弥补各自的不足,从而有效缓解中重度AR患儿的临床症状,明显改善体征,并有助于降低药物联合治疗引发的局部不良反应。
综上所述,生理性海水鼻腔冲洗是安全有效治疗儿童中重度AR的方法,具有使用简单、携带方便、费用低廉等优点;并且鼻腔冲洗联合药物治疗有助于增加疗效,缩短用药疗程,降低经济负担,减少药物不良反应。目前,生理性海水鼻腔冲洗的安全性及有效性在治疗鼻科多种疾病中均得到了印证,但由于研究时间有限,远期效果尚不能明确。在今后临床工作中需要继续增加研究对象的数量,进行随机对照试验,并从细胞学和分子生物学的层面证实生理性海水在治疗儿童中重度AR的作用,以指导临床实践。
[1] Almehizia AA,AlEssa RK,Alwusaidi KM,et al. Allergic rhinitis:Disease characteristics and coping measures in Saudi Arabia[J]. PLoS One,2019,14(6):e217182.
[2] 中国医师协会儿科医师分会儿童耳鼻咽喉专业委员会.儿童过敏性鼻炎诊疗——临床实践指南[J].中国实用儿科杂志,2019,34(3):169-175.
[3] Zhang Y,Zhang L. Increasing prevalence of allergic rhinitis in China[J]. Allergy Asthma Immunol Res,2019,11(2):156-169.
[4] 胡思洁,魏萍,寇巍,等.变应性鼻炎患病率及危险因素Meta分析[J].临床耳鼻咽喉头颈外科杂志,2017,31(19):1485-1491.
[5] 谭路,许昱.鼻腔盐水冲洗在鼻部炎性疾病中的应用[J].临床耳鼻咽喉头颈外科杂志,2019,33(1):90-95.
[6] 中华医学会耳鼻咽喉头颈外科学分会鼻科学组,中华耳鼻咽喉头颈外科杂志编辑委员会鼻科组.变应性鼻炎诊断和治疗指南(2015年,天津)[J].中华耳鼻咽喉头颈外科杂志,2016,51(1):6-24.
[7] 钱建娥,陶丹丹,黄超.皮下注射与舌下含服免疫疗法对儿童变应性鼻炎的疗效及安全性比较[J].中国中西医结合耳鼻咽喉科杂志,2017,25(3):196-199.
[8] 张铭,刘春苗,任秀敏,等.变应性鼻炎外科治疗的临床疗效观察[J].河北医科大学学报,2017,38(1):121-124.
[9] Urdaneta E,Tunceli K,Gates D. Effect of mometasone furoate nasal spray on moderate-to-severe nasal congestion in seasonal allergic rhinitis:a responder analysis[J]. Allergy Asthma Proc,2019,40(3):173-179.
[10] Haruna T,Kariya S,Higaki T,et al. Determining an appropriate time to start prophylactic treatment with intranasal corticosteroids in Japanese cedar pollinosis[J]. Med Sci (Basel),2019,7(1).pii:E11.
[11]  padijer Mirkoviĉ C,Periĉ A,Vukomanoviĉdurdeviĉ B,et al. Effects of fluticasone furoate nasal spray on parameters of eosinophilic inflammation in patients with nasal polyposis and perennial allergic rhinitis[J]. Ann Otol Rhinol Laryngol,2017,126(8):573-580.
padijer Mirkoviĉ C,Periĉ A,Vukomanoviĉdurdeviĉ B,et al. Effects of fluticasone furoate nasal spray on parameters of eosinophilic inflammation in patients with nasal polyposis and perennial allergic rhinitis[J]. Ann Otol Rhinol Laryngol,2017,126(8):573-580.
[12] Dibildox J. Safety and efficacy of mometasone furoate aqueous nasal spray in children with allergic rhinitis:results of recent clinical trials[J]. J Allergy Clin Immunol,2001,108(1 Suppl):S54-58.
[13] 钟康华.依巴斯汀联合布地奈德治疗变应性鼻炎的临床效果观察[J].临床合理用药杂志,2018,11(29):93-94.
[14] Hishinuma S,Sugawara K,Uesawa Y,et al. Differential thermodynamic driving force of first- and second-generation antihistamines to determine their binding affinity for human H1 receptors[J]. Biochem Pharmacol,2014,91(2):231-241.
[15] 孙称心,高瑞尧,底孟林茜.洗鼻疗法结合花粉阻隔剂对妊娠期变应性鼻炎患者的疗效观察[J].河北医科大学学报,2016,37(10):1188-1191.
[16] Head K,Snidvongs K,Glew S,et al. Saline irrigation for allergic rhinitis[J]. Cochrane Database Syst Rev,2018,6:CD012597.
[17] Jung M,Lee JY,Ryu G,et al. Beneficial effect of nasal saline irrigation in children with allergic rhinitis and asthma:a randomized clinical trial[J]. Asian Pac J Allergy Immunol,2019[Epub ahead of print].
[18] 杜经纬,冯俊,马鹏,等.鼻腔冲洗联合鼻用糖皮质激素对AR患者FeNO、肺功能及生活质量的影响[J].山东大学耳鼻喉眼学报,2019,33(1):124-127.
[19] 张进,罗惠方.鼻腔冲洗在变应性鼻炎治疗中的作用[J].临床合理用药杂志,2017,10(11):85-86.