心力衰竭(heart failure,HF)是各种心血管疾病的严重并发症,病死率高,严重影响着人们的健康。近期PARADIGM-HF突破了HF治疗的平台,该研究显示,沙库巴曲缬沙坦(Sacubitril/Valsartan,Sac/Val)可进一步降低射血分数降低心力衰竭(heart failure with reduced ejection fraction,HFrEF)患者的心血管病死率及HF再住院率[1]。多中心、前瞻性、随机临床试验显示,急性前壁心肌梗死经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)术时应用重组人脑利钠肽(recombinant human brain natriuretic peptide,rhBNP)可降低心肌损伤程度,抑制心室重构,改善心脏功能[2]。鉴于,Sac/Val是由血管紧张素受体抑制剂和内啡肽酶抑制剂(angiotensin receptor neprilysin inhibitor,ARNI)组成的复合制剂,不仅可以抑制内源性内啡肽酶降解,增加心钠肽(atrial natriuretic peptide,ANP)、脑钠肽(brain natriuretic peptide,BNP)和C型钠尿肽(C-type natriuretic peptides,CNP)浓度,同时具有抑制肾素-血管紧张素-醛固酮系统(renin-angiotensin-aldosterone system,RAAS)双重作用。Sac/Val可抑制急性心肌梗死(acute myocardial infarction,AMI)后心室重构,预防和延缓HF的进展,改善患者预后。本研究通过观察血浆N-末端脑利钠肽(N-terminal brain natriuretic peptide,NT-proBNP)浓度及超声心动图参数的变化,评估Sac/Val对急性前壁心肌梗死PCI术后HFrEF患者心功能的影响。
1 资料与方法
1.1 一般资料 选取2018年7月—2019年2月就诊于河北医科大学第二医院的急性前壁ST段抬高型心肌梗死(ST-segment myocardial infarction, STEMI)于PCI术后合并HFrEF患者160例。按随机数字表法分为观察组80例,男性69例,女性11例,年龄33~75岁,平均(59.0±10.3)岁,平均体重指数28.60±6.20;合并高血压32例,糖尿病19例,血脂异常37例,吸烟54例;对照组80例,男性67例,女性13例,年龄36~74岁,平均(58.0±10.4)岁,平均体重指数27.80±5.60;合并高血压37例,糖尿病15例,血脂异常46例,吸烟50例。2组患者性别、年龄、体重指数及病史等方面差异均无统计学意义(P>0.05),具有可比性。
本研究经医院医学伦理委员会审批通过,所有患者签署知情同意书。
1.2 入选标准及排除标准 入选标准:①符合急性前壁STEMI诊断标准;②心脏彩色超声提示左心室射血分数(left ventricular ejection fraction,LVEF)≤40%;③18岁≤年龄<75岁;④BNP≥150 ng/L,或NT-proBNP≥600 μg/L;⑤均在心肌梗死时间窗内行PCI治疗。排除标准:①肾小球滤过率≤30 mL·min-1·1.73m-2;②血钾>5.4 mmol/L;③血管性水肿病史及不能耐受血管紧张素转化酶抑制剂(angiotensin converting enzyme inhibitior,ACEI)或血管紧张素受体抑制剂(angiotensin receptor blocker,ARB);④严重肝功能障碍;⑤既往有心肌梗死病史;⑥心房颤动;⑦严重心脏瓣膜病;⑧心肌梗死合并主动脉夹层。
1.3 研究方法 纳入研究的患者PCI术后均接受指南推荐抗血小板、稳定斑块治疗,并在血流动力学稳定情况下接受ACEI/ARB、β受体阻滞剂及醛固酮类(由内科医生评估)。观察组由ACEI或ARB转换为Sac/Val(诺信托,北京诺华制药有限公司)前停服ACEI 36 h或ARB 24 h。Sac/Val起始剂量(25 mg 2次/d,或50 mg 2次/d),每2周递增剂量,直至个体耐受最大剂量(由内科医生决定)。对照组缬沙坦(Valsartan,Val)(代文,北京诺华制药有限公司)起始剂量(20 mg或40 mg 1次/d),药物滴定与观察组相似。
1.3.1 血浆NT-proBNP测定 所有受试者于术后1周(基线)、4周、12周及24周抽血化验,测定血浆NT-proBNP浓度。
1.3.2 超声心动图检测 所有患者于PCI术后1周、6个月行心脏超声检查。测定患者左心室舒张末容积(left ventricular end-diastolic volume,LVEDV)、左心室收缩末容积(left ventricular final systolic volume,LVESV)、室壁运动积分(wall motion score index,WMSI),每次测量3个心动周期,求取平均值。利用改良的简化双平面辛普森(simpson)法,计算LVEF。所有超声参数测定都是由超声科医生在不知分组情况下进行。
1.4 观察指标 血浆NT-proBNP浓度及心脏彩色超声参数变化(LVEDV、LVESV、LVEF、WMSI),评估患者心功能情况。主要终点事件为LVEF变化≥5%。次要终点事件:主要不良的心血管事件(major adverse cardiovascular events,MACE)(心绞痛发作、HF再住院率,室性心律失常,心源性死亡)及不良事件(血管性水肿、肾功能恶化、高血钾、低血压、干咳)。
1.5 统计学方法 应用SPSS 25.0统计软件处理数据。计量资料比较分别采用独立样本的t检验、配对t检验和重复测量的方差分析。计数资料比较采用χ2或连续校正的χ2检验。P<0.05为差异有统计学意义。
2 结 果
2.1 2组间不同时点NT-proBNP浓度比较 2组血浆NT-proBNP浓度基线值差异无统计学意义(P>0.05)。随着时间的推移,治疗期间2组NT-proBNP呈逐渐降低的趋势,观察组NT-proBNP低于对照组,且组间、时点间、组间·时点间交互作用差异均有统计学意义(P<0.01)。见表1。
表1 2组间不同时相NT-proBNP浓度比较
Table 1 The concentrations of NT-proBNP with different phases were compared between two groups![]()
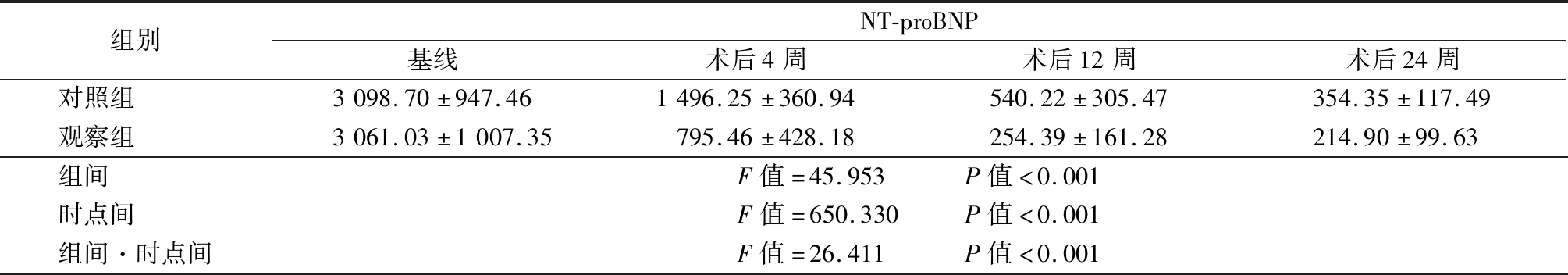
组别NT-proBNP基线术后4周术后12周术后24周对照组 3098.70±947.461496.25±360.94540.22±305.47354.35±117.49观察组 3061.03±1007.35795.46±428.18254.39±161.28214.90±99.63组间 F值=45.953 P值<0.001时点间 F值=650.330 P值<0.001组间·时点间F值=26.411 P值<0.001
2.2 心脏彩色超声参数的比较 2组LVEDV、LVESV、LVEF及WMSI的基线值比较,差异无统计学意义(P>0.05);随访结束时2组LVEF、WMSI均较基线明显改善(P<0.05),组间比较差异有统计学意义(P<0.05或P<0.01);随访6个月,观察组LVESV较基线明显缩小(P<0.05),但2组LVESV差异无统计学意义(P>0.05)。见表2。
表2 2组间心脏彩色超声参数比较
Table 2 Comparison of cardiac ultrasound parameters between two groups![]()
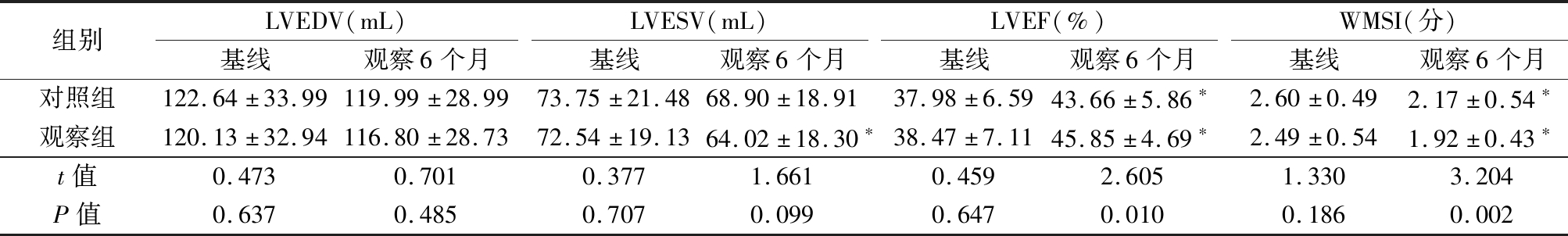
组别LVEDV(mL)基线观察6个月LVESV(mL)基线观察6个月LVEF(%)基线观察6个月WMSI(分)基线观察6个月对照组122.64±33.99119.99±28.9973.75±21.4868.90±18.9137.98±6.5943.66±5.86∗2.60±0.492.17±0.54∗观察组120.13±32.94116.80±28.7372.54±19.1364.02±18.30∗38.47±7.1145.85±4.69∗2.49±0.541.92±0.43∗t值0.4730.7010.3771.6610.4592.6051.3303.204P值0.6370.4850.7070.0990.6470.0100.1860.002
*P值<0.05与基线比较(配对t检验)
2.3 2组治疗前后血压、心率比较 2组收缩压均较基线时明显降低(P<0.05),但观察组收缩压降低更显著(P=0.038);2组舒张压、心率较基线时降低(P<0.05),但治疗后2组相比,舒张压、心率差异无统计学意义(P>0.05)。见表3。
2.4 不良反应发生率比较 2组不良反应发生率差异无统计学意义(P>0.05)。见表4。
2.5 2组MACE的比较 观察6个月,2组均未发生心血管疾病的死亡。2组相比,观察组HF再住院率和MACE发生率低于对照组(P<0.05)。见表5。
表3 2组间血压、心率比较
Table 3 Comparison of blood pressure and HR between the two groups![]()
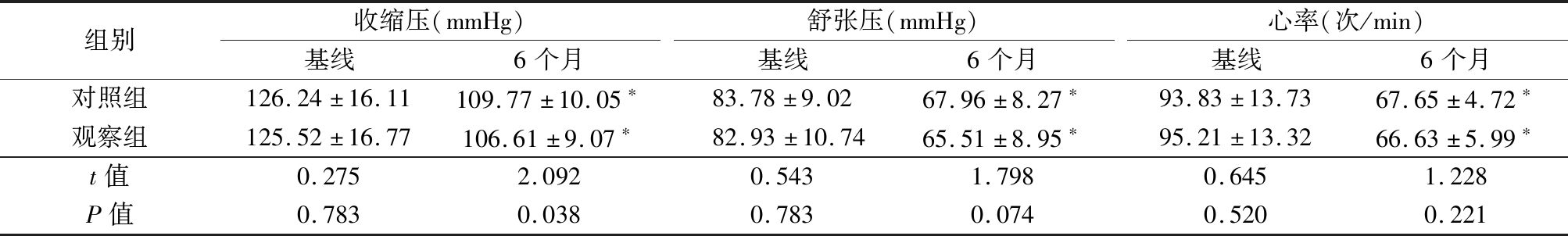
组别收缩压(mmHg)基线6个月舒张压(mmHg)基线6个月心率(次/min)基线6个月对照组126.24±16.11109.77±10.05∗83.78±9.0267.96±8.27∗93.83±13.7367.65±4.72∗观察组125.52±16.77106.61±9.07∗82.93±10.7465.51±8.95∗95.21±13.3266.63±5.99∗t值0.2752.0920.5431.7980.6451.228P值0.7830.0380.7830.0740.5200.221
*P值<0.05与基线比较(配对t检验) 1 mmHg=0.133 kPa
表4 2组不良反应发生率比较
Table 4 Comparison of adverse drug reaction between two groups (n=80,例数,%)
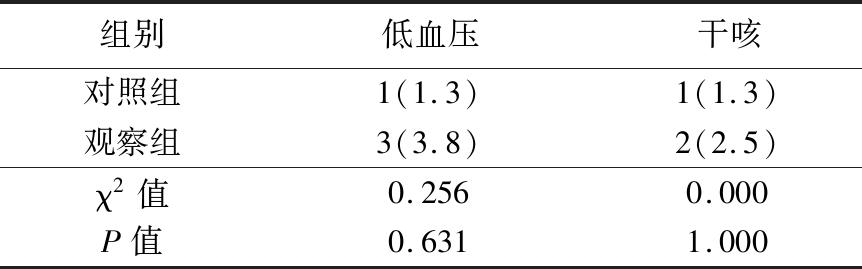
组别低血压干咳对照组1(1.3)1(1.3)观察组3(3.8)2(2.5)χ2值0.2560.000P值0.6311.000
表5 2组的MACE比较
Table 5 Comparison of MACE between the two groups (n=80,例数,%)
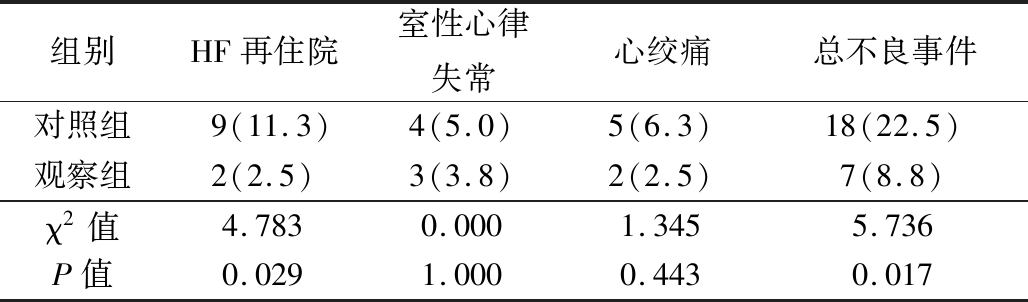
组别HF再住院室性心律失常心绞痛总不良事件对照组9(11.3)4(5.0)5(6.3)18(22.5)观察组2(2.5)3(3.8)2(2.5)7(8.8)χ2值4.7830.0001.3455.736P值0.0291.0000.4430.017
3 讨 论
随着对早期心肌再灌注理念的认识及介入技术的成熟,AMI的院内病死率明显降低,但心肌梗死后HF的发生率和病死率却依然很高。ARIC研究显示,有症状心肌梗死患者发生HF的风险是无心肌梗死患者的2.85倍[3],即使成功的实施了PCI治疗,仍有30%患者术后6个月发生了心室重构,增加了心肌梗死后HF和死亡的风险。因此,早期干预引起HF的不利因素,是预防心肌梗死后MACE的关键措施。
心肌梗死后有多种复杂的因素参与了HF的发生及发展,其中主要因素为心肌梗死后心室病理性重构和神经内分泌系统过度激活,且两者相互影响,加重对心肌的损伤;尤其是RAAS及交感神经系统(sympathetic nervous system,SNS)过度激活对心肌造成的持续损伤是HF进展的病理基础。在心肌梗死的早期,因大量心肌细胞丢失,心肌收缩力降低、心输出量减少,代偿性引起SNS兴奋和RAAS激活,使心输出量增加,维持血流动力学稳定,短期内对HF有利;但长期持续的RAAS及SNS过度激活,则会加重对心肌的损伤。(1)RAAS持续激活使循环血液或局部组织中血管进展素Ⅱ(angiotensin Ⅱ,AngⅡ)增多:①促进血管内皮细胞和平滑肌细胞增生肥厚,外周血管阻力增加,增加心脏的后负荷,使心肌耗氧量增加,促进心肌细胞凋亡、坏死;②使醛固酮分泌增加,引起水钠潴留,增加心脏前负荷,导致心脏扩大;③促进心肌细胞肥厚及成纤维细胞增殖、分化,导致心室重构;④使组织抑制基质金属蛋白酶(tissue inhibitory MMPs,TIMPs)降低,激活基质金属蛋白酶(metalloproteinases,MMPs),降解细胞外蛋白,增加细胞基质沉积,导致梗死区延展,促进HF的进展[4]。(2)SNS激活使去甲肾上腺素分泌增多,使心肌细胞Ca2+内流增加,促进心肌细胞坏死、凋亡;同时去甲肾上腺素还可促使心肌细胞和成纤维细胞分泌转化生长因子β(transforming growth factor,TGF-β),从而诱导心肌细胞、成纤维细胞、血管平滑肌细胞的增生,促进心脏结构和功能的改变。同时在HF发生、发展的过程中,对抗RAAS和SNS的内分泌激素也被激活,即利钠肽系统(natriuretic peptide systems,NPs)[5]。它是心血管系统在容量或压力负荷过重时分泌的一类具有多种生物活性的肽类物质(包括ANP、BNP、CNP),除具有利尿、排钠、扩血管,减轻心脏前后负荷,改善血流动力学障碍外,还有抗炎、抗心肌肥厚及纤维化,是HF的一种代偿性保护因子。但HF时NPs分泌相对不足,难以对抗RAAS过度激活对心肌造成损伤。因此,除阻断RAAS和SNS外,增加NPs的浓度,改善循环血液中神经内分泌激素的不平衡状态,可能是延缓心肌梗死后HF发生、发展的关键措施。
实践证明,ACEI/ARB、β受体阻断剂及醛固酮拮抗剂是目前HF治疗的“金三角”。然而,即使是最佳的药物治疗,心肌梗死后HF患者的死亡风险仍然很高,5年的死亡风险与恶性肿瘤相似。然而,近期PARADIGM-HF研究打破了HF治疗的现状。该研究显示,与ACEI相比,ARNI使慢性HFrEF患者的心血管死亡及HF再住院风险降低20%[1],明显降低了心肌梗死后HF的预后[6]。我中心临床试验发现,rhBNP可预防急性前壁STEMI冠状动脉微循环障碍,改善梗死区域心肌血流灌注,缩小HF面积,预防心室重塑,改善预后。鉴于,Sac/Val既有增加NPs的浓度,又可抑制RAAS的双重作用。预测Sac/Val可抑制急性前壁STEMI于PCI术后合并HFrEF患者心室重构,改善左心功能,且疗效可能更佳。
本研究采用NT-proBNP及超声参数变化对急性前壁STEMI于PCI术后合并HFrEF患者的心功能进行评估。治疗6个月2组的NT-proBNP、LVEF、WMSI均明显改善。随访期间2组患者均未出现高血钾、肾功能恶化、血管性水肿等严重不良反应。且2组均未发生死亡事件,但观察组心肌梗死后HF的再住院率低,这与PARADIGM-HF研究结果相一致。Park等[7]曾对669例急性STEMI患者平均观察1年,发现RAAS抑制剂可以明显缩小LVESV、LVEDV,提高LVEF,降低MACE。动物实验显示,与ACEI相比,Sac/Val使急性心肌梗死后1周大鼠的LVEF及收缩末压力-容积明显改善[8]。近期临床研究显示,Sac/Val可使HFrEF患者的LVEF增加,缩小LVESV及LVEDV,抑制左心室不良重构[9-11]。然而,本研究结果显示,与对照组相比,治疗后观察组LVEF及LVESV改善更明显,但并未发现Sac/Val对LVEDV明显改善。考虑可能原因:①近期临床报道为自身对照研究,而本研究设计Val为对照。②本研究随访时间短,未能观察到LVEDV明显改善。③本研究对照组Val最大耐受剂量,与既往ARB/ACEI类固定剂量不同。
Sac/Val对心脏重构及心功能的影响机制:①升高循环中NPs水平,产生利钠、利尿,改善血流动力学障碍,降低心脏前后负荷,抑制室壁张力及早期梗死后心室扩张,降低心肌收缩的不协调性,降低心肌耗氧量,抑制心肌梗死后延展过程。②抑制AngⅡ引起的促心肌肥厚及纤维化的因子表达,如可溶性肿瘤抑制2[12]、基质金属蛋白酶9(matrix metalloproteinase-9,MMP-9)[13]、组织金色蛋白酶抑制剂1及Ⅰ型胶原蛋白的N端前肽[12]、内皮素[14]及TGF-β[14-15]等,且 Sac/Val在抑制心肌细胞肥厚、成纤维细胞增生及基质胶原蛋白合成方面具有协同作用。③NPs抑制SNS引起的去甲肾上腺素释放,抑制Ca2+内流[16],还可激活P53[17]及通过STAT3通路[18],抑制心肌细胞死亡。④NPs通过cGMP-PKG信号转导通路,激活内皮型一氧化氮合成酶活性,使一氧化氮合成增加,并提高NO的生物利用度[16],改善了慢性HF一氧化氮合成不足及生物利用障碍,诱导血管生成,具有[19-21]抗炎、抗氧化应激、抑制平滑肌细胞肥厚,改善血管内皮功能障碍,扩张冠状动脉血管,改善心肌微循环功能障碍。
本研究结果显示,急性前壁STEMI于PCI术后合并HFrEF的患者,应用Sac/Val后患者血浆NT-proBNP短期内迅速降低,并维持在较低水平。随访结束时LVEF、WMSI、LVESV明显改善,且优于单用Val。反应了Sac/Val较ARB可进一步抑制心室重构,改善左心功能,降低心肌梗死后的MACE。
本研究为单中心、纳入样本量少,且随访时间相对较短,因此,Sac/Val对急性前壁STEMI且在PCI术后合并HFrEF患者心功能影响的深层机制、安全性及远期疗效,有待于大规模、多中心研究进一步评估。
Sac/Val可以改善急性前壁STEMI于PCI术后合并HFrEF患者的室壁运动障碍,提高左心功能,降低6个月内的MACE。
[1] 崔晓通,周京敏,葛均波. PARADIGM-HF研究结果解读[J]. 中国循环杂志,2018,33(2):203-205.
[2] Miao ZL,Hou AJ,Zang HY,et al. Effects of recombinant human brain natriuretic peptide on the prognosis of patients with acute anterior myocardial infarction undergoing primary percutaneous coronary intervention:a prospective,multi-center,randomized clinical trial[J]. J Thorac Dis,2017,9(1):54-63.
[3] Qureshi WT,Zhang ZM,Chang PP,et al. Silent myocardial infarction and long-term risk of heart failure:the ARIC study[J]. J Am Coll Cardiol,2018,71(1):1-8.
[4] Curley D,Lavin Plaza B,Shah AM,et al. Molecular imaging of cardiac remodelling after myocardial infarction[J]. Basic Res Cardiol,2018,113(2):10.
[5] 葛南南. 脑啡肽酶抑制剂在心血管疾病中的最新研究进展[J]. 河北医科大学学报,2018,39(2):236-240.
[6] Mogensen UM,Køber L,Kristensen SL,et al. The effects of sacubitril/valsartan on coronary outcomes in PARADIGM-HF[J]. Am Heart J,2017,188:35-41.
[7] Park H,Kim HK,Jeong MH,et al. Clinical impacts of inhibition of renin-angiotensin system in patients with acute ST-segment elevation myocardial infarction who underwent successful late percutaneous coronary intervention[J]. J Cardiol,2017,69(1):216-221.
[8] Kompa AR,Lu J,Weller TJ,et al. Angiotensin receptor neprilysin inhibition provides superior cardioprotection compared to angiotensin converting enzyme inhibition after experimental myocardial infarction[J]. Int J Cardiol,2018,258:192-198.
[9] Martens P,Beli⊇n H,Dupont M,et al. The reverse remodeling response to sacubitril/valsartan therapy in heart failure with reduced ejection fraction[J]. Cardiovasc Ther,2018,36(4):e12435.
[10] Cosentino ER,Degli Esposti D,Miceli R,et al. Sacubitril/valsartan improves both functional and echocardiographic parameters in patients with chronic heart failure with reduced ejection fraction[J]. Curr Med Res Opin,2019,35(Supp1):9-12.
[11] Almufleh A,Marbach J,Chih S,et al. Ejection fraction improvement and reverse remodeling achieved with Sacubitril/Valsartan in heart failure with reduced ejection fraction patients[J]. Am J Cardiovasc Dis,2017,7(6):108-113.
[12] Zile MR,O'Meara E,Claggett B,et al. Effects of sacubitril/valsartan on biomarkers of extracellular matrix regulation in patients with HFrEF[J]. J Am Coll Cardiol,2019,73(7):795-806.
[13] Ishii M,Kaikita K,Sato K,et al. Cardioprotective effects of LCZ696 (Sacubitril/Valsartan) after experimental acute myocardial infarction[J]. JACC Basic Transl Sci,2017,2(6):655-668.
[14] Oatmen KE,Zile MR,Burnett JC Jr,et al. Bioactive signaling in next-generation pharmacotherapies for heart failure:a review[J]. JAMA Cardiol,2018,3(12):1232-1243.
[15] Suematsu Y,Miura S,Goto M,et al. LCZ696,an angiotensin receptor-neprilysin inhibitor,improves cardiac function with the attenuation of fibrosis in heart failure with reduced ejection fraction in streptozotocin-induced diabetic mice[J]. Eur J Heart Fail,2016,18(4):386-393.
[16] Fu S,Ping P,Wang F,et al. Synthesis,secretion,function,metabolism and application of natriuretic peptides in heart failure[J]. J Biol Eng,2018,12:2.
[17] Iborra-Egea O,G lvez-Montón C,Roura S,et al. Mechanisms of action of sacubitril/valsartan on cardiac remodeling:a systems biology approach[J]. NPJ Syst Biol Appl,2017,3:12.
lvez-Montón C,Roura S,et al. Mechanisms of action of sacubitril/valsartan on cardiac remodeling:a systems biology approach[J]. NPJ Syst Biol Appl,2017,3:12.
[19] 陈莉,逯伟达,吴媛媛,等. 沙库巴曲缬沙坦对射血分数降低的心力衰竭Ⅳ级患者生化指标和左心室结构的干预作用[J]. 中华老年医学杂志,2019,38(5):525-528.
[21] Suematsu Y,Jing W,Nunes A,et al. LCZ696 (Sacubitril/Valsartan),an angiotensin-receptor neprilysin inhibitor,attenuates cardiac hypertrophy,fibrosis,and vasculopathy in a rat model of chronic kidney disease[J]. J Card Fail,2018,24(4):266-275.