ST段抬高型心肌梗死(ST-segment elevation myocardial infarction,STEMI)是一种致残率、致死率都很高的心血管急症,该病的发生和预后是临床心脏病学领域所面临的重要挑战之一。对于急性STEMI患者,及时的经皮冠状动脉介入术(percutaneous coronary intervention,PCI)开通梗死相关动脉(infarction related artery,IRA)和有效抗血小板仍然是目前最有效的治疗措施。然而,尽管直接经皮冠状动脉介入术(primary percutaneous coronary intervention,pPCI)成功开通了IRA,使得心肌梗死溶栓试验(thrombolysis in myocardial infarction,TIMI)血流3级,仍有部分患者出现心肌灌注不良,表现为心脏扩大、心功能不全等。据报道,急性STEMI患者在成功pPCI术后,仍有50%出现心肌灌注不良[1]。这些心肌灌注不良与已知的左心室功能受损和预后不良密切相关。前列地尔因其具有血管舒张、抑制血小板聚集、改善微循环等生物学功能而被广泛应用于临床。依替巴肽为血小板GPⅡb/Ⅲa受体拮抗剂,冠状动脉内应用可增加冠状动脉血流速度,改善心肌灌注[2]。但两药联合应用对急性STEMI患者pPCI术后心肌灌注疗效是否更佳,目前相关研究甚少。本研究观察冠状动脉内靶向给予依替巴肽联合术前应用前列地尔对急性STEMI患者pPCI术后心肌灌注的影响,探讨联合用药对心肌微循环的作用。
1 资料与方法
1.1 一般资料 选取2017年12月—2018年11月河北省邯郸市中心医院收治的急性STEMI患者162例。按随机数字表法分为观察组和对照组各81例。观察组男性56例,女性25例,年龄36~72岁,平均(61.2±7.1)岁,平均体重指数28.57±6.37;合并高血压53例,糖尿病33例,血脂异常48例,吸烟40例;对照组男性58例,女性23例,年龄39~75岁,平均(60.0±10.8)岁,平均体重指数26.75±7.64,合并高血压46例,糖尿病27例,血脂异常39例,吸烟45例。2组患者在性别、年龄及病史等方面差异均无统计学意义(P>0.05),具有可比性。
本研究通过医院伦理委员会批准,所有患者签署知情同意书。
1.2 入选标准和排除标准 入选标准:①符合美国心脏协会/美国心脏病学会(American Heart Association/American College of Cardiology,AHA/ACC)的STEMI诊断标准;②发病在12 h内且有pPCI指证;③同意接受前列地尔和依替巴肽治疗。排除标准:①既往出血脑卒中史及3个月内缺血脑卒中;②已知脑血管结构异常;③严重肝肾功能异常及恶性肿瘤等;④确诊或怀疑主动脉夹层;⑤目前活动性消化道溃疡;⑥有创伤性心肺复苏(创伤性心肺复苏≥10 min),2周内不能实施压迫穿刺处大出血;⑦心源性休克;⑧有依替巴肽、前列地尔过敏者;⑨造影提示左主干病变;⑩陈旧性心肌梗死。
1.3 研究方法 2组患者术前均接受负荷量双联抗血小板治疗。所有患者均采取经桡动脉路径,静脉注射普通肝素[3][观察组50~70 U/kg,维持活化的凝血时间(activated coagulation time,ACT)200~250 s,对照组70~100 U/kg,维持ACT 250~300 s,手术每延长1 h,追加肝素1 000 U]。观察组应用血栓抽吸导管冠状动脉内给予依替巴肽180 μg/kg,3 min内给完,10 min后再次给予依替巴肽(方式同前),之后静脉滴注依替巴肽2 μg·kg-1·min-1,持续18 h。对照组通过血栓抽吸导管冠状动脉内靶向注入相同剂量的生理盐水(方法与观察组相似)。所有入组患者均于术前30 min接受前列地尔 10 μg+10 mL 0.9%氯化钠静脉注射,术后持续应用7 d。所有患者均行pPCI治疗,术中是否行血栓抽吸由术者决定。所用支架均为第2代药物洗脱支架。术后规范抗血小板、降脂、血管紧张素转化酶抑制剂或血管紧张素受体抑制剂等治疗。入院后行心电图、心肌声学造影、实验室检查。于术后4,8,16,24,36 h抽血检测肌酸激酶同工酶(creatine kinase isoenzyme-MB,CK-MB) 和肌钙蛋白I(cardiac troponin-I,cTnI),并记录两者峰值。术后48 h,1周查心肌声学造影。
1.4 观察指标及意义 观察靶血管TIMI血流分级及校正TIMI帧幅数 (corrected TIMI frame count,cTFC),心电图STR情况,术前及术后1周室壁运动积分指数(wall motion score index,WMSI)及左心室射血分数(left ventricular ejection fraction,LVEF),2组患者心肌损伤标志物及心肌声学造影变化。
1.4.1 梗死相关动脉血流评估 TIMI 3级定义为心外膜血流完全灌注,TIMI分级<3级,定义为无复流(no reflow,NR)[4]。
1.4.2 心肌灌注评估 心电图STR≥70%定义为完全心肌灌注。cTFC计算标准参照Gibsonti提出的方法,cTFC≥27反映心肌慢血流[5]。
1.4.3 心肌声学造影 术后48 h及术后1周进行心肌声学造影,利用软件自动成数据[y=A(1-e-βt)],A为最大超声学强度,β代表血流速度,e为常量(软件自带的),t为时间,Aβ为局部心肌血流灌注。
1.5 统计学方法 应用SPSS 25.0统计软件处理数据。正态分布计量资料比较采用t检验;非正态分布计量资料采用Mann-Whitney U检验。计数资料比较采用χ2检验或Fisher确切概率法。P<0.05为差异有统计学意义。
2 结 果
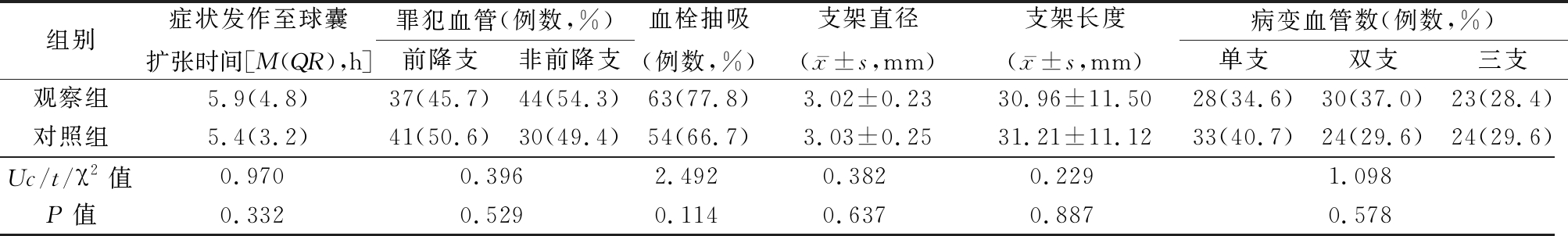
2.1 一般造影资料比较 2组患者在症状发作至球囊扩张时间、犯罪血管分布、血栓抽吸情况、支架直径和长度、病变血管数等方面差异均无统计学意义(P>0.05),见表1。
表1 2组一般造影资料比较
Table 1 Comparisons of general imaging data between two groups (n=81)
组别症状发作至球囊扩张时间[M(QR),h]罪犯血管(例数,%)前降支非前降支血栓抽吸(例数,%)支架直径(x-±s,mm)支架长度(x-±s,mm)病变血管数(例数,%)单支双支三支观察组5.9(4.8)37(45.7)44(54.3)63(77.8)3.02±0.2330.96±11.5028(34.6)30(37.0)23(28.4)对照组5.4(3.2)41(50.6)30(49.4)54(66.7)3.03±0.2531.21±11.1233(40.7)24(29.6)24(29.6)Uc/t/χ2值0.9700.3962.4920.3820.2291.098P值0.3320.5290.1140.6370.8870.578
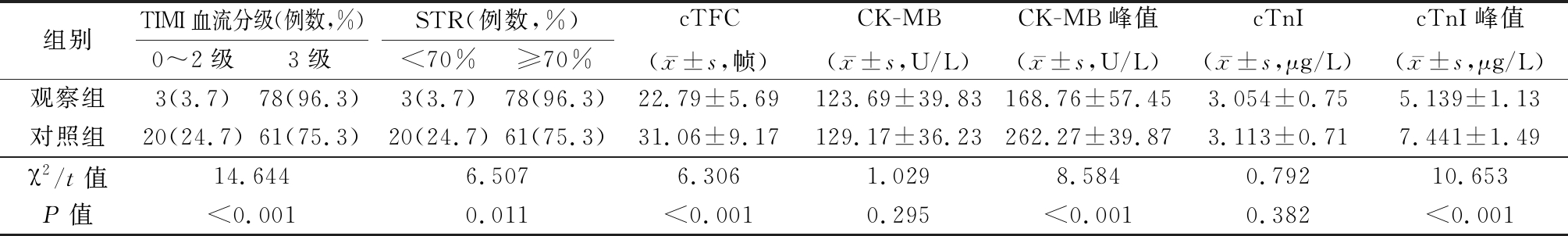
2.2 TIMI分级、心电图STR及心肌损伤标志物等比较 术前2组患者CK-MB及cTnI比较无统计学意义(P>0.05)。观察组TIMI血流3级及STR≥70%发生率高于对照组(P<0.05),而CK-MB峰值、cTnI峰值及cTFC较低(P<0.05)。2组均未发生心肌内出血。见表2。
表2 2组TIMI血流分级、cTFC、STR、心肌内出血及心肌损伤标志物比较
Table 2 Comparisons of TIMI,cFTC,STR,intramuscular hemorrhage and marks of myocardial necrosis between two groups (n=81)
组别TIMI血流分级(例数,%)0~2级3级STR(例数,%)<70%≥70%cTFC(x-±s,帧)CK-MB(x-±s,U/L)CK-MB峰值(x-±s,U/L)cTnI(x-±s,μg/L)cTnI峰值(x-±s,μg/L)观察组3(3.7)78(96.3)3(3.7)78(96.3)22.79±5.69123.69±39.83168.76±57.453.054±0.755.139±1.13对照组20(24.7)61(75.3)20(24.7)61(75.3)31.06±9.17129.17±36.23262.27±39.873.113±0.717.441±1.49χ2/t值14.6446.5076.3061.0298.5840.79210.653P值<0.0010.011<0.0010.295<0.0010.382<0.001
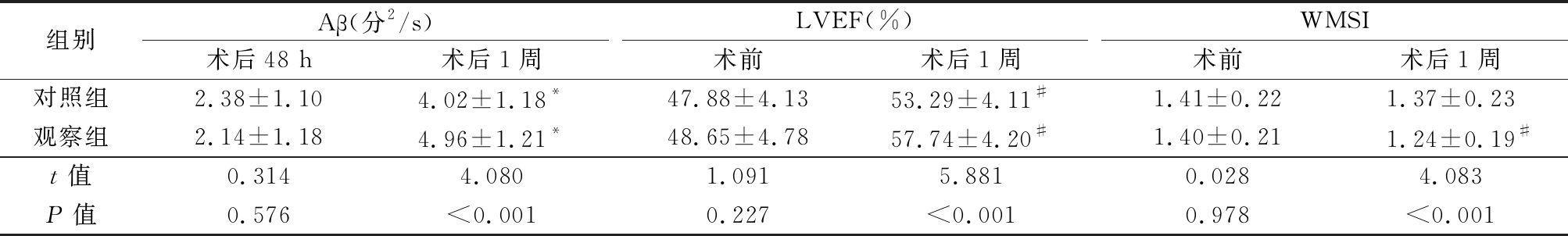
2.3 2组心肌声学造影比较 术后48 h 2组Aβ比较无统计学意义(P>0.05),术前2组LVEF及WMSI比较无统计学意义(P>0.05)。与自身比较,术后1周观察组LVEF,WMSI及Aβ较前明显改善(P<0.05)。对照组与自身比较,Aβ及LVEF较前改善(P<0.05)。术后1周观察组Aβ,LVEF明显高于对照组(P<0.05),WMSI明显低于对照组,差异有统计学意义(P<0.05)。见表3。
表3 2组心肌声学造影参数比较
Table 3 Comparisons of myocardial contrast echocardigraphy parameters between two groups![]()
组别Aβ(分2/s)术后48 h术后1周LVEF(%)术前术后1周WMSI术前术后1周对照组2.38±1.104.02±1.18*47.88±4.1353.29±4.11#1.41±0.221.37±0.23观察组2.14±1.184.96±1.21*48.65±4.7857.74±4.20#1.40±0.211.24±0.19#t值0.3144.0801.0915.8810.0284.083P值0.576<0.0010.227<0.0010.978<0.001
*P值<0.05 与术后48 h比较 #P值<0.05与术前比较(配对t检验)
3 讨 论
NR与心肌微循环障碍密切相关,且在不同临床条件下发生率不同。常规PCI术后NR发生率<2%,急性心肌梗死患者pPCI后发生率更高。而心肌灌注不良与已知的左心室功能受损和预后不良密切相关。因此,首次IRA再灌注后(通过溶栓或PCI)实现心肌再灌注至关重要。改善心肌微循环灌注,预防NR是目前研究的热点。然而引起NR的确切机制不明,考虑可能与微循环栓塞、炎症-血小板机制、缺血/再灌注相关损伤(ischemia/reperfusion injury,IRI) 等相关[6],而微循环阻塞和IRI被认为与NR最为相关。
及时PCI开通IRA是减轻缺血性损伤的有效手段,但再灌注本身也会触发、加重心肌细胞损伤。对于急性STEMI患者,在pPCI过程中由于球囊扩张和支架植入可造成斑块破裂、血栓栓子脱落,直接导致微循环阻塞[7];而微循环阻塞又可导致组织缺氧、血管内皮受损、血小板激活,促进血栓形成,加重微循环障碍;此过程中活化的血小板释放血管活性因子和趋化介质,促进中性粒细胞黏附、聚集,参与炎症反应,加重微循环损坏;另外,再灌注本身亦可引起心肌细胞损伤,如氧自由基释放、细胞内钙超载、促发炎症反应,导致细胞损伤和死亡,从而加重微循环障碍,促进NR发生[8]。
众所周知,血小板在致动脉粥样硬化病变的血栓形成(再)闭塞、支架血栓形成和微循环血流减少中起着重要作用[9],是IRA开通后再闭塞和最终临床结果的一个促进因素。因此,急性心肌梗死后强化抗血小板是缩小梗死面积、预防NR、改善预后的主要治疗方法。冠状动脉应用替罗非班可预防STEMI患者PCI时的NR,明显改善患者的心肌灌注及心功能[10-11]。而针对微循环阻塞及再灌注损伤,目前临床上应用最多的药物有腺苷[7]、硝普纳[7]、尼可地尔[11-12]。Meta分析发现,在冠状动脉内给药治疗NR时,无论是何种类型的药物(扩血管和抗血小板),均可有效地改善心肌灌注[13]。国外研究推荐把GPⅡb/Ⅲa阻断剂作为NR的预防用药[14]。然而,有研究对上述药物持不同观点,认为GPⅡb/Ⅲa阻断剂与心肌内出血的风险增加相关,可能对降低NR不利[15]。因此,更好地了解不同条件下,pPCI术后导致心肌灌注不良的机制,是制定有效干预措施,预防心肌梗死后NR的必要条件。然而,由于对pPCI术后冠状动脉微循环损伤的确切病理机制所知甚少,因此对其危险预测及干预推荐可能不够成熟和有限。鉴于NR常发生于血栓负荷重的一些患者,结合pPCI过程中所致IRI及血小板激活。因此,对于急性STEMI在再灌注前或灌注后立即进行强化抗血小板治疗和微循环保护可能对改善NR有效。
依替巴肽是一种环肽类GPⅡb/Ⅲ阻断剂,目前国内对该药的研究相对较少,对国人来说可作为一种新的抗血小板药物。张海良等[2]对56例急性心肌梗死患者行急诊PCI时,冠状动脉内应用依替巴肽能有效改善患者的心功能,提高冠状动脉血流速度、增加心肌灌注。前列地尔是一种生理活性物质,具有扩张血管,抑制炎症反应,改善血管内皮功能。Meta分析发现,前列地尔可能对再灌注损伤有一定的治疗作用[16]。鉴于NR是一个多因素参与的病理过程,最终导致微循环阻塞和IRI[17]。基于此种理念,本研究采取对急性STEMI的患者在行PCI时,局部靶血管注射依替巴肽联合静脉应用作用机制不同的前列地尔,观察心肌灌注情况。本研究结果显示,2组患者均未发生心肌内出血事件。与对照组相比,观察组TIMI血流3级率高,Aβ增高,心电图STR≥70%高,CK-MB峰值、cTnI峰值水平低,WMSI低,cTFC少。因TIMI分级反映的是心外膜血流灌注情况,cTFC反映造影当时心肌灌注情况(cTFC多提示心肌灌注不良),而Aβ反映心肌灌注情况,可判断存活心肌及再灌注治疗的效果[18]。观察组TIMI血流3级率高,提示IRA血流速度快、灌注好;与对照组比较,观察组心电图STR完全回落率及Aβ高,cTFC少,反映心肌微循环灌注好。观察组CK-MB峰值、cTnI峰值及WMSI低,LVEF高,这些指标反映了观察组较对照组心肌坏死面积小,心功能好。提示依替巴肽联合前列地尔不仅提高心肌的血流灌注,降低NR,且对缺血区存活心肌具有保护作用。这与国外报道不相符,GPⅡb/Ⅲa受体阻断剂增加心肌内出血的风险[15]。分析原因可能有:①与本研究提前应用前列地尔有关(心肌内出血可能与多种因素相关,如炎症反应、氧化应激、内皮损伤、组织水肿等),前列地尔具有多种生理活性,抑制血栓素A2的合成、抗炎[19],抑制氧化应激反应,保护血管内皮细胞,改善心肌微循环[20]。荟萃分析结果显示前列地尔具有白细胞介素6及白细胞介素8作用,抑制再灌注损伤[16],且在血管内皮受损或痉挛处浓度更高,因此在血管受损处可有效发挥微循环保护作用。②与心肌缺血再灌注时机相关,实施再灌注时间短。③依替巴肽相对安全。④本研究例数较少,存在偶然性。另外,本研究采取对GPⅡb/Ⅲa受体阻断剂冠状动脉内给药的方式,具有优点,避免肝脏的首过效应,直接在病变部位形成比较稳定的高剂量血药浓度,与血小板充分结合,抑制血小板激活及炎性因子释放,预防PCI过程中微血栓形成,降低NR。
综上所述,冠状动脉给予依替巴肽联合静脉应用前列地尔可改善心肌灌注,降低NR,改善心功能。研究局限性为单中心、小样本研究,且观察时间较短。期待今后扩大样本量,进一步研究。
[1] Durante A,Camici PG. Novel insights into an “old” phenomenon:the no reflow[J]. Int J Cardiol,2015,187:273-280.
[2] 张海良,王西辉,贺鹏辉,等.冠状动脉内应用依替巴肽在急性心肌梗死患者急诊PCI中的效果观察[J].广西医科大学学报,2017,34(8):1216-1218.
[3] 中华医学会心血管病学分会,中华心血管病杂志编辑委员会.急性ST段抬高型心肌梗死诊断和治疗指南[J].中华心血管病杂志,2015,43(5):380-393.
[4] Avci E,Yildirim T,Aydin G,et al. Combining clinical predictors to better predict for the no-reflow phenomenon[J]. Eur Rev Med Pharmacol Sci,2018,22(15):4987-4994.
[5] Gibson CM,Cannon CP,Daley WL,et al. TIMI frame count:a quantitative method of assessing coronary artery flow[J]. Circulation,1996,93(5):879-888.
[6] 杨波,杨树森.血栓抽吸与替罗非班在急诊冠状动脉介入慢血流/无复流中的作用[J].中国循证心血管医学杂志,2017,9(11):1406-1408.
[7] Rezkalla SH,Stankowski RV,Hanna J,et al. Management of no-reflow phenomenon in the catheterization laboratory[J]. JACC Cardiovasc Interv,2017,10(3):215-223.
[8] Zhu H,Sun A. Programmed necrosis in heart disease:Molecular mechanisms and clinical implications[J]. J Mol Cell Cardiol,2018,116:125-134.
[9] Allencherril J,Alam M,Levine G,et al. Do we need potent intravenous antiplatelet inhibition at the time of reperfusion during ST-segment elevation myocardial infarction[J]. J Cardiovasc Pharmacol Ther,2019,24(3):215-224.
[10] 李亚,刘永兴,彭万忠,等.微导管注射替罗非班联合不同血管扩张剂对直接介入治疗中无复流的疗效比较[J].岭南心血管病杂志,2017,23(1):31-35.
[11] 齐琪,牛竞辉,陈涛,等.尼可地尔联合替罗非班对急性ST段抬高型心肌梗死患者PPCI无复流的疗效观察[J].河北医科大学学报,2017,38(7):750-755.
[12] 冯春光,韩冰,刘奕,等.早期冠状动脉内应用尼可地尔对急性前壁心肌梗死患者再灌注无复流和左心室重构的影响[J/CD].中华临床医师杂志(电子版),2017,11(1):6-11.
[13] 曹野,邹远林,王伟琼,等.冠状动脉内微导管给药治疗无复流现象疗效的Meta分析[J].中国介入心脏病学杂志,2018,26(3):159-166.
[14] Kingma JG. Effect of platelet GPIIb/IIIa receptor blockade with MK383 on infarct size and myocardial blood flow in a canine reocclusion model[J]. J Cardiovasc Pharmacol Ther,2018[Epub ahead of print].
[15] Amier RP,Tijssen R,Teunissen P,et al. Predictors of intramyocardial hemorrhage after reperfused ST-segment elevation myocardial infarction[J]. J Am Heart Assoc,2017,6(8).pii:e005651.
[16] Zhu H,Xu X,Ding Y,et al. Effects of prostaglandin E1 on reperfusion injury patients:A meta-analysis of randomized controlled trials[J]. Medicine(Baltimore),2017,96(15):e6591.
[17] Davidson SM,Ferdinandy P,Andreadou I,et al. Multitarget strategies to reduce myocardial ischemia/reperfusion injury:JACC review topic of the week[J]. J Am Coll Cardiol,2019,73(1):89-99.
[18] 王珊珊,韩薇.心肌超声造影在冠状动脉血运重建术中的应用[J].心血管病学进展,2018,39(5):806-809.
[19] 黄朝莉,谷粒,宁成.前列地尔联合左卡尼汀对维持性血液透析患者微炎症及营养状态的影响[J].昆明医科大学学报,2017,38(3):87-89.
[20] Zhu H,Ding Y,Xu X,et al. Prostaglandin E1 protects coronary microvascular function via the glycogen synthase kinase 3β-mitochondrial permeability transition pore pathway in rat hearts subjected to sodium laurate-induced coronary microembolization[J]. Am J Transl Res,2017,9(5):2520-2534.