胃镜检查时偶尔会发现胃白色多发扁平隆起病变(multiple white and flat elevated lesions,MWFLs),有些基层医院内镜医师会将其诊断为肠上皮化生,将此类患者划分为胃癌高危人群。然而MWFLs是否为肠上皮化生,经过查阅文献并未见相关报道。MWFLs内镜下特征性表现为大小各异的多发白色扁平隆起,隆起表面无类似胃底腺息肉的扩张血管结构,抵近观察可见管状微结构,组织学上为胃底腺小凹上皮的增生性变化[1]。Uedo等[2]研究发现,这些病变不是萎缩或者肠上皮化生。本研究拟分析并总结MWFLs临床病理和内镜特征及其危险因素。
1 资料与方法
1.1 一般资料 选取2017年1—12月来我院内镜中心行胃镜检查的邢台市本地患者926例,男性552例,女性374例,年龄45~81岁,平均(55.2±8.6)岁。均否认特殊食物接触史及家族史、遗传史,且既往未行胃镜检查。排除标准:①未行幽门螺杆菌检测,幽门螺杆菌感染状态不明确;②食管或胃切除术后;③上消化道狭窄无法观察胃底及胃体情况。
1.2 筛查流程 内镜型号:Olympus GIF- H260Z,H290。内镜系统:EVIS LUCERA SPECTRUM(Olympus)。操作医师具有5年以上连续内镜操作的经验,>5 000例胃镜操作次数。MWFLs判定标准:MWFLs常分布于胃底、胃体上部,偶尔位于胃体中部,具有管状或圆形的表面结构,具有清晰的边界(图1)。对于微小病变使用内镜窄带成像技术(narrow band imaging,NBI)及放大NBI协助诊断(图2~4)。由于MWFls常被忽视或遗漏,常规使用NBI及放大NBI观察胃底及胃体上部。发现胃底或胃体存在MWFLs后对其进行活组织检查和病理组织学检查,对胃窦进行活组织检查,判断胃黏膜有无萎缩,同时进行快速尿素酶试验测定,判断幽门螺杆菌感染状态。详细询问并记录每例患者的个人史、家族史、烟酒嗜好、用药史情况等。
1.3 统计学方法 应用SPSS 19.0统计软件分析数据。正态分布的计量资料比较采用t检验,非正态分布的计量资料比较采用秩和检验,计数资料比较采用χ2检验。采用Logistic回归分析确定MWFLs的危险因素。P<0.05为差异有统计学意义。
2 结 果
2.1 MWFLs检出情况 926例受试者中诊断MWFLs75例,检出率为8.1%(75/926)。MWFLs阳性组女性占比和服用质子泵抑制剂(proton pump inhibitors,PPIs)占比高于MWFLs阴性组,年龄大于MWFLs阴性组,差异有统计学意义(P<0.05),2组幽门螺杆菌阳性、胃黏膜萎缩、PPIs使用时间差异无统计学意义(P>0.05)。见表1。75例MWFLs患者病理结果均为黏膜慢性炎及胃底腺小凹上皮增生性变化,未见肠上皮化生及萎缩改变(图5)。
表1 MWFLs阳性组与MWFLs阴性组临床特征比较
Table 1 Comparison of clinical features between patientss with and without MWFLs (例数,%)
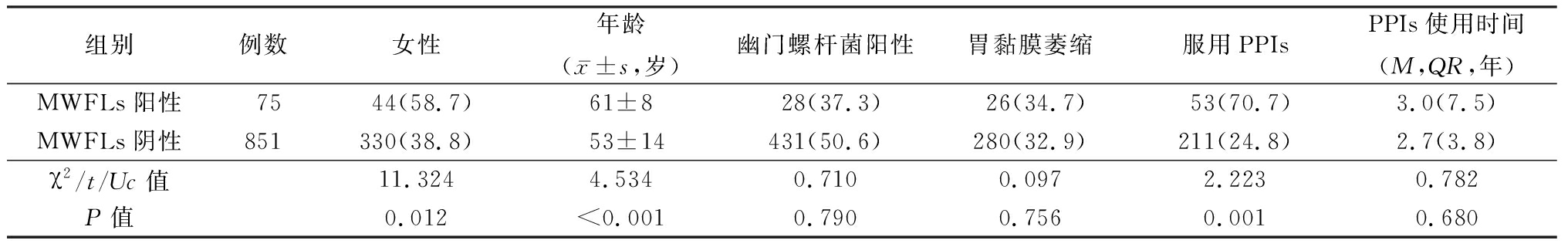
组别例数女性年龄(x-±s,岁)幽门螺杆菌阳性胃黏膜萎缩服用PPIsPPIs使用时间(M,QR,年)MWFLs阳性7544(58.7)61±828(37.3)26(34.7)53(70.7)3.0(7.5)MWFLs阴性851330(38.8)53±14431(50.6)280(32.9)211(24.8)2.7(3.8)χ2/t/Uc值11.3244.5340.7100.0972.2230.782P值0.012<0.0010.7900.7560.0010.680
2.2 Logisitic回归分析 以MWFLs为因变量,以性别、年龄、服用PPIs为自变量,进行Logisitic回归分析,结果显示,女性(OR=2.112,95%CI:1.180~3.762),年龄(>55岁)(OR=2.541,95%CI:1.400~4.611)、服用PPIs(OR=1.951,95%CI:1.052~3.613)是MWFLs的危险因素。见表2,3。
表2 变量赋值表
Table 2 Variable assignment table

变量类别变量名变量赋值自变量性别男性=0,女性=1年龄<55岁=0;≥55岁=1PPIs未服用=0,服用=1因变量MWFLs阴性=0,阳性=1
表3 Logistic回归分析MWFLs的危险因素
Table 3 Risk factors for MWFLs identified by Logistic regression analysis
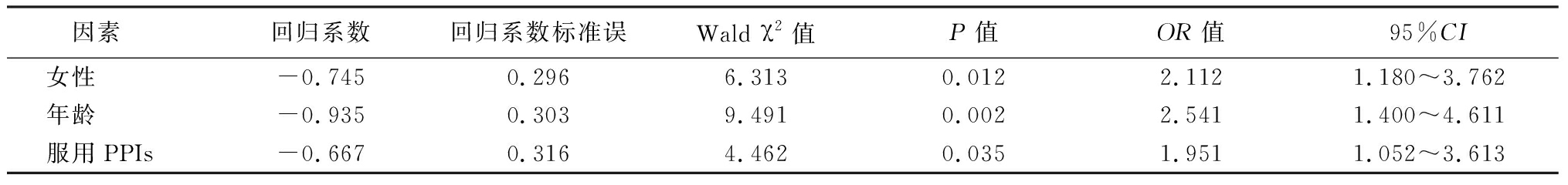
因素 回归系数回归系数标准误Wald χ2值P值OR值95%CI女性 -0.745 0.2966.3130.0122.1121.180~3.762年龄 -0.935 0.3039.4910.0022.5411.400~4.611服用PPIs-0.667 0.3164.4620.0351.9511.052~3.613
2.3 随访 对MWFLs阳性患者随访1年,在第1次进行胃镜检查时未服用PPIs 22例,其中在随访期间未使用PPIs 19例,7例复查胃镜时MWFLs无明显变化;其余3例因为烧心或胃部胀痛间断性服用PPIs,复查胃镜发现,MWFLs轻微增大,数量无明显变化。在首次胃镜检查前已服用PPIs的MWFLs患者53例,随访18例均未停PPIs,复查胃镜未发现MWFLs有进展性变化。
3 讨 论
本研究结果显示,女性、老年、长期服用PPIs是MWFLs的危险因素。70.7%(53/75)MWFLs患者服用PPIs。Kiso等[3]报道的数据为24.4%,可能与不同国家、地区的PPIs使用情况不同有关。本研究中女性与男性比值为44∶31,与Majima等[4]报道的43∶37相似。MWFLs阳性组年龄大于MWFLs阴性组,与Majima等[4]报道的结果一致。而2组幽门螺杆菌感染情况及胃黏膜萎缩状态差异无统计学意义。
本研究结果表明,MWFLs检出率为8.1%(75/926),低于Majima等[4]报道的10.4%,高于Adachi等[5]报道的3.0%。导致此病变检出率差异的原因,可能是人口学特征、临床资料及研究方法的差异,本研究具有目的性,在胃镜检查中注重观察胃底及胃体上部是否存在MWFLs,并且应用NBI及放大NBI技术,使得微小MWFLs被发现,所以病变检出率较高。
尽管目前MWFLs的发病机制尚不明确,但是已有“高胃泌素学说”。有报道称32%MWFLs患者具有高胃泌素表现[3]。另外,在接受PPIs治疗的患者中,胃泌素水平显著升高[5],可能是由于PPIs增加胃泌素水平[6],而胃泌素具有促进上皮黏膜细胞增生的功能[7],因此PPIs可能是通过提高胃泌素水平增加MWFLs的发生[4]。胃泌素水平随着年龄增长而增加,MWFLs检出率也随着年龄的增长而增加。已知女性胃泌素水平低于男性,所以,除了胃泌素水平肯定还有其他因素导致女性MWFLs发生率升高[8],因此MWFLs的形成原因有待于进一步研究。Adachi等[8]认为MWFLs主要发生于幽门螺杆菌根除后的患者。本研究结果显示,MWFLs阳性组和MWFLs阴性组幽门螺杆菌感染状态差异无统计学意义,与Adachi等[8]的研究结果不同。
另外,胃黏膜萎缩的判断取决于胃窦活组织检查病理。由于胃镜诊断萎缩性胃炎的准确率低于病理诊断,因此对每例MWFLs病灶进行活组织检查,发现病理结果均为黏膜慢性炎症,伴胃底腺小凹上皮增生,75例病灶的病理组织学均未见肠上皮化生或胃黏膜萎缩,这与Uedo等[2]的结论一致。在中国,胃癌的早期筛查面临着重大挑战,每年约679 100例新发现胃癌患者,胃癌居中国癌症死亡原因的第2位,因为80%胃癌患者被诊断时已进入进展期,所以5年生存率极低[9],除此之外,在其他东南亚国家如日本和韩国,胃癌的发生率也比较高,但相比于中国,韩国和日本政府对于胃癌的早期筛查投入较多,胃镜及其他检查的普及,导致韩国及日本早期胃癌检出率为50%以上,而胃癌的5年生存率在日本和韩国分别为64.6%和71.5%[10]。我国早期胃癌检出率仅为19%[11],提高我国的早期胃癌检出率尤为重要。我国40岁以上成年人的胃癌风险逐渐增加,人口众多,大量筛查会增加胃镜医师的工作量,增加医疗费用,因此需要区分胃癌的高危因素。众所周知,胃癌的高危因素有高龄、幽门螺杆菌感染、萎缩性胃炎、肠上皮化生[12]等。存在肠上皮化生的患者相比于没有肠上皮化生的患者胃癌风险上升7.6倍。传统白光胃镜下肠上皮化生常常表现为胃窦部MWFLs,结节样粗糙,但是有的肠上皮化生病变在传统白光胃镜下难以明确诊断,而运用NBI及放大NBI技术可以显著提高肠上皮化生的内镜诊断率,在NBI下肠上皮化生可见亮蓝脊和白色不透明物质[13]。本研究MWFLs与肠上皮化生有相似之处,都表现为胃部多发白色扁平隆起,但是后者主要位于胃窦、胃体部,白光难以鉴别二者。放大NBI技术可以观察胃黏膜表面的微血管及微结构,MWLFs没有亮蓝脊和白色不透明物质,其放大胃镜下可见规则增大、延长椭圆形微结构,病理显示为胃底腺小凹上皮增生性变化, MWFLs表现为一种
新型的增生性息肉[1]。
综上所述,女性、老年、长期服用PPIs是MWFLs的危险因素,内镜医师应该认识这些病变组织学上为胃底腺小凹上皮的增生性变化,为一种新型的增生性息肉,不要与萎缩和肠上皮化生混淆,避免将具有这些病变的人群划分为胃癌高危人群,避免过度活组织检查,减少不必要的医疗消耗。虽然PPIs是MWFLs的危险因素,但是根据幽门螺杆菌诊治相关指南[14],对于具有指征的患者,仍然建议根除幽门螺杆菌。(本文图见封三)
[1] Hasegawa R,Yao K,Ihara S,et al. Magnified endoscopic findings of multiple white flat lesions: a new subtype of gastric hyperplastic polyps in the stomach[J]. Clin Endosc,2018,51(6):558-562.
[2] Uedo N,Yamaoka R,Yao K. Multiple white flat lesions in the gastric corpus are not intestinal metaplasia[J]. Endoscopy,2017,49(6):615-616.
[3] Kiso M,Ito M, Boda T,et al. Endoscopic findings of the gastric mucosa during long-term use of proton pump inhibitor-a multicenter study[J]. Scand J Gastroenterol,2017,52(8):828-832.
[4] Majima K, Muraki Y,Shimamoto T. Multiple white and flat elevated lesions observed in the stomach: a prospective study of clinical characteristics and risk factors[J]. Intern Med, 2018,57(18):2613-2619.
[5] Shiotani A, Katsumata R, Gouda K,et al. Hypergastrinemia in long-term use of proton pump inhibitors[J]. Digestion,2018,97(2):154-162.
[6] Lundell L,Vieth M,Gibson F,et al. Systematic review: the effects of long-term proton pump inhibitor use on serum gastrin levels and gastric histology[J]. Aliment Pharmacol Ther,2015,42(6) 649-663.
[7] Shan JH,Bai XJ,Han LL,et al. Changes with aging in gastric biomarkers levels and in biochemical factors associated with Helicobacter pylori infection in asymptomatic Chinese population[J] . World J Gastroenterol,2017,23(32): 5945-5953.
[8] Adachi K,Mishiro T,Okada M,et al. Prevalence of multiple white and flat elevated lesions in individuals undergoing a medical checkup[J]. Intern Med,2018,57(9):1213-1218.
[9] Chen W,Zheng R,Baade PD,et al. Cancer statistics in China,2015[J]. CA Cancer J Clin,2016,66(2):115-132.
[10] Allemani C,Weir HK,Carreira H,et al. Global surveillance of cancer survival 1995-2009:analysis of individual data for 25676887patients from 279 population-based registries in 67 countries(CONCORD-2)[J]. Lancet,2015,385(9972):977-1010.
[11] 赵恩昊,赵刚,曹晖.中国、日本和韩国微创理念下的胃功能保留手术开展的现状与思考[J].中华胃肠外科杂志,2018,21(2):132-137.
[12] Shichijo S,Hirata Y,Niikura R,et al. Histologic intestinal metaplasia and endoscopic atrophy are predictors of gastric cancer development after Helicobacter pylori eradication[J]. Gastrointest Endosc,2016,84(4):618-624.
[13] Kanemitsu T,Yao K,Nagahama T,et al. Extending magnifying NBI diagnosis of intestinal metaplasia in the stomach: the white opaque substance marker[J]. Endoscopy,2017,49(6):529-535.
[14] 王春燕,李胜棉.2017幽门螺杆菌感染诊治相关国内外指南更新[J].河北医科大学学报,2019,40(2):125-128.