血管外科作为一个迅速发展的新兴学科,伴随着腔内器械不断更新及腔内技术的日益进步,疾病的治疗方式发生巨大变化,微创有效的腔内治疗已成为学科最主要的治疗手段之一。而腔内治疗必不可少的带来碘造影剂的大量使用;且随着腔内治疗在复杂病变及疾病的使用,造影剂的个人使用剂量明显增多,造影剂相关的肾功能损伤也引起更多重视。本中心近年在治疗中,腔内手术率达90%以上,现将腔内治疗且资料完善的患者临床数据收集分析如下。
1 资料与方法
1.1 一般资料 选择2017年1月—2018年10月广西医科大学第四附属医院柳州市工人医院血管外科行腔内治疗的患者279例,男性177例;年龄15~88岁,中位年龄63岁;平均体重58.9 kg;术前合并糖尿病32例,高血压94例,冠心病33例。静脉血栓性疾病(venous thromboembolism,VTE,包括深静脉血栓、肺动脉栓塞等)150例,主动脉疾病(aortic disease,AD,包括胸腹主动脉夹层/动脉瘤)67例,外周动脉疾病(peripheral artery disease,PAD,包括下肢动脉硬化闭塞症、急性下肢动脉栓塞等)35例,其他疾病(包括出血性疾病、肿瘤介入栓塞疾病等)27例。造影剂类型:非等渗造影剂158例(碘海醇50 mL:17.5 g,国药准字H10970327,扬子江药业/碘佛醇 50 mL:33.9 g,国药准字H20067896,江苏恒瑞)、等渗造影剂121例(碘克沙醇100 mL:65.2 g,国药准字H20103675,江苏恒瑞)。造影剂用量50~700 mL。术前血肌酐 32~474 μmol/L。术前肾功能正常252例,代偿期9例,失代偿期 14例,衰竭期 4例。造影剂个人限量超量使用43例(15.4%)。所有患者住院期间均行腔内治疗,其中VTE组150例,主要行下腔静脉滤器安置+置管溶栓术和(或)球囊扩张/支架植入术;PAD组35例,主要行下肢动脉球囊扩张+支架植入和(或)置管溶栓术;AD组67例,行主动脉覆膜支架植入术;其他疾病组27例,主要行介入栓塞术。
1.2 造影剂肾病纳入标准 根据腔内治疗前后肾功能变化分为造影剂肾病组和非造影剂肾病组。根据2011年欧洲泌尿生殖放射协会对造影剂肾病(contrast-induced nephropathy,CIN)的定义[1],本研究造影剂肾病组纳入标准 :①排除其他导致肾功能恶化的因素;②进行腔内治疗术后,72 h内血清肌酐浓度增加≥25%或≥ 44. 2 μmol/L;③术前血肌酐值取腔内治疗前最近的检验结果,术后肌酐值取腔内治疗后72 h内数值最高者;④所有患者及家属均知情同意并签署知情同意书。
1.3 相关危险因素指标 二分类变量因素包括性别、合并症(高血压、冠心病、糖尿病,造影剂类型,个人造影剂限量超量使用;四分类变量因素包括主要诊断(即需进行腔内治疗的主要疾病)分成VTE、AD、PAD和其他疾病。连续变量因素包括年龄、体重,造影剂用量,术前肾功能(血肌酐水平)。个人造影剂限量(记Vmax)计算方法[2]:Vmax=W×5/Cre(W指体重,kg;Cre术前血肌酐值,μmol/L),其中W×5≤300。
1.4 统计学方法 应用SPSS 22.0统计软件分析数据。计数资料比较采用χ2检验;计量资料比较采用t检验。CIN独立危险因素分析采用多因素逐步回归分析。P<0.05为差异有统计学意义。
2 结 果
2.1 CIN发病情况 279例行腔内治疗的血管外科患者术后发生CIN 37例,发生率为13.3%;18例术后血肌酐≥177 μmol/L(即失代偿期和衰竭期肾功能),发生率为6.5%。3例患者术后需临时血液透析治疗,但无1例需长期血透;住院期间无因CIN死亡病例。
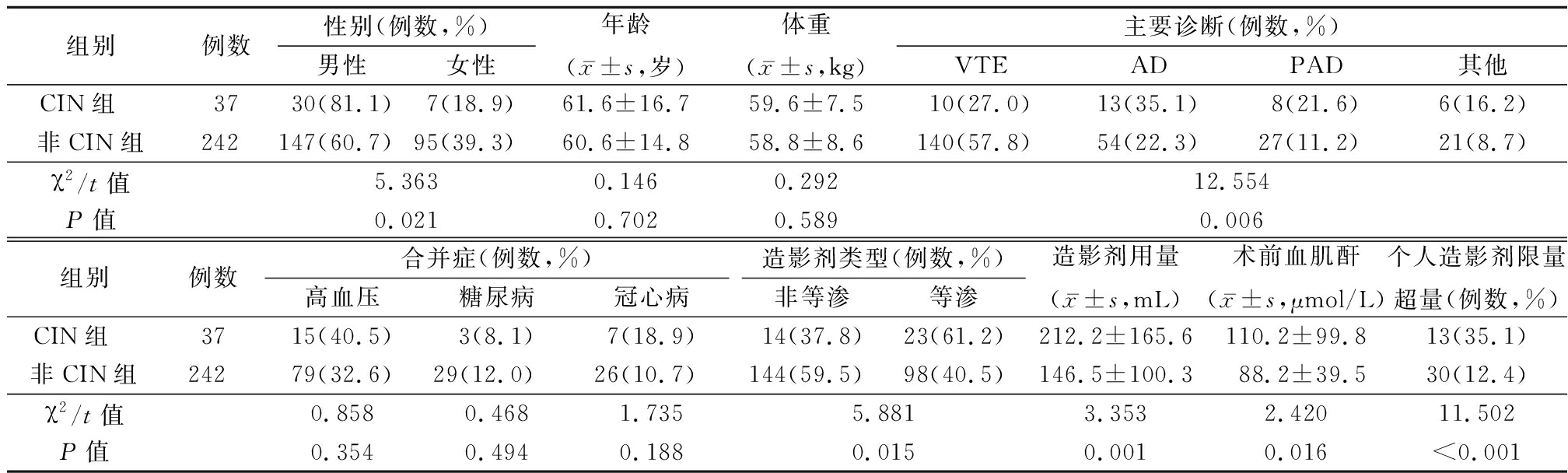
2.2 单因素分析结果 2组性别、主要诊断、造影剂类型、造影剂剂量、术前肌酐及个人造影剂限量超量使用差异有统计学意义(P<0.05);2组年龄、体重、合并症差异无统计学意义(P>0.05)。见表1。
表1 单因素分析结果
Table 1 Results of univariate analysis
组别例数性别(例数,%)男性女性年龄(x-±s,岁)体重(x-±s,kg)主要诊断(例数,%)VTEAD PAD 其他CIN组 3730(81.1)7(18.9)61.6±16.759.6±7.510(27.0)13(35.1)8(21.6)6(16.2)非CIN组242147(60.7)95(39.3)60.6±14.858.8±8.6140(57.8)54(22.3)27(11.2)21(8.7)χ2/t值5.3630.1460.29212.554P值0.0210.7020.5890.006组别例数合并症(例数,%)高血压糖尿病冠心病造影剂类型(例数,%)非等渗等渗造影剂用量(x-±s,mL)术前血肌酐(x-±s,μmol/L)个人造影剂限量超量(例数,%)CIN组 3715(40.5)3(8.1)7(18.9)14(37.8)23(61.2)212.2±165.6110.2±99.813(35.1)非CIN组24279(32.6)29(12.0)26(10.7)144(59.5)98(40.5)146.5±100.388.2±39.530(12.4)χ2/t值0.8580.4681.7355.8813.3532.42011.502P值0.3540.4940.1880.0150.0010.016<0.001
2.3 多因素分析结果 通过Wald法逐步回归分析,以造影剂肾病(是=0,否=1)为因变量,以性别(男性=0,女性=1)、主要诊断(VTE=0,AD=1,PAD=2,其分疾病=3)、造影剂类型(等渗=0,非等渗=1)、造影剂剂量(连续变量)、术前肌酐(连续变量)及个人造影剂限量超量使用(是=0,否=1)为自变量进行多因素回归分析,结果显示,个人造影剂限量超量使用是腔内治疗造影剂肾病的危险因素(P<0.05),见表2。
表2 多因素分析结果
Table 2 Results of multivariate analysis
指标回归系数标准误Waldχ2值P值OR值95%CI个人造影剂限量超量使用1.3420.39611.502<0.0013.8281.762~8.314
3 讨 论
据统计,在医院获得性肾衰竭中,CIN是仅次于手术因素、低血压的第三大常见原因,占11%;在造影剂相关的死亡事件中,造影剂相关肾衰竭或肾病是主要原因,其次是造影剂过敏[3]。CIN不仅影响原发病的治疗效果,延长住院时间,在远期随访中不良事件发生率也明显高于非CIN患者。Sun等[4]对696例行经皮冠状动脉介入治疗患者进行了平均2.79年的远期随访,发现并发CIN患者病死率高于非CIN患者,CIN是预示预后更差的独立危险因素(HR=2.79)。Zlatanovic等[5]对546例急性肢体缺血进行腔内治疗的患者进行随访分析,结果类似,CIN是预示预后更差的独立危险因素(HR=2.6)。
鉴于CIN较高的发生率、较差的预后,在使用造影剂前识别CIN的易感人群和相关危险因素并针对性采取预防措施显得尤为重要。心内科、放射科等专业对CIN进行了很多深入的研究[6-13],提示高龄、合并高血压、冠心病、糖尿病、基础肾功能、造影剂用量及低渗造影剂等是CIN可能的相关危险因素。血管外科作为新兴的进行腔内治疗的专业,对于CIN的相关研究有限。本研究将研究的群体定位于进行腔内治疗的血管外科患者,增加了主要诊断、个人造影剂限量超量使用等因素,旨在评估血管外科进行腔内治疗时CIN的发生率、相关风险因素。
本研究结果显示,CIN发生率为13%,与其他研究3%~20%发生率相仿[14-15]。2组年龄、体重、合并症差异无统计学意义(P>0.05);2组性别、主要诊断、造影剂类型、造影剂剂量、术前肾功能及个人造影剂限量超量使用差异有统计学意义(P<0.05)。男性患者CIN发生率为16.8%,明显高于女性的6.9%,这与多数的研究结果不同[16-17]。进一步分析发现,男性下肢动脉疾病百分比较女性大、造影剂平均用量较女性多、术前肾功能较女性差,所以不排除性别是通过其他因素导致CIN发生率的差异,需更多病例甚至前瞻性研究进一步明确。造影剂的类型与CIN的关系目前仍有较大争议。研究提示,等渗造影剂可减少CIN的发病率[18],而也有研究提示等渗和非等渗造影剂CIN的发生率差异无统计学意义(P>0.05)[19]。本研究结果显示,2组糖尿病、高血压及冠心病等合并症差异无统计学意义(P>0.05),与经典认识不符,原因主要考虑为本研究病例数较少,且为回顾性分析,需要进一步大宗数据、前瞻性及多中心的研究。血管外科进行腔内治疗的主要疾病有主动脉疾病、下肢动脉疾病和静脉血栓性疾病,本研究将主要诊断纳入研究因素,AD与PAD较VTE的CIN发生率明显高,且差异有统计学意义,在对AD、PAD进行腔内治疗时,应更加注意预防CIN的发生。
基础肾功能与CIN的关系在多数研究结果[12,14]一致,均提示CIN发生率随着术前血肌酐值的升高而增加。本研究以腔内治疗最近的血肌酐值表示基础肾功能,CIN组与非CIN组差异有统计学意义,CIN发生率随着术前肌酐值的增高而升高。其中,术前血肌酐≥133 μmol/L患者25例中CIN 5例,发生率为20.0%;血肌酐<133 μmol/L 254例中CIN 30例发生率为11.8%。术前血肌酐代表肾功能代偿能力,代偿能力差者发生CIN的危险性更高。
研究表明,造影剂剂量与CIN明显正相关,造影剂每增加100 mL,CIN发生率提高12%[19]。本研究结果显示,CIN组造影剂平均用量212.1 mL,而非CIN组平均用量146.5 mL,差异有统计学意义。目前对于造影剂肾病机制研究[20]中,考虑造影剂主要通过肾脏血流动力学改变、渗透效应、黏滞度的影响、对肾小管上皮的直接细胞毒性作用等环节影响肾功能。随着造影剂剂量在循环中增多,肾动脉血液和肾小管黏滞度增加,肾皮质缺血、肾小管堵塞或坏死发生率升高,这些均有可能造成肾功能的损伤。
个人造影剂限量是早期肾病专家提出的[2],根据术前的肾功能和体重计算个人最大造影剂使用量。多因素回归分析结果显示,个人造影剂限量超量使用是CIN的独立危险因素。这个因素将基础肾功能和造影剂的剂量两个因素融合成一个因素,具备更简单、有效的预测价值。通过个体化计算个人最大的造影剂使用量,根据术中造影剂用量是否超过其最大用量,对于超量使用的患者CIN的发生率更高,应更积极予以预防性措施。
血管外科在腔内治疗造影剂的用量与手术的难易程度、治疗时间相关。随着腔内治疗在主动脉弓病变、累及内脏区域腹主动脉瘤/夹层、下肢静脉血栓后遗症/支架再狭窄、下肢动脉长端闭塞病变等治疗困难疾病的应用,造影剂使用量也随着显著增多。本研究中43例超量使用造影剂的患者中,累及弓上分支病变的胸主动脉夹层/瘤7例,复杂瘤颈腹主动脉瘤6例,下肢动脉长段闭塞11例,下肢静脉血栓后遗症5例,支架再狭窄或闭塞14例。这些病例的共同特点是腔内治疗方案复杂,需反复的造影指导治疗,造影剂用量明显高于常规腔内治疗。对于这些目前腔内治疗不可避免需要大量造影剂的患者,需要更积极并针对性预防CIN的发生。
腔内治疗是血管外科学科发展的趋势,造影剂的使用甚至大剂量使用不可避免。腔内治疗前的仔细评估对预防CIN极其重要,并通过提高行业准入、增加熟练度,避免不必要增加造影剂用量等措施尽可能减少造影剂用量,特别尽量避免造影剂的超限量使用,以此减少CIN的发生。
[1] Stacul F,Van der Molen AJ,Reimer P,et al. Contrast induced nephropathy:updated ESUR contrast media safety committee guidelines[J]. Eur Radiol,2011,21(12):2527-2541.
[2] 乔树宾.心血管介入治疗高级培训教程[M].北京:人民卫生出版社,2011:28-32.
[3] Cruz DN,Goh CY,Marenzi G,et al. Renal replacement therapies for prevention of radiocontrast-induced nephropathy:a systematic review[J]. Am J Med,2012,125(1):66-78.e3.
[4] Sun G,Chen P,Wang K,et al. Contrast-induced nephropathy and long-term mortality after percutaneous coronary intervention in patients with acute myocardial infarction[J]. Angiology,2019,70(7):621-626.
[5] Zlatanovic P,Koncar I,Dragas M,et al. Combined impact of chronic kidney disease and contrast induced acute kidney injury on long-term outcomes in patients with acute lower limb ischaemia[J]. Eur J Vasc Endovasc Surg,2018,56(1):78-86.
[6] Andreucci M,Faga K,Pisani A,et al. Prevention of contrast-induced nephropathy through a knowledge of its pathogenesis and risk factors[J]. Scient World J,2014,2014:823169.
[7] Wichmann JL,Katzberg RW,Litwin SE,et al. Contrast-induced nephropathy[J]. Circulation,2015,132(20):1931-1936.
[8] 黄凯荣.冠状动脉造影和经皮冠状动脉介入治疗中造影剂肾病相关危险因素的临床观察[J].吉林医学,2018,39(9):1630-1632.
[9] Yang JP,Ran P,Chen JY,et al. Development of contrast-induced acute kidney injury after elective contrast media exposure in patients with type 2 diabetes mellitus:effect of albuminuria[J]. PLoS One,2014,9(9):e106454.
[10] 李亮,王帅,孙庆春,等.造影剂肾病影响因素Logistics回归分析[J].临床误诊误治,2017,30(6):74-76.
[11] Kawatani Y,Nakamura Y,Mochida Y,et al. Contrast medium induced nephropathy after endovascular stent graft placement:an examination of its prevalence and risk factors[J]. Radiol Res Pract,2016,2016:5950986.
[12] Han XF,Zhang XX,Liu KM,et al. Contrast- induced nephropathy in patients with diabetes mellitus between iso- and low-osmolar contrast media:a meta-analysis of full-text prospective,randomized controlled trials[J]. PLoS One,2018,13(3):e0194330.
[13] Aubry P,Brillet G,Catella L,et al. Outcomes,risk factors and health burden of contrast-induced acute kidney injury:an observational study of one million hospitalizations with inmage-guided cardiovascular procedures[J]. BMC Nephrol,2016,17(1):167.
[14] 陈文,裴源源,朱继红.急性心肌梗死行介入术发生造影剂肾病的危险因素[J].中华急诊医学杂志,2018,27(7):752.
[15] Rear R,Bell RM,Hausenloy DJ. Contrast-induced nephropathy following angiography and cardiac interventions[J]. Heart,2016,102(8):638-648.
[16] Lee J,Cho JY,Lee HJ. Contrast-induced nephropathy in patients undergoing intravenous contrast-enhanced computed tomography in korea:a multi-institutional study in 101487 patients[J]. Korean J Radiol,2014,15(4):456-463.
[17] Houben IPL,van Berlo CJLY,Bekers O,et al. Assessing the risk of contrast-induced nephropathy using a finger stick analysis in recalls from breast screening:the cinfibs explorative study[J]. Contrast Media Mol Imaging,2017,2017:5670384.
[18] Hsieh MS,Chiu CS,How CK,et al. Contrast medium exposure during computed tomography and risk of development of end-stage renal disease in patients with chronic kidney disease:a nationwide population-based,propensity score-matched,longitudinal follow-up study[J]. Medicine(Baltimore),2016,95(16):e3388.
[19] Grossman PM,Ali SS,Aronow HD,et al. Contrast-induced nephropathy in patients undergoing endovascular peripheral vascular intervention:incidence,risk factors,and outcomes as observed in the blue cross blue shield of michigan cardiovascular consortium[J]. J Interv Cardiol,2017,30(3):274-280.
[20] Yang JS,Peng YR,Tsai SC,et al. The molecular mechanism of contrast-induced nephropathy(CIN) and its link to in vitro studies on iodinated contrast media(CM)[J]. Biomedicine(Taipei),2018,8(1):1.