支气管哮喘(简称哮喘)作为当今世界范围内儿童群体中极为常见的一种慢性呼吸系统疾病,以气道慢性炎症、气道高反应性、气道重塑作为主要临床特征。相关研究显示,近年来世界范围内儿童哮喘的发病率已经高于成年群体,且呈逐年上升趋势,给儿童群体的身心健康及其家庭经济带来严重影响[1]。除遗传因素与促发因素以外,变应原也是引发儿童哮喘的主要原因,而尘螨则是其中引发儿童变应性鼻炎与支气管哮喘的主要过敏原之一。研究显示,尘螨已经成为诱发患者哮喘及增加其患症严重程度的重要因素之一[2]。基于此,加强对尘螨过敏性哮喘患儿的治疗研究,对于提升尘螨过敏性哮喘疾病治疗的临床效果、保障哮喘患儿的身心健康具有非常积极的作用。特异性治疗与非特异性治疗是当前临床针对尘螨过敏患儿常用的方案。多项研究显示,沙美特罗替卡松气雾剂在哮喘患儿的治疗中具有积极的临床疗效;同时,舌下含服粉尘螨滴剂治疗也已成为哮喘患儿特异性免疫治疗的重要方案之一[3-4]。因此,现将联合应用沙美特罗替卡松气雾剂与舌下含服粉尘螨滴剂免疫治疗方案,研究其对尘螨过敏性哮喘患儿的治疗效果,报告如下。
1 资料与方法
1.1 一般资料 选择2017年1月—2018年12月我院门诊收治的尘螨过敏性哮喘患儿85例作为研究对象,依照随机数字表法分为2组。观察组43例,男性23例,女性20例,平均年龄(7.2±1.2)岁,平均病程(13.2±3.5)个月;对照组42例,男性22例,女性20例,平均年龄(7.4±1.2)岁,平均病程(13.4±3.4)个月。2组患儿治疗前基线资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 纳入标准与排除标准 纳入标准:①患儿诊断结果均符合中华医学会呼吸病学分会哮喘学组制定的《支气管哮喘防治指南》(2020版)中的哮喘诊断标准[5];②患儿皮肤点刺试验结果显示其屋尘螨、粉尘螨血清特异性免疫球蛋白(specific immunoglobulin,SIg)E均为2级或以上;③患儿病情诊断结果均为非急性哮喘,发作时分级为轻度或中度。排除标准:①合并有严重脏器功能障碍、严重先天性脏器疾病;②身体检查结果显示其合并有严重的免疫学疾病及慢性炎症疾病;③对本研究中所用药物存在过敏性反应或者无法坚持完成所有规定疗程的患儿;④此前治疗中服用β2受体阻滞剂患儿或者哮喘病情不稳定患儿。
本研究经过我院伦理委员会批准,且与患儿家属签署知情同意书。
1.3 治疗方法 对照组患儿单独予以沙美特罗替卡松气雾剂(Laboratoire Glaxo Smith Kline生产,批号:H20140382,规格:25 μg/60揿)吸入治疗:用药剂量结合患儿实际病情设计为50 μg/100 μg,持续3个月后根据患儿病情改善情况逐渐降低用药剂量,直至病情缓解后停药。后期,若患儿病情再次发作,可重复用药并根据其实际病情调整药物剂量。
观察组患儿在对照组用药基础上予以舌下免疫治疗,使用粉尘螨滴剂1~4号(浙江我武生物科技股份有限公司生产,批号:国药准字S20060012,规格:2 mL/1瓶)作为治疗药物进行舌下含服治疗。患儿治疗前3周用药剂量为粉尘螨滴剂1号1 mg/L、粉尘螨滴剂2号10 mg/L、粉尘螨滴剂3号100 mg/L,这一治疗阶段,每周星期一至星期日分别按照1、2、3、4、6、8、10滴的顺序逐渐增加用药剂量。待第4周,使用粉尘螨滴剂4号333 mg/L(3次/d)进行维持治疗。粉尘螨滴剂治疗时,每次舌下含服1~2 min,并叮嘱患儿每次用药结束后15 min内不得饮水说话。治疗期间若患儿出现哮喘急性发作情况,则暂停用药直至哮喘病情稳定后,观察无异常可依照当前流程继续接受治疗,若哮喘再次急性发作则排除本研究。
1.4 观察指标 2组患儿均持续治疗3个月,并在治疗后接受为期1年的随访观察。(1)近期疗效[6],①显效:患儿治疗结束后咳嗽喘息等临床症状已完全消失,实验室检测结果显示第1 s用力呼气容积占预计值的百分比≥80%,随访1年内未复发;②有效:患儿治疗结束后咳嗽喘息等临床症状的发作频率及严重程度相较治疗前有明显改善,随访1年后实验室检测结果显示其第1 s用力呼气容积占预计值的百分比为50%~79%;③无效:患儿治疗结束后咳嗽喘息等临床症状的发作频率及严重程度相较治疗前无改善,实验室检测结果显示其第1 s用力呼气容积占预计值的百分比<50%。有效率=(显效例数+有效例数)/总例数×100%。(2)血清检测:使用荧光酶联免疫法检测患儿治疗前后血清尘螨SIgE、SIgG4指标变化,使用化学发光免疫分析法检测患儿治疗前后血清白细胞介素12(interleukin-12,IL-12)、IL-13指标变化。(3)症状评价:依照对哮喘症状的日间评分标准与夜间评分标准方法[7]对2组患儿治疗前后哮喘症状的病情发展进行评价,见表1。(4)不良反应:观察2组治疗期间的不良反应发生情况。
表1 哮喘症状的日间评分标准与夜间评分标准
Table 1 Daytime and nighttime scoring criteria for asthma symptoms

日间评分标准夜间评分标准分值无症状无症状0分少许症状,持续时间很短醒来一次或者早醒1分2次或者2次以上,持续时间很短醒来2次,包括早醒2分一天中较多时间有轻微症状,但是对生活和工作影响不大醒来多次3分一天较多时间症状较重,对工作和生活有影响晚上不能入睡4分
分值越高代表哮喘越严重
1.5 统计学方法 应用SPSS 22.0统计软件分析数据。计量资料比较采用独立样本t检验和配对t检验;计数资料比较采用χ2 检验。P<0.05为差异有统计学意义。
2 结 果
2.1 近期疗效 观察组治疗总有效率为93.02%明显高于对照组的76.19%,比较差异有统计学意义(P<0.05)。见表2。
表2 2组近期疗效比较
Table 2 Comparison of short-term curative effect between two groups (例数)
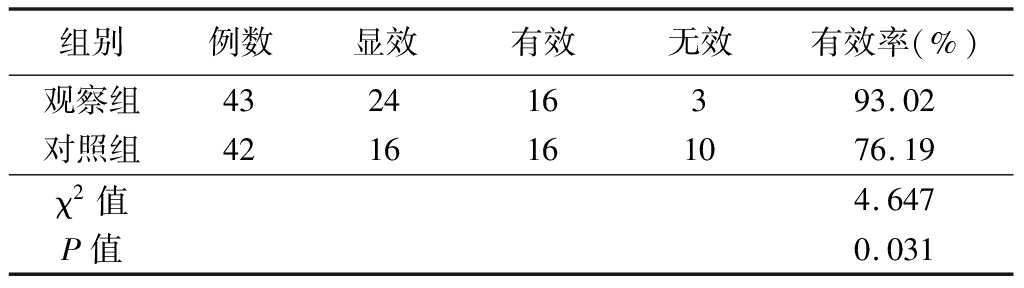
组别例数显效有效无效有效率(%)观察组432416393.02对照组4216161076.19χ2值4.647P值0.031
2.2 血清检测 2组治疗前血清尘螨SIgE、SIgG4,以及血清IL-12、IL-13水平比较差异均无统计学意义(P>0.05);治疗后观察组患儿血清尘螨SIgG4、血清IL-12水平改善明显优于对照组,组间差异有统计学意义(P<0.05)。见表3。
表3 2组血清检测结果比较
Table 3 Comparison of serum test results between two groups![]()
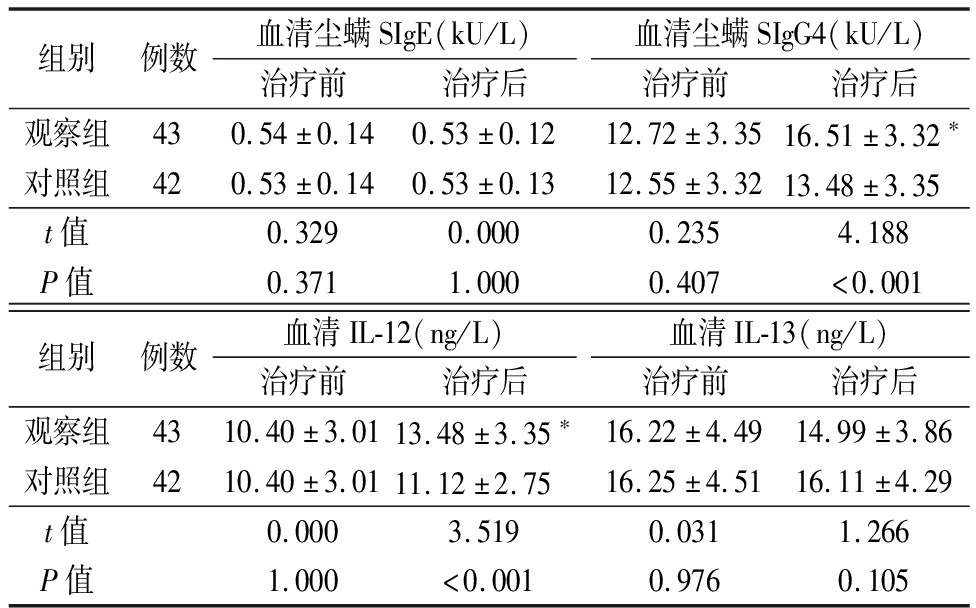
组别例数血清尘螨SIgE(kU/L)治疗前治疗后血清尘螨SIgG4(kU/L)治疗前治疗后观察组430.54±0.140.53±0.1212.72±3.3516.51±3.32∗对照组420.53±0.140.53±0.1312.55±3.3213.48±3.35 t值0.3290.0000.2354.188P值0.3711.0000.407<0.001组别例数血清IL-12(ng/L)治疗前治疗后血清IL-13(ng/L)治疗前治疗后观察组4310.40±3.0113.48±3.35∗16.22±4.4914.99±3.86对照组4210.40±3.0111.12±2.75 16.25±4.5116.11±4.29t值0.0003.5190.0311.266P值1.000<0.0010.9760.105
*P值<0.05与治疗前比较(配对t检验)
2.3 症状评价 治疗前两组患儿哮喘日间症状、夜间症状评分比较差异均无统计学意义(P>0.05);但治疗后观察组患儿哮喘日间症状及夜间症状评分均较对照组低,组间比较差异有统计学意义(P<0.05)。见表4。
表4 2组患儿症状评价结果比较
Table 4 Comparison of the evaluation results between two groups ![]() 分)
分)
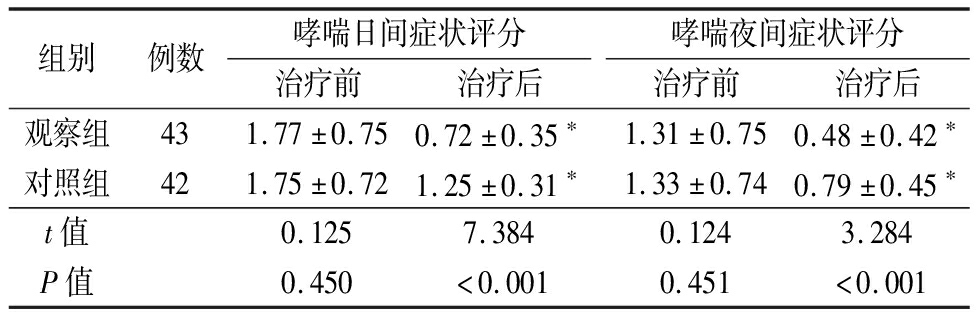
组别例数哮喘日间症状评分治疗前治疗后哮喘夜间症状评分治疗前治疗后观察组431.77±0.750.72±0.35∗1.31±0.750.48±0.42∗对照组421.75±0.721.25±0.31∗1.33±0.740.79±0.45∗t值0.1257.3840.1243.284P值0.450<0.0010.451<0.001
*P值<0.05与治疗前比较(配对t检验)
2.4 不良反应 治疗期间两组患儿均存在轻微程度的咽喉疼痛,其中观察组4例(9.30%),对照组3例(7.14%),组间比较差异无统计学意义(χ2=0.131,P=0.717)。2组患儿经过对症护理后疼痛症状有效缓解,未影响到本次研究的治疗进程。
3 讨 论
2000—2010年间我国城市范围内儿童过敏性哮喘的发病率已经由以往的1.97%增长至3.02%[8]。在此情况下,加强对过敏性哮喘患儿的治疗研究已经成为社会各界都积极关注的话题。然而由于种种原因,当前医疗领域针对哮喘疾病的治疗仍然缺乏特效方案,只能依靠长期、规范、有效的方案来控制过敏性哮喘患儿的病情发展,达到改善症状程度,降低发作频率直至不再发作的目的。其中,尘螨过敏性哮喘是一种由尘螨过敏原引发的哮喘,是过敏性哮喘中最为常见的一种类型。儿童成长阶段其成长环境中对于屋尘螨的敏感反应直接影响着哮喘疾病的发生发展,因此应当适时加强对过敏症状的治疗干预[9]。舌下免疫与皮下免疫均是针对尘螨过敏性哮喘患儿的常见治疗方法,但研究结果显示相较于皮下免疫治疗,舌下免疫方案在治疗进程中患儿免疫应答反应的出现时间更早[10]。本研究选择在常规沙美特罗替卡松气雾剂治疗的基础上联合应用粉尘螨滴剂作为舌下免疫治疗药物,以此观察和总结特异性治疗方案与非特异性治疗方案在尘螨过敏性哮喘患儿治疗中的联合应用效果。
本研究中所用沙美特罗替卡松气雾剂在尘螨过敏性哮喘患儿治疗中的应用效果已经得到广泛的研究证实,在此不再赘述。粉尘螨滴剂作为一种特异性免疫治疗类药物,其在尘螨过敏性哮喘患儿治疗中的应用能够帮助患儿产生具有特异性的阻断抗体以及免疫耐受反应,进而达到有效降低患儿过敏反应发生频率的目的。这也是本研究选择粉尘螨滴剂作为舌下免疫治疗药物的主要原因。同时,研究还发现,粉尘螨滴剂治疗尘螨过敏性哮喘时能有效调节患儿免疫功能,对患儿的治疗效果具有积极作用[11]。本研究结果也证明,采用沙美特罗替卡松气雾剂与粉尘螨滴剂舌下免疫联合治疗方案,对于尘螨过敏性哮喘患儿的临床治疗效果更为显著、积极。
然而,需要注意的是,虽然粉尘螨滴剂舌下免疫治疗方案在尘螨过敏性哮喘患儿中的应用效果已经得到广泛的研究证实[12-13],但粉尘螨滴剂舌下免疫治疗方案本身的治疗机制仍然缺乏明确的研究总结。因此本研究特针对2组患儿的血清尘螨SIgE、SIgG4指标与血清IL-12、IL-13指标进行检测对比。其中血清尘螨SIg4、SIgG4是反映患儿对尘螨变应原抗过敏反应的主要指标[14]。本研究结果中观察组患儿治疗后血清尘螨SIgE与对照组患儿比较差异无统计学意义(P>0.05),根据世界卫生组织推荐的特异性免疫治疗持续时间一般为3~6年[15],因此考虑其可能是由于患儿体内抗原特异性T淋巴细胞构象改变后,导致对抗体产生的变化需要较长时间的发展才能体现,亦或者是本研究中所用药物剂量不足以完成抗体型别的转换要求。而观察组患儿血清尘螨SIgG4指标水平在治疗后明显高于对照组,说明联合治疗方案能够有效提升尘螨过敏性哮喘患儿的SIgG4水平,使其能更早地发挥自身活性与亲和性能,从而更早地在血液中捕获相应的变应原并以此发生竞争反应,阻断肥大细胞与尘螨特异性IgE的结合,由此达到降低患儿气道炎性介质释放浓度、抑制气道炎性反应发生的治疗目的。
血清IL-12、IL-13指标是反映人体Th1/Th2细胞功能的重要指标。其中IL-12能有效促进人体内的Th0细胞逐渐向Th1细胞分化,从而降低人体气道的高反应性状态,而IL-13则是人体Th2细胞中的多功能细胞因子,能有效促进人体IgE的合成水平并诱导人体气道高反应性状态的发生。本研究中,观察组患儿治疗后血清IL-12水平相较对照组患儿明显增长,说明在患儿体内血清IL-12水平升高的情况下其Th1/Th2细胞平衡状态得到有效改善,气道高反应性得到有效调节。但患儿体内血清IL-13指标治疗后相较对照组无明显变化,猜测可能是由于本研究观察时间较短,使得尘螨过敏性哮喘患儿治疗后血清IL-13指标水平的长期变化未能得到全面观察。亦有可能是即使接受舌下免疫治疗,尘螨过敏性哮喘患儿的血清IL-13指标水平也不会发生明显变化。
综上所述,尘螨过敏性哮喘患儿接受沙美特罗替卡松气雾剂联合粉尘螨滴剂舌下免疫治疗,对改善患儿气道炎症、免疫失衡及哮喘症状均有明显效果,具有积极的临床价值。
[1] 鲍一笑,白沙沙.儿童支气管哮喘易感基因相关研究进展[J].中华实用儿科临床杂志,2019,34(4):241-244.
[2] 王万钧,鲜墨,谢燕清,等.屋尘螨鼻激发可诱发和增加不合并哮喘的过敏性鼻炎患者上下气道炎症及气道反应性[J].中华结核和呼吸杂志,2017,40(10):765.
[3] 黄羽,刘瑛.孟鲁司特对咳嗽变异性哮喘患儿Treg及Th17相关细胞因子表达的影响[J].昆明医科大学学报,2019,40(6):125-128.
[4] 丁臻博,鲁萍,黄永坤,等.孟鲁司特钠与西替利嗪联合布地奈德治疗儿童咳嗽变异性哮喘临床效果、肺功能及安全性[J].昆明医科大学学报,2020,41(3):86-90.
[5] 中华医学会呼吸病学分会哮喘学组.支气管哮喘防治指南(2020年版)[J].中华结核和呼吸杂志,2020,43(12):1023-1048.
[6] 赵雅婷,张焕萍.糖皮质激素不同给药方式对哮喘急性发作患者气道炎症的影响[J].山西医科大学学报,2019,46(9):698-700.
[7] 卞芳芳,吴月娥,龚亮,等.两种特异性免疫方案治疗尘螨过敏哮喘临床对比研究[J].临床肺科杂志,2019,24(6):1034-1038.
[8] 黄秋菊,林霞,魏欣,等.特异性免疫治疗对过敏性哮喘合并过敏性鼻炎患者的疗效分析[J].中国临床医生杂志,2019,47(3):327-329.
[9] 谢诚,艾涛,王丽,等.设下粉尘螨滴剂对儿童呼吸道过敏性疾病肺功能及气道嗜酸性验证控制水平的影响[J].四川医学,2020,41(10):18-22.
[10] 刘维,江洪,蒲红,等.评估粉尘螨舌下特异性免疫治疗对成人变应性哮喘伴鼻炎控制水平及肺功能的影响[J].临床耳鼻咽喉头颈外科杂志,2019,33(9):63-67.
[11] 武勇进,王鹏,刘智献,等.标准化粉尘螨滴剂舌下免疫治疗变应性鼻炎患儿的疗效及TGF-β和IL-13 mRNA表达水平的变化[J].临床耳鼻咽喉头颈外科杂志,2018,32(4):256-259.
[12] 王凡,付红敏,戴静毅,等.舌下特异性免疫治疗对尘螨过敏致儿童变应性咳嗽的临床疗效及安全性研究[J].实用心脑肺血管病杂志,2020,28(6):90-98.
[13] 王洁,常换换,魏苗,等.舌下含服尘螨滴剂治疗单一或多重过敏原儿童变应性鼻炎的疗效观察[J].临床耳鼻咽喉头颈外科杂志,2018,32(21):1646-1650.
[14] 薛建荣,马敬,邱昌余,等.362例变应性鼻炎患者屋尘螨皮下免疫治疗全身不良反应的观察分析[J].中华耳鼻咽喉头颈外科杂志,2020,55(5):445-451.
[15] 黄贇,刘丽娟,尹燕丹,等.标准化尘螨特异性皮下免疫治疗尘螨过敏性哮喘伴变应性鼻炎患儿的长期随访研究[J].中国循证儿科杂志,2018,13(2):93-96.